Case Report
Uniportal 完全内視鏡的後外側経椎間孔腰椎椎体間固定術
要約
このプロトコルは、FE-TLIF手順の各ステップを詳述する貴重な方法を提供します。適切な教育を受ければ、FE-TLIFを効果的に学習することができ、良好な臨床結果につながります。
要約
Uniportal 完全内視鏡的後外側腰椎椎体間固定術 (FE-TLIF) は、最近有望な結果を示しています。ただし、初心者は、より効率的で安全な手順の学習曲線を克服するために必要な技術スキルを習得する上で課題に直面する可能性があります。この研究の目標は、詳細なFE-TLIF手順を提供し、すべての方法の段階的な説明を提供すること、およびより安全で効率的な手順を確保するための主要な技術と予防措置を説明するために書かれたテキストを使用することです。脊柱管狭窄症候群と右坐骨神経痛を伴うL4-L5変性脊椎すべり症の症例を紹介します。この研究では、FE-TLIF手順の各ステップを詳述した貴重な教育用ビデオ映像を提供しています。このプロトコルには、従来のTLIF手順に共通するいくつかの器具の使用、IAP切除用のトレフィンを使用した効率的なアウトサイドイン技術、終板準備のための内視鏡的視覚化、および神経保護が組み込まれています。適切な教育を受ければ、FE-TLIFを効果的に学習することができ、合併症を最小限に抑えながら良好な臨床結果を得ることができます。
概要
腰椎固定術は、さまざまな変性腰椎疾患の標準治療と考えられています1.低侵襲脊椎手術の普及に伴い、内視鏡技術や器具の進歩により、脊椎内視鏡手術の適応が拡大しています2。内視鏡支援固定術は、最近、回復の迅速化、失血の減少、背中の筋肉損傷の最小化など、有望な結果を示しています3,4,5。ファセット温存トランスカンビン内視鏡固定術と比較して、ファセット犠牲後外側経椎間孔腰椎椎体間固定術 (TLIF) は、低侵襲管アプローチ TLIF (MIS-TLIF)、脊椎減圧中の直接視覚化、および出口が少ない神経根損傷6.
ユニポータル完全内視鏡後外側経椎間孔腰椎椎体間固定術 (FE-TLIF) は、片側バイポータル内視鏡補助 TIF (UBE-TLIF) 3,6,7 と比較して、手術技術と器具が大きく異なります。どちらの内視鏡融合技術も、術後初期および中期の転帰が同様に良好であることが示されています5,8、FE-TLIFの学習曲線は急です。初心者は、より効率的で安全な手順4の学習曲線を克服するために必要な技術的スキルを習得する上で課題に直面するかもしれません。
以下に概説するFE-TLIFのプロトコルは、KimグループとWuグループ6,7,9,10,11によって記述された技術にいくつかの変更を加えて組み込んでいます。より長いレバーアーム7を有する小型の内視鏡装置の使用に加えて、この手順は、装置の制限、特に椎間板切除術および軟骨終板準備のための器具12、ならびに隣接する処置中に特殊なケージグライダーを使用する場合の視覚化された神経保護の欠如などの課題を提示し、神経根損傷13のリスクを増大させる。Wu et al.11 は、経験豊富な外科医の手であっても、FE-TLIF を受けている 35 人の患者において、根の損傷を横断することを含む合併症率が 6% であると報告しました。逆に、Zhaoら14は、治療を受けた患者の最初の3分の1で9.6%の修正率を観察し、学習曲線中のX線曝露時間が大幅に増加しました。
これらの課題を克服するために、プロトコールでは、従来のTLIF手順に共通するいくつかの器具の使用、エンドプレート準備中の神経保護のための内視鏡的視覚化、およびケージ挿入を組み込んでいます。上記の適用可能な参考文献7,11,14に対する利点は2つありました:まず、エンドプレートシェーバー、漏斗、および標準のTLIF拡張不可能なケージなどの器具に精通していることにより、手続きの安全性が向上します。そして第二に、視覚化された神経保護により、神経構造が適切に保護されます。
本研究の目的は、FE-TLIFの手順をビデオに録画し、ビデオクリップを添えて段階的な説明を提供すること、およびより安全で効率的な手順を確保するための主要な技術と注意事項をテキストで説明することです。
ケースプレゼンテーション:
腰痛、右ふくらはぎ痛、歩行困難を呈する68歳男性をご紹介いたします。関連する症状には、右L5領域のしびれと間欠的な跛行が含まれていました。イメージングにより、脊柱管狭窄症候群を伴うL4-L5変性脊椎すべり症が明らかになりました(図1)。徹底的な話し合いの結果、患者は右 L4-L5 ユニポータル完全内視鏡的後外側経椎間孔腰椎椎体間固定術 (FE-TLIF) を予定しました。
プロトコル
本研究(Ref.202500125B0)は、台湾の長功医学基金会の治験審査委員会で承認され、適切なインフォームドコンセントが得られました。
1.ポジショニング、皮膚マーキング、および患者の準備
- 患者の位置:全身麻酔後、患者をウィルソンフレームにうつ伏せにして、わずかに屈曲させて減圧効率を向上させます。
- 以下に説明するように、透視ガイド下皮膚マーキングを実行します。
- APビューの右峡部に隣接する右側のL4経椎弓根スクリューエントリポイントを内視鏡作業ポータルとしてマークします。
注:従来の経椎弓根スクリューエントリーポイントは、通常、前後の透視図でL4椎弓根の目の近くにあります。修正されたエントリーは、より内側と尾側に配置されているため、それぞれ対側の減圧と椎間板の準備に簡単にアクセスできます。 - 他の 3 つの経椎弓根スクリュー入口点を通常の領域としてマークし、前後の透視図で両側の L4 および L5 椎弓根の眼に隣接します。
- APビューの右峡部に隣接する右側のL4経椎弓根スクリューエントリポイントを内視鏡作業ポータルとしてマークします。
- 以下の手順で手術の準備を行います。
- ポビドンヨードで背中の真ん中から臀部まで消毒を行います。
- 手術野を無菌的にドレープします。内視鏡手術の水の流出に必要なダムとウォーターバッグで術野を準備します。ウォーターバッグを灌漑ポーチとして、外科医に最も近い正方形の手術野の側面に配置します。サージカルドレープを使用して他の3つの側面を持ち上げてダムを作り、水がバッグに流れ込むようにします。最後に、防水抗菌加工の切込みドレープでセットアップを固定します。
- 器具と通常の生理食塩水袋を約2m上に吊り下げて、重力の流れを確保します。機器には、カメラシステムに接続された内視鏡、光ファイバーケーブル、灌漑チューブ、内視鏡用バリ、内視鏡用高周波アブレーターが含まれます。クランプを使用してこれらの器具をドレープにしっかりと固定し、良好な可動域を確保します。
2. 作業スペースの作成とランドマークの特定
- 以下に説明するように、内視鏡作業ポータルを設定します。
- ステップ1.2の最初のマークでメスで長さ1.2cmの縦切開を行い、その下に筋膜を広く切開することにより、内視鏡ポータルを作成します。筋膜は、皮下組織のすぐ下にある最初の固い層です。全長2.5〜3.0 cmのメスを使用して、筋膜に頭蓋と尾の切開を行います。
- 透視検査をチェックして、オブチュレーターを右側のL4峡部にドッキングします。オブチュレーターを使用して骨に接触し、透視画像でその位置を確認します。
- シリアル拡張器を取り付け、最後にオープンベベルワーキングチューブ(外径11.2mm/内径10.2mm; 図2A)。しっかりと保持したオブチュレーターをガイドとして使用しながら、拡張器を挿入します。疑わしい場合は、オブチュレーターを再配置して再度骨に接触させ、透視法を使用して位置を確認します。
- 目印を見つけるには、15°の角度の内視鏡(外径10mm)を導入します。高周波アブレーターを使用して軟部組織を解剖し、右側のL4/L5ファセットの周囲のスペースを空け、透視画像でWuとKimのポイント7を特定します(図2B-C)。バリを使用して、透視法で位置を確認した後、骨の表面を目印として作成し、見当識障害を回避します。
3. 同側減圧
- 下関節突起(IAP)の除去:アウトサイドイン技術10 を使用して、トレフィンと骨切り術を使用して、WuのポイントからKimのポイントまでIAPを効率的に除去します。トレフィンまたは骨切り口のIAP骨片が骨折した場合は、自家移植片として保存します。
- リーマー用の作業管を大きめのもの(外径12.5mm/内径11.5mm)に変更し、トレフィンを使用して下関節突起を除去する際に、作業管のシースを関節スペースに進めて安定化させます。もう一方の手で作業チューブを安定させながら、トレフィンを静かに回転させます。トレフィンのIAP骨片が骨折すると、トレフィンの回転中に骨が回転します。
- 内視鏡的骨切り術で残留IAPを取り除きます。骨片を自家移植片として保存します。
- 以下に説明するように、硬膜減圧術と同側静脈切除術を行います。
- 右 L4 の尾側椎弓板、右 L5 の頭蓋椎弓板、および上関節突起 (SAP) の内側基部を取り除くことにより、同側靭帯の起源と挿入を特定します。高速4mmダイヤモンドバリまたはKerrison Rongeurのいずれかを使用してください。
注:減圧15では、アウトサイドインの技術ではなく、インサイドアウトの技術を使用し、神経構造を減圧の解剖学的参照として使用します。 - 同側靭帯を一つずつ取り除き、内視鏡下垂体またはケリソン・ロンガーで右のL5トラバースルートルートと有孔椎間板を露出させます。
- 右 L4 の尾側椎弓板、右 L5 の頭蓋椎弓板、および上関節突起 (SAP) の内側基部を取り除くことにより、同側靭帯の起源と挿入を特定します。高速4mmダイヤモンドバリまたはKerrison Rongeurのいずれかを使用してください。
4. 対側減圧
- オーバーザトップテクニック:対側頭蓋椎弓板、尾側椎弓板、および対側椎間板が見えるまで、棘突起基部を取り外します。
- 硬膜減圧術と対側静脈切除術: 対側靭帯の起源と挿入物を取り除きます。SAPの反対側の内側基部を取り外して、左のL5トラバースルートを解放します。
- これらの構造を特定することは、最も重要なステップです。対側椎弓板の起源と挿入がはっきりと見えるまで、頭蓋椎弓板と尾椎弓板を取り除きます。解放された亜板状靭帯を、内視鏡下垂体ロンジャーまたはケリソンロンゲールのいずれかを使用して、硬膜が露出するまで慎重に抽出します。
- 亜層靭帯の外側部分は、SAPの内側基部の下に伸びています。硬膜の外側にある対側トラバースルートを保護するために、靭帯フラバムの最も外側の部分を保持しながら、SAPの内側基部を取り外します。最後に、反対側の靭帯フラバム全体を取り除きます。解剖学的な詳細については、ビデオを参照してください。
5. ディスクスペースのクリアランスとエンドプレートの準備
- 骨切り術による上関節突起の頭蓋突起の頭蓋先端を茎の頭蓋縁まで除去することにより、十分な頭蓋尾郭の入口スペースがあることを確認します。右のL5トラバースルートに近い硬膜外腔をクリアして、十分な中外側スペースがあることを確認します。
- 以下に説明するように、根の保護を横断することにより、内視鏡的椎間板切除術を行います。
- 元の作業チューブを引き出し、ハンドルと長いリップ(外径16mm/内径15mm)の大きな作業チューブに交換します。ディセクタを使用して右のL5トラバースルートを保護し、長い先端をゆっくりと回転させてトラバース神経根を引っ込めます。
- 計画されたケージのエントリーサイトでフックはさみを使用してアニュロトミーを行います。エンドプレートシェーバーは、従来の経椎間孔腰椎椎体間固定術に従って直列に挿入します。透視鏡を横投影に変更して、エンドプレートシェーバーの位置を監視します(図3A)。
- 内視鏡による可視化の下で神経構造が安全に保護されるように、作業管をしっかりと保持します。エンドプレートシェーバーが通過するように内視鏡を引き出します。各エンドプレートシェーバーを回収するときは、長い唇を回転させて神経根を解放します。内視鏡を使用して椎間板の材料を検査し、神経の状態を評価します。
- 椎間板材料と軟骨を下垂体クランプで除去し、直接可視化します。
- 以下に説明するように、試行ケージの挿入を行います。
- 軟骨下骨の点状出血を伴う所望の終盤を準備した後、ケージトライアルを連続して挿入し、L5トラバースルートを保護しながらケージサイズを決定します。
- 8 mmから1 mm刻みの連続的なケージトライアルを使用して、理想的なケージの高さを決定します(図3B)。理想的なケージサイズは、ケージトライアルを移動するために必要な張力、骨の質、および隣接するレベルの椎間板の高さに基づいて決定できます。各ケージトライアルを取り外すときは、スラップハンマーを使用して片手で軸方向の力を加え、もう一方の手でしっかりと保持する必要がある作業チューブへの衝撃を慎重に回避します。
6.骨移植とケージによる椎体間固定術
- 骨移植:作業管をしっかりと保持し、内視鏡を引き出して、骨移植漏斗が椎間板空間に通過できるようにします。漏斗状の骨移植装置を使用して、椎間板空間への理想的な配置をX線透視で確認します(図3C)。自家骨移植を挿入し、続いて人工骨代替物を順番に挿入します。
- 内視鏡による可視化の下で神経構造が安全に保護されるように、作業管をしっかりと保持します。内視鏡を引き出して、漏斗状の骨移植装置を通過させ、椎間板スペース内に配置できるようにします。最適な深さは、L5椎体の前方3分の1と半分の間にあります。
注:骨移植材料は、漏斗を介して送達し、骨移植インパクターを使用して前椎間板腔に配置できます。この手順では、脱灰骨基質パテ製の人工骨代用品2.5ccを使用しました。自家薄板チップの体積は日常的に測定されていません。ただし、通常、骨移植片の全量を挿入するには、数ラウンドの漏斗インパクションが必要です。
- 内視鏡による可視化の下で神経構造が安全に保護されるように、作業管をしっかりと保持します。内視鏡を引き出して、漏斗状の骨移植装置を通過させ、椎間板スペース内に配置できるようにします。最適な深さは、L5椎体の前方3分の1と半分の間にあります。
- 以下に説明するようにTLIFケージを挿入します。
- 従来の椎間固定ケージ(TLIFケージ、弾丸型、長さ26mm、PEEK)を挿入します。内視鏡による可視化の下で神経構造が安全に保護されるように、作業管をしっかりと保持します。内視鏡を引き出して、ケージを通過させます。ケージを後椎間板スペースに噛み合わせるときは、神経構造と終板への危険を避けるために、横方向の透視画像で位置と軸を確認してください。
- 透視法でケージの位置を確認します(図3D)。最適な位置は、ディスク領域の中央に配置されます。側面図では、ケージの後方マーカーが後椎体ラインの前方に配置されていることを確認し、前後図では、前方マーカーが棘突起と位置合わせされていることを確認します。
7. 最終チェック
- ケージを挿入した後、適切な硬膜と根の減圧のために内視鏡検査を再度使用します(図4A-C)。解放された椎間板組織や血栓を検査して取り除きます。水の流入を閉じて、硬膜と根の膨張と脈動を確認します。
- 海綿骨と硬膜外血管によって出血を止めます。出血点を検査し、無線周波数アブレーターで止めます。流入する水を閉じて、過度の出血がないか確認してください。必要に応じて止血剤を使用することができます。
8.ペディクルスクリューとロッドの応用
- 透視下で経皮的椎弓根スクリューを挿入します。ウィルソンフレームの屈曲を減らして、循環看護師によって患者の前弯を回復させます。典型的な手法で両側のL4およびL5経皮的椎弓根スクリューを挿入します(図5A-B)。
- カニューレ付き針を使用してKワイヤーを挿入します。カニューレ針を取り外したら、Kワイヤーをそのままにしておきます。軟部組織が拡張したら、カニューレ挿入された椎弓根スクリューをkワイヤーの上に置きます。相対的な尾側および内側の皮膚切開部または右のL4エントリーの皮膚の緊張を克服するには、皮下トンネルと元の皮膚切開部から別の筋膜エントリーを作成します。
- ロッドを締めて、脊椎すべり症を軽減します。ロッドを経皮的に適用し、最初に遠位ネジを取り付けます。同側のスクリュー圧縮を適用しながら、最初に遠位スクリューを締め、次に近位スクリューを締めて、脊椎すべり症のロッド縮小を行います(図5C-D)。手動でネジの圧縮を行います。経皮的スクリューシステムに関連する特殊な器具も使用できます。
9.ドレーンを挿入して層状に皮膚を閉じます
- 先端をケージ領域に差し込むように1本のHemovacドレナージチューブを挿入します(図4D)。スキンをレイヤーで閉じます。筋膜をNo.1 Vicrylで縫合し、皮下層を2-0および3-0 Vicrylで縫合します。ドレナージチューブを2-0 Vicryl縫合糸で皮膚に固定します。
結果
2024年9月から2025年3月までに当院で合計10名の患者様が脊柱管狭窄症を伴うL4-L5変性脊椎すべり症と診断され、手術を受けました。コホートには5人の男性と5人の女性が含まれ、平均年齢は67.0歳±9.27歳(範囲:52〜82歳)でした。平均手術時間は333.2分±47.25分(範囲:274〜424)でした。術後、患者は、7.2 ± 1.14 から 1.3 ± 1.34 への視覚的なアナログ スケール (0-10) で背中と脚の両方の痛みスコアの大幅な改善を報告しました。彼らは術後 1.4 日目 ± 0.52 に病棟に座ったり立ったりすることができ、2.3 日目 ± 0.82 にテイラー装具を使用して自立歩行を開始しました。ドレナージチューブは2.6日目±0.52日目に抜去され、患者は4.1日目±1.60日目に退院しました。マクナブの基準16によれば、6人の患者(60%)が優れた転帰を示し、3人目(30%)が良好な転帰を示し、1人(10%)が中程度の転帰を示しました。神経損傷、硬膜外血腫、スクリューの誤装着などの合併症はありませんでした(表1)。 図6 は、手術の2日後に撮影された症例の術後X線写真と6週間後のMRI画像を示しており、記載されているプロトコルの有効性を示しています。

図1:患者の手術画像(A)L4-L5の非対称椎間板空間の狭窄。(B、C)L4-L5 動的滑りを伴う変性脊椎すべり症。(D、E、F)MRI T2WIは、脊柱管狭窄症、SchizasグレードC.とL4-L5脊椎すべり症を示したこの図の拡大版を表示するには、ここをクリックしてください。
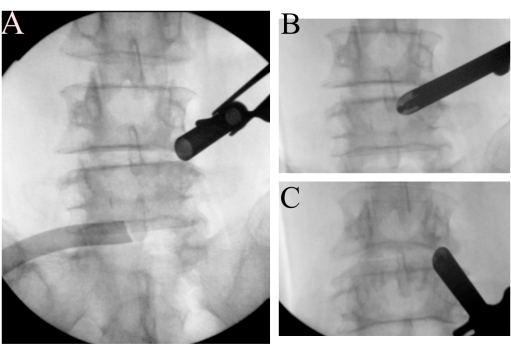
図2:ランドマークの識別。(A) 開いたベベルワーキングチューブは、右側のL4峡部にドッキングしています。(B)呉のポイントと(C)キムのポイントの特定。 この図の拡大版を表示するには、ここをクリックしてください。
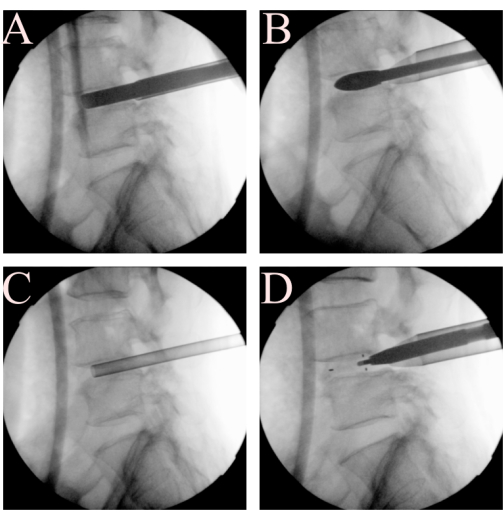
図3:ディスクとエンドプレートの手順。 椎間板スペースクリアランスのステップでは、エンドプレートの準備、(A)エンドプレートシェーバー、(B)ケージトライアル、(C)骨移植用漏斗、および(D)TLIFケージの使用。 この図の拡大版を表示するには、ここをクリックしてください。
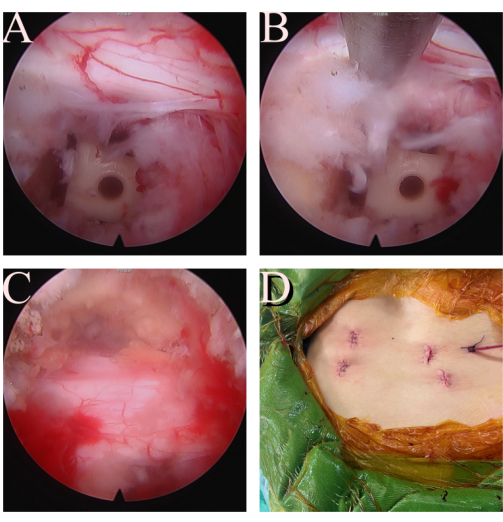
図4:最終チェック。 (A、B)L5同側トラバースルートは無傷で、十分に減圧されています。(C)硬膜と対側のL5トラバースルートも解放されます。(D)FE-TLIF手順の切開と創傷。 この図の拡大版を表示するには、ここをクリックしてください。
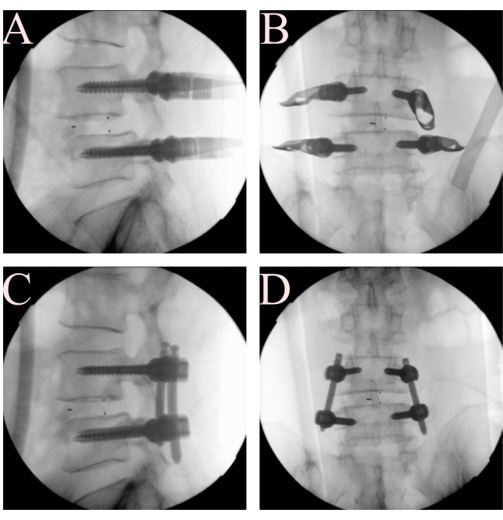
図 5.経皮的椎弓根スクリュー挿入とロッド縮小。 (A、B)椎弓根のネジとロッドを装着し、(C、D)ロッドを使用して脊椎すべり症を軽減します。 この図の拡大版を表示するには、ここをクリックしてください。
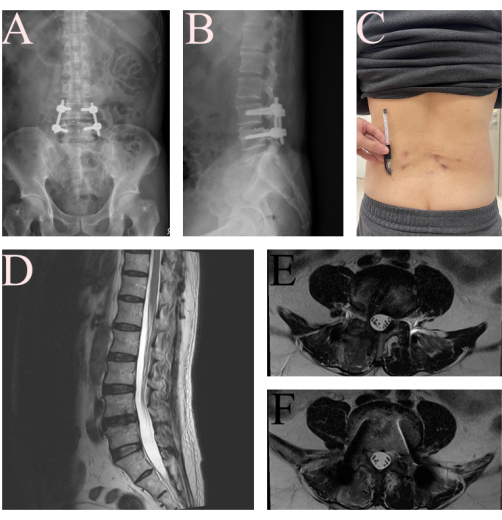
図6:FE-TLIF後の患者の術後画像。 (A) 患者の前後 (B) X 線写真で、インプラントの位置が良好で、2 日後に脊椎すべり症が縮小していることが示されています。(C)FE-TLIFの腰の傷の写真。(D、E、F)6週間後のフォローアップMRI T2WIでは、L4-L5神経構造の良好な減圧が示されました。 この図の拡大版を表示するには、ここをクリックしてください。
| パラメーター | 価値 |
| 患者数 | 10 |
| 年齢(年) | 67.0 ± 9.27 (52-82) |
| 視覚化されたアナログスケールでの術前疼痛スコア | 7.2 ± 1.14 |
| 視覚化されたアナログスケールでの術後疼痛スコア | 1.3 ± 1.34 |
| ベッド外での活動 | 1.4日目 ± 0.52 |
| 独立した歩行 | 2.3日目 ± 0.82 |
| ドレナージチューブの取り外し | 2.6日目 ± 0.52 |
| 退院 | 4.1日目 ± 1.60 |
| 操作時間(分) | 333.2 ± 47.25 (274-465) |
| 輸血の必要性 (n, %) | 1 (10%) |
| MacNab基準に基づく操作の結果(n、%) | |
| たいへん良い | 6 (60%) |
| よし | 3 (30%) |
| 市 | 1 (10%) |
| 貧しい | 0 |
| 錯綜 | |
| 硬膜外血腫 | 0 |
| デュロトミー | 0 |
| 根の損傷 | 0 |
| ネジの置き忘れ | 0 |
表1:FE-TLIFの良好な回復の代表的な結果。
ディスカッション
FE-TLIFの手順は、脊椎手術の現在の傾向が低侵襲アプローチにシフトし続けているにもかかわらず、決して簡単ではありませんでした17。この研究は、FE-TLIF技術の詳細なビデオデモンストレーションを提供する最初の研究の1つです。Zhaoら14 は、手術時間と入院期間を短縮するために25例を要したと報告した。一方、Ali et al.18 は、学習曲線が主に特定の外科的指標に影響を与えるが、内視鏡的椎間板切除術の臨床転帰には影響を与えないことを発見しました。これらの知見は、FE-TLIFが適切なトレーニングを行うことで効果的に学習し、良好な臨床結果をもたらすことができることを示しています。著者は、いくつかの国際的な専門家によるトレーニングを受け、複数のライブおよび死体コースに参加し、500を超える脊椎内視鏡手術を行ってきました。この研究では、初心者が学習曲線を克服するのに役立つシングルレベルFE-TLIFの理想的なプロトコルを共有します。
初心者は、従来の融合手術で一般的に使用される標準的な手術器具やUBE-TLIFを利用できないため、機器の制約によりFE-TLIFの実行に習熟するのに苦労することがよくあります3,19。具体的には、椎間板切除術および軟骨終板準備のための器具の設計は、ブランド間で大きく異なり、外科医の好みにも依存する12。この課題に対処するために、エンドプレートシェーバー、漏斗、ポリエーテルエーテルケトン(PEEK)拡張不可能なケージなど、従来のTLIF手順に典型的ないくつかの機器を使用しました。Du et al.19は、使い慣れた手術器具を使用することで、コストを削減し、運用効率を向上させることができることも報告しています。一部の批評家は、ディスクシェーバーとスクレーパーが過度に攻撃的であり、エンドプレートの損傷を引き起こすリスクがあると主張しています3。提示されたアプローチは、2つの重要な点を強調しています:まず、機器に精通していると手続きの安全性が向上します。第二に、手動の力とエンドプレートの状態は、使用するたびに内視鏡による視覚化を通じて注意深く監視できます。
トレフィンを使用したアウトサイドイン技術は、自家骨を維持しながらIAP切除に効果的であることが証明されました。Kim et al.10 は、IAP 除去のアウトサイドインとインサイドアウトの技術を比較し、前者の方が効率的であることを発見しました。同様に、Du et al.19 は、視覚トレフィンが効率的で便利な顔面部分切除術を可能にすると報告しました。このステップに内視鏡ドリルまたはダイヤモンドバリを使用することも効果的であるが 4,6,9,10,11 しかし、これらの方法は移植のための自家骨をあまりもたらさない可能性があり、これは X 線写真による融合を達成するための重要な要素である20,21。このため、私たちは、自家骨の保存を最大化するために、視覚トレフィンとアウトサイドイン技術の使用を提唱しています。減圧15のアウトサイドイン技術という用語について混乱がないようにしてください。これは、靭帯フラバムの一括除去前に行われる骨の減圧を指します。
隣接する手順中の視覚化された神経保護は、FE-TLIFプロトコルの重要な進歩を表しています。Kim と Wu らによって報告された技術では7、エンドプレートの準備後に専用のケージグライダーが使用され、その後の骨移植とケージ挿入は透視法によってガイドされました。著者らは、特殊な機器によって適切に保護されている場合、神経構造は完全に保護されると主張しました。それにもかかわらず、同じ研究グループは、FE-TLIFを受けた35人の患者の間で、根の損傷を横断することを含む6%の合併症率を報告しました。怪我のリスクは、より深刻な椎間板スペースの崩壊の場合に増加します9。Chang et al.13 は、FE-TLIF手順におけるケージエントリーポイントとトラバースルートの間の平均距離が3.3 mmであると報告し、この課題に対処するためのケージグライダー戦略のバリエーションを推奨しています。このプロトコルでは、長い唇を持つ作業チューブを使用して同側トラバースルートを引っ込め、手でしっかりと保持し、ケージ挿入前に安全で視覚化された神経保護を可能にしました。
それでも、手術器具には限界があり、ステップ3.1のトレフィンやリーマー用作業管など、一部の器具はリクエストに応じてのみ入手可能です。しかし、他の器具のほとんどは、脊椎フェローシップのトレーニングや基本的な脊椎内視鏡手術のコースを修了した外科医には馴染み深いものです。さらに、私たちのケース シリーズでは、症例数が限られているため、血腫、神経根損傷、スクリューの誤装着、緩みなどの合併症が発生していないため、研究にバイアスがかかる可能性があります。また、両側減圧のための片側椎弓切開術の一部のケースでは、脊椎すべり症の解剖学的縮小は必ずしも必要ではありません。臨床的意義は、神経減圧の成功に依存していますが、X線写真の縮小に依存していません。FE-TLIFのX線写真による腰椎固定率は、自家骨移植片と同種骨移植片の組み合わせを使用した場合、97.5%から100%の範囲であると報告されている19,22。自家骨移植と人工骨代替物を用いたアプローチと同様に、Tsai 氏と Liu et al.23 は FE-LIF の融合率が 100% であると報告しました。ただし、患者数が限られている小規模なケース シリーズでは、融合率はまだ利用できません。
結論として、この研究は、FE-TLIF手順の各ステップを詳述した貴重な教育用ビデオ映像を提供します。このプロトコルには、従来のTLIF手順に共通するいくつかの器具の使用、IAP切除用のトレフィンを使用した効率的なアウトサイドイン技術、終板準備のための内視鏡的視覚化、および神経保護が組み込まれています。適切な教育を受ければ、FE-TLIFを効果的に学習することができ、良好な臨床結果につながります。
開示事項
すべての著者は利益相反を開示しませんでした。
謝辞
スマートフォンと三脚を使用して手順を記録してくれたLouis Laiに感謝します。この研究は外部資金を受け取っていません。
資料
| Name | Company | Catalog Number | Comments |
| 10mm shaver | REBORN | 420-0710 | |
| 10mm trial | REBORN | 420-0610A | |
| 11mm shaver | REBORN | 420-0711 | |
| 11mm trial | REBORN | 420-0611A | |
| 12mm shaver | REBORN | 420-0712 | |
| 12mm trial | REBORN | 420-0612A | |
| 13mm shaver | REBORN | 420-0713 | |
| 13mm trial | REBORN | 420-0613A | |
| 14mm shaver | REBORN | 420-0714 | |
| 14mm trial | REBORN | 420-0614A | |
| 8mm shaver | REBORN | 420-0708 | |
| 8mm trial | REBORN | 420-0608A | |
| 9mm shaver | REBORN | 420-0709 | |
| 9mm trial | REBORN | 420-0609A | |
| Biopsy Forceps, Blakesley | JOIMAX | BFS323061 | WL 320 mm / OD 3.5 mm / JL 6.0 mm |
| Biopsy Forceps, Spoon | JOIMAX | THF322541 | WL 320 mm / OD 2.5 mm / JL 4.0 mm |
| Biopsy Forceps, Spoon, angled | JOIMAX | THF322041 | WL 320 mm / OD 2.0 mm / JL 4.0 mm / 45° |
| Bone graft impactor | REBORN | 410-1216 | |
| Dissector | JOIMAX | JDA273515 | WL 275 mm / OD 3.5 mm |
| Dissector, angled | JOIMAX | ON REQUEST | WL 280 mm / OD 3.5 mm / 40° |
| Distractor 10mm | REBORN | 420-1610 | |
| Distractor 11mm | REBORN | 420-1611 | |
| Distractor 12mm | REBORN | 420-1612 | |
| Distractor 13mm | REBORN | 420-1613 | |
| Distractor 14mm | REBORN | 420-1614 | |
| Distractor 8mm | REBORN | 420-1608 | |
| Distractor 9mm | REBORN | 420-1609 | |
| Endo-Flexprobe | JOIMAX | TEFP32020 | L 320 mm / OD 2.0 mm |
| Endo-Flexprobe Handle | JOIMAX | TEFH45025 | L 450 mm / OD 2.5 mm |
| Endo-Kerrison-Pistol Handle | JOIMAX | EKH550000 | OD 5.5 mm |
| Endo-Kerrison-Shaft | JOIMAX | EKS24551540 | WL 240 mm / OD 5.5 mm / F 1.5 mm / 40° |
| Endo-Kerrison-Shaft | JOIMAX | EKS24553040 | WL 240 mm / OD 5.5 mm / F 3.0 mm / 40° |
| Funnel for bone graft | REBORN | 410-1215 | |
| Grasper Forceps | JOIMAX | THG323555 | WL 320 mm / OD 3.5 mm / JL 5.5 mm |
| Guiding Rod, conical | JOIMAX | GRD226315 | L 225 mm / OD 6.3 mm |
| Guiding Tube, conical, red | JOIMAX | GTC177010 | L 165 mm / ID 7 mm / OD 10 mm |
| Guiding Tube, conical, violet | JOIMAX | GTC151510 | L 175 mm / ID 10 mm / OD 15 mm |
| Hook Scissor | JOIMAX | JHS243545 | WL 240 mm / OD 3.5 mm / JL 4.5 mm |
| Laminoscope | JOIMAX | LS1006125O | WL 125 mm / OD 10.0 mm / 15° / WChD 6.0 mm / 2x IC 2.0 mm |
| Lumbar implant impactor | REBORN | 420-3303 | |
| Nerve Hook | JOIMAX | TNH322533 | L 320 mm / OD 2.5 mm / JL 3.3 mm |
| Osteotome | JOIMAX | ON REQUEST | WL 260 mm / OD 5.5 mm |
| Peek lumbar 11#-14# implant driver | REBORN | 420-1715 | |
| Peek lumbar 8#-10# implant driver | REBORN | 420-1714 | |
| Reamer Push-Ejector | JOIMAX | RPE280600 | L 280 mm / OD 6.0 mm |
| Semi-Flexible Grasper Forceps, curved, up-biting | JOIMAX | TFG322522U | WL 320 mm / OD 2.5 mm / Helix |
| Slap hammer | REBORN | 420-0401B | |
| T-handle | REBORN | 460-0101A | |
| Working Reamer Tube, put endoscope into for trephining | JOIMAX | ON REQUEST | L 125 mm / ID 10.2 mm / OD 11.2 mm |
| Working Tube with Handle | JOIMAX | ON REQUEST | L 125 mm / ID 10.2 mm / OD 11.2 mm |
| Working Tube with Handle, long Lip | JOIMAX | WTS121602 | L 132 mm / ID 15 mm / OD 16 mm |
| Working Tube, use with reamer | JOIMAX | ON REQUEST | L 120 mm / ID 11.5 mm / OD 12.5 mm |
参考文献
- Ricart, P. H., Gandhi, S. D., Geisinger, J., Baker, K., Park, D. K. Clinical and ct analysis of lumbar spine arthrodesis: Beta-tricalcium phosphate versus demineralized bone matrix. J Am Acad Orthop Surg Glob Res Rev. 2 (9), e024(2018).
- Pholprajug, P., Kotheeranurak, V., Liu, Y., Kim, J. S. The endoscopic lumbar interbody fusion: A narrative review, and future perspective. Neurospine. 20 (4), 1224-1245 (2023).
- Pao, J. L. Biportal endoscopic transforaminal lumbar interbody fusion using double cages: Surgical techniques and treatment outcomes. Neurospine. 20 (1), 80-91 (2023).
- Nakajima, Y., Dezawa, A., Lim, K. T., Wu, P. H. Full-endoscopic posterior lumbar interbody fusion: A review and technical note. World Neurosurg. 189, 418-427.e3 (2024).
- Heo, D. H., Lee, D. C., Kim, H. S., Park, C. K., Chung, H. Clinical results and complications of endoscopic lumbar interbody fusion for lumbar degenerative disease: A meta-analysis. World Neurosurg. 145, 396-404 (2021).
- Kim, H. S., Wu, P. H., Sairyo, K., Jang, I. T. A narrative review of uniportal endoscopic lumbar interbody fusion: Comparison of uniportal facet-preserving trans-kambin endoscopic fusion and uniportal facet-sacrificing posterolateral transforaminal lumbar interbody fusion. Int J Spine Surg. 15 (suppl 3), S72-S83 (2021).
- Kim, H. S., Wu, P. H., Jang, I. T. Technical note on uniportal full endoscopic posterolateral approach transforaminal lumbar interbody fusion with reduction for grade 2 spondylolisthesis. Interdiscipl Neurosurg. 21, 100712(2020).
- Park, M. K., Park, S. A., Son, S. K., Park, W. W., Choi, S. H. Clinical and radiological outcomes of unilateral biportal endoscopic lumbar interbody fusion (ulif) compared with conventional posterior lumbar interbody fusion (plif): 1-year follow-up. Neurosurg Rev. 42 (3), 753-761 (2019).
- Wu, P. H., et al. Uniportal full endoscopic posterolateral transforaminal lumbar interbody fusion with endoscopic disc drilling preparation technique for symptomatic foraminal stenosis secondary to severe collapsed disc space: A clinical and computer tomographic study with technical note. Brain Sci. 10 (6), 373(2020).
- Kim, H. S., et al. Evaluation of two methods (inside-out/outside-in) inferior articular process resection for uniportal full endoscopic posterolateral transforaminal lumbar interbody fusion: Technical note. Brain Sci. 11 (9), 1169(2021).
- Wu, P. H., et al. Prospective cohort study with a 2-year follow-up of clinical results, fusion rate, and muscle bulk for uniportal full endoscopic posterolateral transforaminal lumbar interbody fusion. Asian Spine J. 17 (2), 373-381 (2023).
- Chien, K. T., et al. Optimizing disc and cartilage endplate preparation in full-endoscopic lumbar interbody fusion: An in-depth exploration of surgical instruments with a technique note and narrative review. World Neurosurg. 189, 228-247 (2024).
- Hsu, Y. C., et al. How to prevent nerve root injury in uniportal full endoscopic lumbar fusion surgery? Insights from a cadaveric anatomic study with simulation surgery. Spine. 49 (18), 1301-1310 (2024).
- Zhao, T., Dai, Z., Zhang, J., Huang, Y., Shao, H. Determining the learning curve for percutaneous endoscopic lumbar interbody fusion for lumbar degenerative diseases. J Ortho Surg Res. 18 (1), 193(2023).
- Kim, H. S., Wu, P. H., Jang, I. T. Lumbar endoscopic unilateral laminotomy for bilateral decompression outside-in approach: A proctorship guideline with 12 steps of effectiveness and safety. Neurospine. 17 (Suppl 1), S99-S109 (2020).
- Macnab, I. Negative disc exploration. An analysis of the causes of nerve-root involvement in sixty-eight patients. J Bone Joint Surg Am. 53 (5), 891-903 (1971).
- Antonacci, C. L., et al. A narrative review of endoscopic spine surgery: History, indications, uses, and future directions. J Spine Surg. 10 (2), 295-304 (2024).
- Ali, R., et al. Impact of the learning curve of percutaneous endoscopic lumbar discectomy on clinical outcomes: A systematic review. Interdiscip Neurosurg. 32, 101738(2023).
- Du, Y., et al. Full endoscopic posterolateral transarticular lumbar interbody fusion using transparent plastic working tubes: Technical note and preliminary clinical results. Front Surg. 9, 884794(2022).
- Ito, Z., et al. Bone union rate with autologous iliac bone versus local bone graft in posterior lumbar interbody fusion (plif): A multicenter study. Eur Spine J. 22 (5), 1158-1163 (2013).
- Yoo, J. S., Min, S. H., Yoon, S. H. Fusion rate according to mixture ratio and volumes of bone graft in minimally invasive transforaminal lumbar interbody fusion: Minimum 2-year follow-up. Eur J Orthop Surg Traumatol. 25 (Suppl 1), S183-S189 (2015).
- Wang, J. C., Cao, Z., Li, Z. Z., Zhao, H. L., Hou, S. X. Full-endoscopic lumbar interbody fusion versus minimally invasive transforaminal lumbar interbody fusion with a tubular retractor system: A retrospective controlled study. World Neurosurg. 165, e457-e468 (2022).
- Tsai, P. C., et al. The novel kambin torpedo full-endoscopic lumbar interbody fusion technique: A case series. Eur Spine J. 33 (2), 417-428 (2024).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved