Method Article
Nuova fusione intersomatica lombare transforaminale mini-aperta
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Il protocollo introduce un nuovo TLIF mini-aperto, che può ridurre significativamente la perdita di sangue intraoperatoria, ottenendo risultati minimamente invasivi con un recupero migliorato.
Abstract
La fusione intersomatica lombare transforaminale (TLIF) è una procedura chirurgica efficace e popolare per la gestione di varie patologie spinali, in particolare le malattie degenerative. Dall'avvento della TLIF, i chirurghi hanno perseguito tecniche minimamente invasive. Attualmente, la TLIF può essere eseguita attraverso approcci transforaminali mediante chirurgia a cielo aperto, chirurgia minimamente invasiva o endoscopia percutanea. Questo studio fornisce una descrizione dettagliata di una TLIF aperta modificata con viti peduncolari percutanee, denominata TLIF mini-aperta. L'obiettivo è quello di presentare la fattibilità di questa procedura e i suoi risultati preliminari. La procedura viene eseguita da gennaio 2021 e il numero di pazienti che soddisfano i criteri di inclusione ha superato i 300. I dati raccolti includono il tempo dell'operazione, la perdita di sangue, il tempo ambulatoriale, i livelli di ematocrito e le complicanze perioperatorie. I sintomi clinici vengono valutati a 1 settimana, 3 mesi e 12 mesi dopo l'intervento. Vengono valutati i punteggi della scala analogica visiva (VAS) per il dolore lombare e delle gambe e l'indice di disabilità di Oswestry (ODI). La risonanza magnetica viene condotta prima dell'intervento e 12 mesi dopo l'intervento per misurare l'area della sezione trasversale dei muscoli paraspinali. I tassi di fusione intersomatica lombare sono valutati mediante scansioni TC. La procedura può essere applicata alle più comuni malattie degenerative lombari nella pratica clinica. I dati attualmente raccolti indicano che il tempo medio di funzionamento per un singolo livello è stato di 102,3 min e di 130,2 min per le procedure multilivello. La perdita di sangue intraoperatoria è stata in media di 62,5 ml per gli interventi chirurgici a livello singolo e di 108,3 ml per gli interventi chirurgici a più livelli. I punteggi VAS e ODI hanno mostrato miglioramenti significativi post-operatorio (p < 0,001), ottenendo differenze clinicamente importanti minime. I tassi di atrofia muscolare paraspinale sono stati del 2,5% sul lato sintomatico e dell'1,2% sul lato asintomatico. Le variazioni delle aree della sezione trasversale e i tassi di atrofia non sono statisticamente significativi (p > 0,05). MO-TLIF è efficace e fattibile per il trattamento delle malattie degenerative lombari, soprattutto nei casi multilivello, con un danno muscolare minimo e tempi di intervento più brevi.
Introduzione
La malattia degenerativa lombare (LDD) è prevalente tra la popolazione anziana, spesso si presenta con ernia del disco lombare e stenosi spinale lombare, che si manifesta come mal di schiena cronico e sintomi neurologici1. Dalla sua introduzione negli anni '80, la fusione intersomatica lombare transforaminale (TLIF) si è evoluta e rimane una delle procedure chirurgiche più classiche e consolidate per il trattamento delle malattie degenerative lombari2. Nel 2002, Foley et al. hanno introdotto la chirurgia minimamente invasiva della fusione intersomatica lombare transforaminale (MIS-TLIF)3,4,5. Nel 2012, Osman et al. hanno riferito di aver utilizzato un endoscopio a canale singolo sulla fusione lombare 6,7. Nel 2018, Kim e Choi hanno introdotto l'endoscopia biportale unilaterale (UBE), applicandola con successo alle procedure TLIF, denominandola tlif endoscopica biportale (BE-TLIF)8.
L'adozione graduale di MIS-TLIF e PE-TLIF negli ultimi anni ha migliorato significativamente i risultati clinici e la soddisfazione dei pazienti rispetto agli interventi chirurgici tradizionali9. Alcuni studiosi ritengono addirittura che le tecniche endoscopiche finiranno per sostituire la chirurgia a cielo aperto. Tuttavia, anche la chirurgia tradizionale a cielo aperto sta migliorando continuamente e sta diventando meno invasiva, con la TLIF modificata che sta emergendo come una procedura a cielo aperto ampiamente accettata10. La TLIF modificata prevede l'incisione della fascia lombo-dorsale lungo il processo spinoso, il distacco meticoloso dei muscoli e dei legamenti attaccati al processo spinoso e la lamina sotto il periostio e l'esposizione dei peduncoli vertebrali senza dissezione estesa o retrazione prolungata. Questa tecnica raggiunge risultati minimamente invasivi simili rispetto all'approccio Wiltse11.
In questo contesto, questo studio propone in modo innovativo un ulteriore passo avanti rispetto all'approccio mini-invasivo, il TLIF MINI-OPEN (MO-TLIF), assistito da viti peduncolari percutanee. Molti studi riportano che la chirurgia lombare posteriore spesso porta all'atrofia muscolare paraspinale postoperatoria, possibilmente correlata alla retrazione prolungata dei muscoli della schiena durante l'intervento chirurgico, che è associata a lombalgia (LBP) e sintomi radicolari 12,13,14. Mengiardi et al. hanno scoperto che l'aumento dell'infiltrazione di grasso nel muscolo multifido spesso provoca dolore lombare cronico7, mentre Hyun et al. hanno suggerito un legame tra radicolopatia lombare e atrofia da denervazione muscolare12. Altri studi hanno dimostrato che l'atrofia muscolare paraspinale è strettamente correlata all'insorgenza e all'aggravamento dei sintomi della malattia degenerativa lombare15. La quantità e la funzione dei muscoli paraspinali svolgono un ruolo cruciale nel mantenimento dell'equilibrio sagittale lombo-pelvico e sono essenziali per la stabilità lombare postoperatoria16. Pertanto, l'impatto sui muscoli paraspinali è una considerazione fondamentale nella scelta dell'approccio chirurgico e della tecnica per la fusione spinale, con approcci anteriori o posteriori minimamente invasivi che riducono la disgregazione muscolare17.
Questo studio analizza in modo prospettico l'efficacia clinica a breve termine e le variazioni dei muscoli paraspinali in pazienti con degenerazione lombare a livello singolo e multilivello trattati con MO-TLIF (47 maschi e 49 femmine con un'età media compresa tra 54,8 ± 17,5 anni, come mostrato nella Tabella 1). Sono stati valutati l'efficacia chirurgica, la perdita di sangue, gli esiti della fusione, i punteggi funzionali e del dolore e l'interruzione del muscolo paraspinale, confrontando questi risultati con i pazienti sottoposti a TLIF modificata durante lo stesso periodo. Questo confronto mira a esplorare i vantaggi di MO-TLIF nel trattamento delle malattie degenerative lombari, in particolare il suo impatto sui muscoli paraspinali.
Protocollo
Questo studio è stato condotto in linea con i principi della Dichiarazione di Helsinki. L'approvazione è stata concessa dal Comitato Etico del Secondo Ospedale Affiliato dell'Università di Soochow (n. JD-LK2023045-I01). Il consenso informato è stato ottenuto da tutti i singoli partecipanti inclusi nello studio. Tutte le immagini nell'articolo hanno ottenuto il consenso informato dei partecipanti alla ricerca umana.
1. Criteri di inclusione ed esclusione
- Utilizzare i seguenti criteri di inclusione: Diagnosi clinica di ernia del disco lombare a livello singolo o multiplo, stenosi spinale lombare, instabilità lombare o spondilolistesi lombare di grado I o II; lombalgia persistente e/o dolore alle gambe, intorpidimento o debolezza che non ha risposto al trattamento conservativo per 3 mesi.
- Utilizzare i seguenti criteri di esclusione: Chirurgia di revisione; presenza di scoliosi, spondilite anchilosante, nuove fratture vertebrali, tumori spinali o altri tumori maligni; spondilolistesi lombare di grado III o superiore; pazienti con disturbi della coagulazione.
2. Procedura chirurgica
- Preparazione preoperatoria
- Posizionare tutti i pazienti sottoposti a intervento chirurgico in anestesia generale proni su un tavolo di chirurgia spinale radiotrasparente. Posizionare un cuscinetto di supporto o un cuscino di dimensioni adeguate sotto l'area toracica e pelvica per sollevare rispettivamente il torace e il bacino. Regolare con precisione l'altezza e l'angolo dei supporti per massimizzare l'esposizione intersomatica e consentire all'addome di abbassarsi liberamente per evitare la compressione inferiore della vena cava.
NOTA: Generalmente, una lordosi lombare anteriore da 10° a 15° e un'inclinazione pelvica appropriata sono considerate ottimali per ottenere la migliore esposizione dello spazio intervertebrale. Le regolazioni di precisione durante l'operazione sono fondamentali per bilanciare l'esposizione desiderata con la sicurezza del paziente. - Iniziare con l'identificazione del segmento L5-S1; utilizzare una guida alla localizzazione sotto fluoroscopia con braccio a C sulla base delle viste anteroposteriori standard per determinare il segmento della lesione e la proiezione superficiale dei peduncoli sul corpo del paziente.
- Utilizzare un pennarello per contrassegnare le incisioni chirurgiche della linea mediana, le sporgenze superficiali dei peduncoli e le incisioni di 1 cm sul margine laterale delle proiezioni peduncolari.
- Disinfettare il sito chirurgico con iodoforo in tre applicazioni separate, estendendo il disinfettante di almeno 15 cm oltre l'incisione prevista per creare un adeguato margine antisettico. Fare attenzione a non spalmare o rimuovere i segni preoperatori.
- Posizionare quattro teli sterili attorno al sito di incisione. Applicare teli chirurgici sia all'estremità cefalica che a quella caudale del campo operatorio. Coprire l'area chirurgica con un grande telo sterile, fissandolo in posizione.
- Posizionare tutti i pazienti sottoposti a intervento chirurgico in anestesia generale proni su un tavolo di chirurgia spinale radiotrasparente. Posizionare un cuscinetto di supporto o un cuscino di dimensioni adeguate sotto l'area toracica e pelvica per sollevare rispettivamente il torace e il bacino. Regolare con precisione l'altezza e l'angolo dei supporti per massimizzare l'esposizione intersomatica e consentire all'addome di abbassarsi liberamente per evitare la compressione inferiore della vena cava.
- Istituzione del canale di accesso chirurgico
- Praticare un'incisione longitudinale di 3 cm lungo la linea segnata sulla parte bassa della schiena con una lama #10 (Figura 1). Tagliare la pelle, il tessuto sottocutaneo e la fascia toracolombare con un elettrotomo ad alta frequenza in sequenza.
- Staccare i muscoli paraspinali lungo il processo spinoso per esporre il processo spinoso interessato, la lamina e parte della faccetta articolare con elettrotomo ad alta frequenza. Posizionare il divaricatore della lamina sul bordo esterno della faccetta superiore della vertebra inferiore per esporre il campo chirurgico, stabilendo in genere il canale di avvicinamento entro 5 minuti.
- Decompressione
- Utilizzare un coltello osseo a ultrasuoni o un normale coltello osseo per rimuovere il processo subarticolare superiore e parte del processo sovraspinoso inferiore. Rimuovere parte del legamento flavum ventrale per esporre la dura madre e le radici nervose. Nel frattempo, preservare il legamento flavum dorsale e il grasso epidurale per ridurre al minimo l'interruzione della normale anatomia del canale spinale.
- Se è necessaria la decompressione bilaterale o la stenosi controlaterale, inclinare il tavolo chirurgico spinale radiotrasparente verso il lato controlaterale. Rimuovere la base del processo spinoso e resecare il legamento flavum ipertrofico fino a raggiungere l'incavo laterale controlaterale. Questo approccio consente di ottenere una decompressione completa di 270°.
- Ritrarre le radici nervose e il sacco durale con un divaricatore della radice nervosa per esporre l'area operatoria. Incidere l'anulus fibroso con un bisturi #11. Rimuovere il nucleo polposo con un Kerrison e raschiare la cartilagine della placca terminale con un rongeur osseo per esporre la placca terminale ossea. Dilatare in sequenza lo spazio intervertebrale con uno scalpello a disco intervertebrale e sciacquare con soluzione fisiologica normale per ottenere l'emostasi.
- Tagliare i processi articolari asportati e una parte della lamina utilizzando un rongeur osseo per creare frammenti ossei di circa 2 mm2 di dimensione. Impacchettare una parte di questi innesti ossei nella gabbia e posizionare i frammenti rimanenti nello spazio intervertebrale. Posizionare la gabbia centralmente all'interno dello spazio intervertebrale.
- Utilizzare un coltello osseo a ultrasuoni o un normale coltello osseo per rimuovere il processo subarticolare superiore e parte del processo sovraspinoso inferiore. Rimuovere parte del legamento flavum ventrale per esporre la dura madre e le radici nervose. Nel frattempo, preservare il legamento flavum dorsale e il grasso epidurale per ridurre al minimo l'interruzione della normale anatomia del canale spinale.
- Chiusura dell'incisione
- Verificare che la posizione del dispositivo di fusione intervertebrale sia soddisfacente mediante fluoroscopia laterale e antero-posteriore. Usa uno spogliarellista neurale per sondare il sacco durale e le radici nervose per una buona mobilità, nessuna compressione e nessuna stenosi del canale spinale.
- Sciacquare lo spazio intervertebrale con una soluzione salina. Utilizzare suture riassorbibili 3-0 per chiudere lo strato fasciale con una tecnica di bloccaggio ed eseguire una sutura continua per lo strato di grasso. Sutura la pelle utilizzando graffette o punti di sutura, a seconda delle preferenze e dei requisiti clinici. Questa procedura non richiede il posizionamento di routine del drenaggio.
- Posizionamento della fissazione interna e incisione chiusa
- Praticare un'incisione di 1 cm nei siti di proiezione dei peduncoli delle vertebre sopra e sotto lo spazio intervertebrale mirato (i marcatori sono stati realizzati prima dell'intervento).
- Eseguire le seguenti procedure sotto fluoroscopia con arco a C per evitare violazioni del peduncolo o danni ai nervi circostanti. Inserire un ago da trocar affilato attraverso la pelle per accedere al peduncolo. Garantire il posizionamento preciso dell'ago nel punto di ingresso pianificato.
- Dopo il corretto posizionamento dell'ago, utilizzare un alesatore di piccolo diametro per allargare gradualmente il canale peduncolare, garantendo spazio sufficiente per la vite peduncolare. Utilizzare un sistema di guida dedicato per inserire la vite peduncolare e le bielle nel canale alesato e quindi serrare i tappi a vite. Irrigare l'incisione con soluzione fisiologica per ottenere un'emostasi completa.
- Utilizzare 3-0 punti di sutura riassorbibili per chiudere l'incisione strato per strato e coprire con una medicazione. Controllare l'attività degli arti inferiori dopo l'intervento.
NOTA: Per gli interventi chirurgici a più livelli, l'incisione posteriore della linea mediana è di circa 4 cm per due segmenti e 5 cm per tre segmenti (Figura 2). Il canale di approccio chirurgico può essere stabilito utilizzando lo stesso metodo, modificando solo la posizione del divaricatore della lamina per decomprimere più spazi intervertebrali. Estendere leggermente l'incisione a più livelli può aumentare lo spazio operatorio, rendendo la procedura più conveniente e fornendo una migliore esposizione senza aumentare significativamente traumi e sanguinamenti.
3. Valutazione clinica
- Raccogli i seguenti dati prima dell'intervento, intraoperatorio, 1 settimana dopo l'intervento, 3 mesi dopo l'intervento e 12 mesi dopo l'intervento. Registra il tempo dell'operazione, la perdita di sangue, il tempo ambulatoriale postoperatorio, il tempo di follow-up, le complicanze e i punteggi della scala analogica visiva (VAS) e dell'indice di disabilità di Oswestry (ODI), ampiamente utilizzati per il dolore lombare e degli arti inferiori18.
- Misurare la perdita di sangue visibile durante l'intervento chirurgico utilizzando una sacca di aspirazione graduata. Sottrarre il volume dei liquidi, come la soluzione fisiologica, utilizzati durante la procedura. Inoltre, stimare il volume di sangue assorbito dalla garza pesando la garza imbevuta di sangue.
- Utilizzare l'ematocrito preoperatorio e postoperatorio (Hct) per calcolare la perdita di sangue. Determinare il volume ematico stimato del paziente (EBV) utilizzando la formula di Nadler19:
EBV (mL)= [k1 x altezza (m)3 + k2 x peso (kg) + k3] x 1000]
Per i maschi: k1=0,3669, k2=0,03219, k3=0,6041. Per le femmine: k1=0,3561, k2=0,03308, k3=0,1833. - Successivamente, calcolare la perdita di sangue totale (TBL) utilizzando la formula lorda20
TBL (mL)=EBV (mL) x (HctPre−HctPost)/HctAve
dove HctPre rappresenta l'ematocrito preoperatorio, HctPost è il valore dell'ematocrito misurato il secondo giorno postoperatorio e HctAve è la media di HctPre e HctPost. - Utilizzare la radiografia laterale e la tomografia computerizzata (TC) per valutare la fusione intervertebrale21. Eseguire la risonanza magnetica (MRI) prima dell'intervento e 1 anno dopo l'intervento per emulare l'area della sezione trasversale (CSA) dei muscoli paraspinali dei segmenti della lesione. Calcolare le proprietà dell'infiltrazione di grasso con ImageJ22 (Figura 3).
4. Analisi statistica
- Confronta i punteggi VAS e ODI prima e dopo l'intervento chirurgico con un t-test a campione accoppiato. Confrontare l'area della sezione trasversale misurata con la risonanza magnetica T2WI nei segmenti operativi prima e dopo l'operazione. Tutte le analisi statistiche sono state eseguite utilizzando SPSS. I dati sono presentati come media ± deviazione standard e p < 0,05 è stato considerato significativo.
Risultati
Per il funzionamento a livello singolo (n = 50), il tempo medio di funzionamento è stato di 102,3 min (intervallo 75-160 min) e 130,2 min (intervallo 112-185 min) per gli interventi chirurgici multilivello (n = 46). La perdita media di sangue intraoperatoria per la procedura a livello singolo è stata di 62,5 ml (intervallo 35-125 ml) e per la procedura a più livelli è stata di 108,3 ml (Tabella 2). I livelli preoperatori e postoperatori di sezione trasversale (CSA) e di infiltrazione di grasso (FI) dei muscoli paraspinali bilaterali sono mostrati nella Tabella 3.
Prima dell'intervento, il CSA sul lato di decompressione era di 2088,4 ± 226,7 mm2 e sul lato controlaterale era di 2081,8 ± 238,6 mm2, senza mostrare differenze significative. A 1 anno dall'intervento, il CSA sul lato della decompressione era 2077,9 ± 225,5 mm2 e sul lato controlaterale era 2076,1 ± 235,5 mm2. Il tasso di atrofia sul lato decompressione è stato del 2,5%, mentre è stato dell'1,2% sul lato controlaterale, senza differenze statisticamente significative (p > 0,05).
Il rapporto di infiltrazione di grasso sul lato decompressivo è stato del 22,14% ± 9,21% prima dell'intervento e del 22,09% ± 9,04% dopo l'intervento. Sul lato controlaterale, il rapporto di infiltrazione di grasso era del 21,78% ± 8,71% prima dell'intervento e del 22,20% ± 9,19% dopo l'intervento. Non ci sono state differenze statisticamente significative nel confronto della CSA né prima che dopo l'intervento sullo stesso lato o tra il lato di decompressione e il lato controlaterale. Dati dettagliati sulla disgregazione del muscolo paraspinale sono forniti nella Tabella 3 e nella Tabella 4.
Questi risultati indicano che la perdita di sangue intraoperatoria in MO-TLIF è inferiore a quella della tradizionale TLIF a cielo aperto, pur essendo paragonabile a quella di BE-TLIF. La durata dell'intervento chirurgico è significativamente più breve di quella di BE-TLIF, ma simile a quella della tradizionale TLIF a cielo aperto. Inoltre, sulla base del completamento con successo di oltre 400 procedure fino ad oggi, MO-TLIF ha ridotto significativamente l'invasività muscolare, dimostrando appena un aumento del danno muscolare sul lato decompressivo rispetto al lato controlaterale.
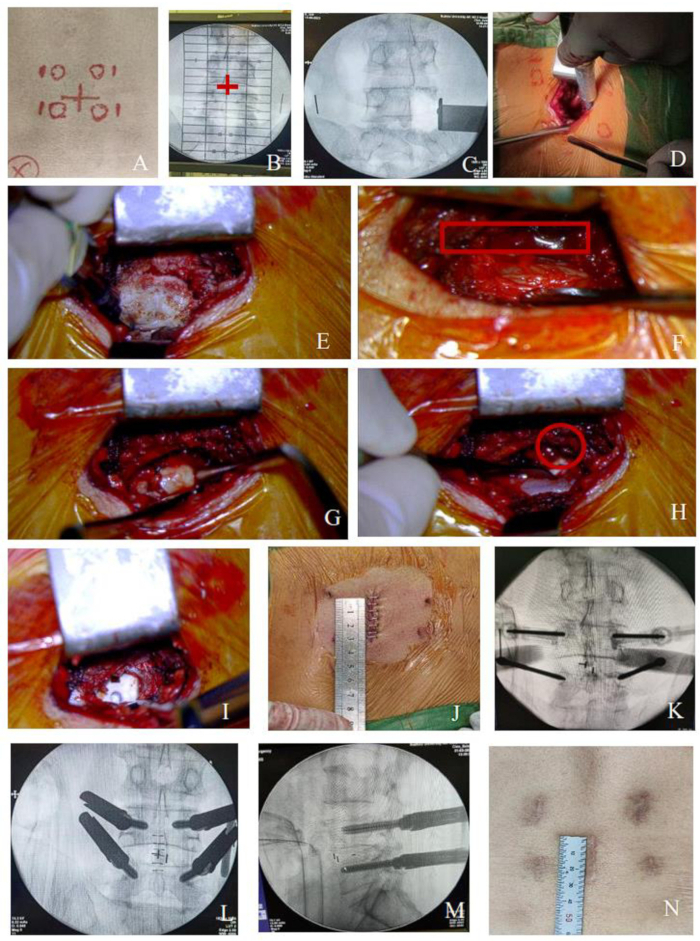
Figura 1: Procedura di MO-TLIF per la lesione a livello singolo. (A-B) Lo spazio intervertebrale e la proiezione del peduncolo sono stati determinati mediante fluoroscopia con braccio a C, come è stato dimostrato dalla croce rossa. Quindi, segnare l'incisione chirurgica lungo il processo spinoso tra i due spazi intervertebrali e 1,5 cm lateralmente al peduncolo segnare i punti di puntura delle viti peduncolari percutanee. (C-I) Diagrammi schematici del campo chirurgico durante il processo di decompressione (la radice nervosa era circondata da una linea continua rossa). (J) Incisione centrale di 3 cm per lesione a livello singolo. (K-M) Processo di posizionamento percutaneo della vite. (N) L'incisione dopo la guarigione. Clicca qui per visualizzare una versione più grande di questa figura.
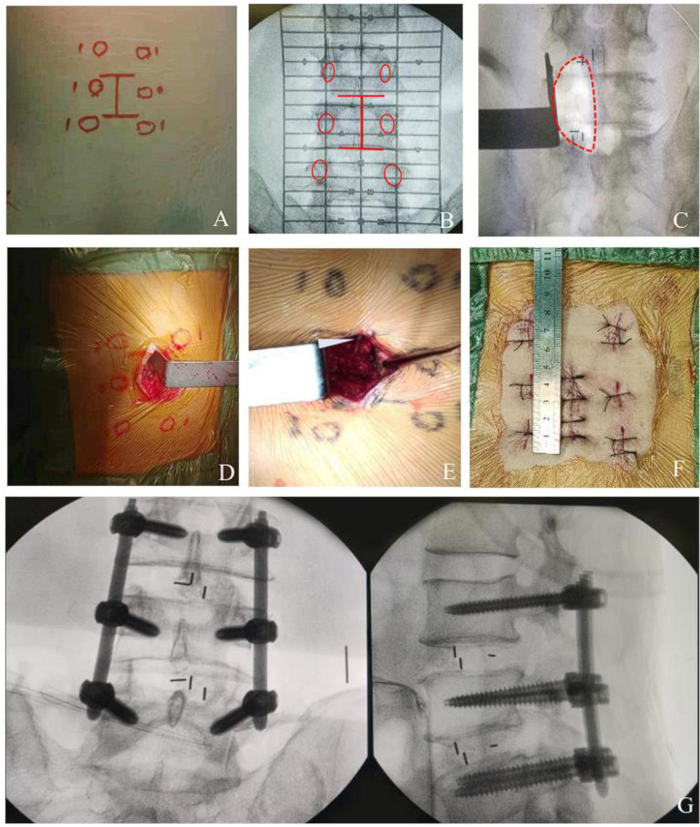
Figura 2: Procedura di MO-TLIF per lesione multilivello. (A-B) Linea di marcatura multilivello sulla pelle. (C-E) campo chirurgico di decompressione multilivello. (F) Fotografia postoperatoria che mostra l'incisione in MO-TLIF di circa 4 cm per la chirurgia a due segmenti. (G) Fotografia completata da MO-TLIF che mostra le viti peduncolari e le gabbie in posizione. Clicca qui per visualizzare una versione più grande di questa figura.
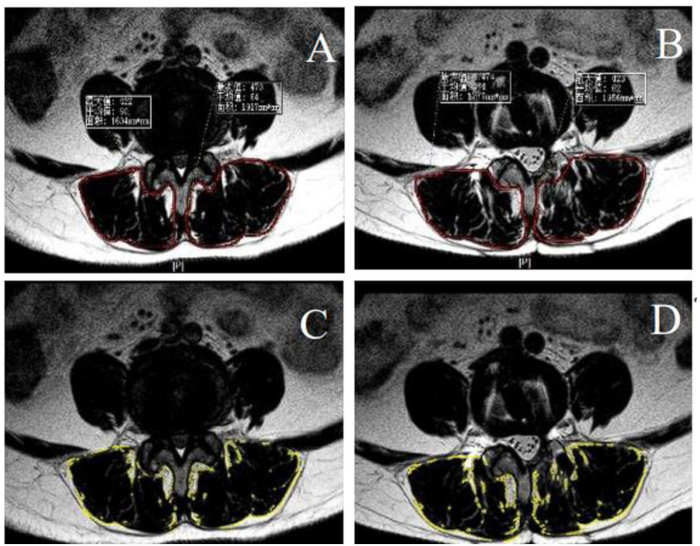
Figura 3: Infiltrazione di grasso preoperatoria e postoperatoria e area della sezione trasversale del muscolo paraspinale. (A-B) Aree della sezione trasversale preoperatoria e postoperatoria del muscolo paraspinale circondate dalla linea rossa. (C-D) L'infiltrazione di grasso preoperatoria e postoperatoria del muscolo paraspinale, calcolando le proprietà di ImageJ, è stata circondata dalla linea gialla. Clicca qui per visualizzare una versione più grande di questa figura.
| Caratteristiche | Valori |
| Età media (anni) | 54,8 ± 17,5 |
| Sesso (M/F) | 47/49 |
| Diagnosi | |
| Spondilolistesi lombare | 21 |
| Ernia del disco lombare con instabilità segmentaria | 45 |
| Stenosi foraminale lombare con instabilità segmentaria | 30 |
| BMI | 23,9 ± 2,8 |
| Livello di funzionamento | |
| A livello singolo | |
| L3-4 | 5 |
| L4-5 | 24 |
| L5-S1 | 21 |
| Multilivello | |
| L3-5 | 18 |
| L4-S1 | 24 |
| L3-S1 | 4 |
| Periodo di follow-up (mesi) | 13.2 ± 2.1 |
Tabella 1: Caratteristiche demografiche dei pazienti.
| Metriche | Livello singolo | Multilivello |
| Ematocrito preoperatorio (%) | 41,6 ± 4,8 | 42,7 ± 7,1 |
| Ematocrito postoperatorio (%) | 38,5 ± 3,4 | 38,8 ± 6,8 |
| Perdita di sangue intraoperatoria (mL) | 62,5 ± 28,2 | 108,3 ± 31,2 |
| Perdita di sangue totale stimata (mL) | 213,9 ± 124,8 | 282,8 ± 155,9 |
| Tempo di funzionamento (min) | 102,3 ± 17,2 | 130,2 ± 18,3 |
| Tempo di deambulazione postoperatoria (giorni) | 1,7 ± 0,4 | 2,0 ± 0,5 |
Tabella 2: Dati perioperatori.
| Lato | CSA (mm2) | FI (%) |
| Preoperatorio | ||
| Lato decompressione | 2088,4 ± 226,7 | 22.14 ± 9.21 |
| Lato controlaterale | 2081,8 ± 238,6 | 22.09 ± 9.04 |
| Postoperatorio | ||
| Lato decompressione | 2077,9 ± 225,5 | 21,78 ± 8,71 |
| Lato controlaterale | 2076,1 ± 235,5 | 22.20 ± 9.19 |
Tabella 3: CSA preoperatoria e postoperatoria del muscolo paraspinale e infiltrazione di grasso.
| Media ± SD (mm2) | p Valore | |
| Lato di decompressione preoperatorio - Lato controlaterale preoperatorio | 6.59 ± 36.65 | 0.081 |
| Lato decompressivo preoperatorio - Lato decompressivo postoperatorio | 10.51 ± 59.68 | 0.088 |
| Lato controlaterale preoperatorio - Lato controlaterale postoperatorio | 5.77 ± 30.84 | 0.07 |
| Lato controlaterale postoperatorio - Lato di decompressione postoperatoria | 1,85 ± 80,48 | 0.822 |
Tabella 4: Confronto efficace dei muscoli paraspinali. Tutte le analisi statistiche sono state eseguite utilizzando il test t a campione accoppiato.
Discussione
Nell'ultimo decennio, MIS-TLIF, PE-TLIF e BE-TLIF sono gradualmente diventate alternative alla tradizionale chirurgia TLIF a cielo aperto, offrendo vantaggi in termini di trauma, perdita di sangue e recupero postoperatorio23. Alcuni studiosi ritengono addirittura che la chirurgia di fusione lombare endoscopica assistita finirà per sostituire la chirurgia a cielo aperto. Tuttavia, il nostro studio mostra che anche la chirurgia TLIF a cielo aperto ha fatto progressi significativi in termini di tecniche minimamente invasive. Pur mantenendo la semplicità e l'ampia applicabilità delle tradizionali procedure aperte, ha ottenuto risultati clinici ed effetti minimamente invasivi simili alle tecniche endoscopiche minimamente invasive.
Prima dell'intervento, contrassegniamo la proiezione del peduncolo, i punti di ingresso dell'ago da puntura, lo spazio intervertebrale dei segmenti target e l'incisione chirurgica. Tuttavia, si consiglia di verificare nuovamente il segmento attraverso la fluoroscopia prima della decompressione. Questo perché anche un leggero cambiamento di angolo durante la dissezione può portare a errori segmentali, poiché abbiamo riscontrato due casi di questo tipo durante i nostri interventi chirurgici. Dopo la dissezione, un bisturi osseo a ultrasuoni viene utilizzato di routine per eseguire l'osteotomia ed esporre il canale spinale. Quando si ha a che fare con il canale spinale, è consigliabile trattenere parzialmente il legamento flavum per ridurre l'adesione cicatriziale, rimuovendo solo le porzioni eccessivamente spesse che comprimono i nervi. Se è necessaria la decompressione controlaterale del canale centrale, l'angolo del letto chirurgico può essere regolato per rimuovere parte dell'osso radicolare del processo spinoso, ottenendo la decompressione sul lato opposto. La decompressione bilaterale da incasso laterale può richiedere una dissezione bilaterale. Durante la decompressione, per motivi di sicurezza, non è necessario esporre completamente la radice uscente; Un gancio può essere utilizzato per sondare intorno alla radice nervosa e, se c'è spazio sufficiente, non è necessaria una manipolazione estesa. Dopo aver completato la decompressione e la fusione, la piccola incisione centrale può essere chiusa e possono essere posizionate viti peduncolari percutanee, che possono ridurre il tempo di retrazione sui muscoli paraspinali. In termini di selezione della gabbia, MO-TLIF può utilizzare gabbie di fusione delle stesse dimensioni del tradizionale TLIF aperto senza la necessità di gabbie più piccole o espandibili, il che aiuta a ripristinare l'altezza del disco e riduce il rischio di cedimento della gabbia24. Una meta-analisi ha suggerito che la gabbia diritta occupa un'area maggiore della piastra terminale rispetto alla gabbia a forma di banana, creando così una migliore distribuzione della pressione, che può contribuire a un tasso di cedimento inferiore25. Questo studio ha riscontrato un solo caso di cedimento della gabbia durante il follow-up. MO-TLIF può anche ottenere una decompressione esagerata sul lato controlaterale, rendendolo adatto per la laminotomia unilaterale per la decompressione bilaterale (ULBD). Ciò aumenta efficacemente l'area del canale spinale, sebbene siano necessarie ulteriori analisi statistiche per misurare i miglioramenti dell'altezza intervertebrale, degli angoli lombari e dell'area del canale spinale.
A causa delle piccole dimensioni dell'incisione centrale, non è adatto per interventi di revisione che richiedono la sostituzione della fissazione interna. Tuttavia, questo approccio rimane applicabile nella maggior parte degli altri casi. Ad esempio, negli interventi chirurgici che coinvolgono quattro segmenti, possono essere utilizzate due piccole incisioni centrali, ciascuna delle quali gestisce la decompressione di due segmenti.
La tecnica MO-TLIF può essere eseguita sotto visualizzazione diretta o con l'assistenza di strumenti visivi come lenti d'ingrandimento o microscopi. In questo studio, i pazienti sottoposti a MO-TLIF multilivello hanno mostrato buoni risultati, con un tempo medio di intervento chirurgico di 108,3 minuti e una perdita media di sangue di 130,2 ml. La limitata dissezione sottoperiostale e la minima retrazione muscolare possono proteggere i muscoli paraspinali, con conseguenti risultati clinici e impatto muscolare simili a quelli della chirurgia di fusione lombare endoscopicamente assistita.
Nel prossimo futuro, le tecniche endoscopiche o tubolari potrebbero non sostituire completamente gli approcci chirurgici aperti. MO-TLIF è in grado di eseguire una chirurgia a cielo aperto minimamente invasiva pur mantenendo i vantaggi unici della chirurgia a cielo aperto, come la comodità delle operazioni multilivello, il tempo operatorio più breve, una curva di apprendimento regolare, l'assenza di strumenti specializzati e la conservazione delle risorse idriche. La ricerca di Zhang et al. indica che il tempo operatorio per PE-TLIF è di 202 ± 31,4 minuti con perdita di sangue di 73 ± 26,4 ml, che è significativamente inferiore alla perdita di sangue intraoperatoria per MIS-TLIF (192 ± 18,9 minuti, 129 ± 31,7 ml), sebbene il tempo di intervento sia più lungodi 26 ml. Al contrario, uno studio di Xue et al. ha rilevato che il tempo operatorio per PE-TLIF (140,3 ± 35,6 min) è più breve di MIS-TLIF (170,6 ± 54,8 min), con una perdita di sangue intraoperatoria per PE-TLIF (65,6 ± 15,3 mL) inferiore a MIS-TLIF (140,5 ± 21,5 mL)27. Le differenze nel tempo dell'intervento chirurgico possono essere correlate alla competenza del chirurgo. Le meta-analisi mostrano che il tempo operatorio medio per PE-TLIF è di 155 minuti con una perdita media di sangue intraoperatoria di 101,1 ml, mentre MIS-TLIF ha un tempo operatorio medio di 181,1 minuti e una perdita di sangue intraoperatoria di 174 ml28,29.
La perdita di sangue intraoperatoria per MO-TLIF a livello singolo (64,5 ± 30,2 mL) è simile a quella di PE-TLIF e migliore di MIS-TLIF, con un tempo operatorio significativamente più breve (102,3 ± 17,2 min). MO-TLIF è vantaggioso per le operazioni a più livelli, con un'incisione a livello singolo di 3 cm estesa di 1 cm prossimalmente o distalmente per ogni livello aggiuntivo. Questo approccio consente operazioni di decompressione con un'estensione minima dell'incisione e solo un lieve aumento della perdita di sangue e del tempo dell'operazione.
In conclusione, mentre le tecniche endoscopiche minimamente invasive presentano chiari vantaggi, la continua evoluzione delle procedure aperte minimamente invasive come MO-TLIF continua a offrire vantaggi unici, mantenendo la loro rilevanza ed efficacia nella chirurgia spinale.
Divulgazioni
Gli autori non hanno conflitti di interesse da rivelare.
Riconoscimenti
Questo studio è stato sostenuto da un fondo della National Natural Science Foundation of China nel 2021 (numero di progetto: 82474251) e da un fondo del progetto scientifico e tecnologico della Suzhou Health Commission nel 2024 (numero di progetto: LCZX202307).
Materiali
| Name | Company | Catalog Number | Comments |
| Absorbable sutures | Suzhou Jiahe | VT401L | |
| Blade | KYUAN | T00100 | |
| C-arm fluoroscopy | Siemens | Siremobile Compact L | |
| High frequency electrotome | Zhejiang Huatong | 20162010692 | |
| Iodophor | Likang High-tech | 31005102 | |
| Lumbar fusion cage | Shandong Weigao | GJXT310417 | |
| Premier posterior spine minimally invasive nail rod system | Shandong Weigao | GJXT310417 | |
| Suture | MERSILK | SA86G | |
| Ultrasonic bone knife | SMTP Technology | XD860A |
Riferimenti
- Souslian, F. G., Patel, P. D. Review and analysis of modern lumbar spinal fusion techniques. Brit J Neurosurg. 38, 61-67 (2024).
- Mobbs, R. J., Phan, K., Malham, G., Seex, K., Rao, P. J. Lumbar interbody fusion: Techniques, indications and comparison of interbody fusion options including plif, tlif, mi-tlif, olif/atp, llif and alif. J Spine Surg. 1 (1), 2-18 (2015).
- Foley, K. T., Gupta, S. K., Justis, J. R., Sherman, M. C. Percutaneous pedicle screw fixation of the lumbar spine. Neurosurg Focus. 10 (4), E10(2001).
- Zhao, J., Zhang, F., Chen, X., Yao, Y. Posterior interbody fusion using a diagonal cage with unilateral transpedicular screw fixation for lumbar stenosis. J Clin Neurosci. 18 (3), 324-328 (2011).
- Foley, K. T., Lefkowitz, M. A. Advances in minimally invasive spine surgery. Clin Neurosurg. 49, 499-517 (2002).
- Kambin, P. Arthroscopic microdiscectomy. Arthroscopy. 8 (3), 287-295 (1992).
- Osman, S. G. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: A case series report. Int J Spine Surg. 6, 157-166 (2012).
- Kim, J. E., Choi, D. J. Biportal endoscopic transforaminal lumbar interbody fusion with arthroscopy. Clin Orthop Surg. 10 (2), 248-252 (2018).
- Derman, P. B., Albert, T. J. Interbody fusion techniques in the surgical management of degenerative lumbar spondylolisthesis. Curr Rev Musculoskelet Med. 10 (4), 530-538 (2017).
- Meng, F. J., et al. Comparison research of mMO-TLIF via midline approach versus MIS-TLIF via Wiltse approach for thoracolumbar surgery. Orthop J China. 28, 118-122 (2020).
- Li, S. W., et al. Comparison of mMO-TLIF via midline incision versus MIS-TLIF via Wiltse approach in lumbar degenerative disease. Indian J Orthop. 58, 1278-1287 (2024).
- Anand, N., Hamilton, J. F., Perri, B., Miraliakbar, H., Goldstein, T. Cantilever tlif with structural allograft and rhbmp2 for correction and maintenance of segmental sagittal lordosis: Long-term clinical, radiographic, and functional outcome. Spine. 31 (20), E748-E753 (2006).
- Shafaq, N., et al. Asymmetric degeneration of paravertebral muscles in patients with degenerative lumbar scoliosis. Spine. 37 (16), 1398-1406 (2012).
- Laasonen, E. M. Atrophy of sacrospinal muscle groups in patients with chronic, diffusely radiating lumbar back pain. Neuroradiology. 26 (1), 9-13 (1984).
- Hira, K., et al. Relationship of sagittal spinal alignment with low back pain and physical performance in the general population. Sci Rep. 11 (1), 20604(2021).
- Hiyama, A., et al. The correlation analysis between sagittal alignment and cross-sectional area of paraspinal muscle in patients with lumbar spinal stenosis and degenerative spondylolisthesis. BMC Musculoskelet Disord. 20 (1), 352(2019).
- Singh, K., et al. A perioperative cost analysis comparing single-level minimally invasive and open transforaminal lumbar interbody fusion. Spine J. 14 (8), 1694-1701 (2014).
- Phan, K., Rao, P. J., Kam, A. C., Mobbs, R. J. Minimally invasive versus open transforaminal lumbar interbody fusion for treatment of degenerative lumbar disease: systematic review and meta-analysis. Eur Spine J. 24 (5), 1017-1030 (2015).
- Nadler, S. B., Hidalgo, J. H., Bloch, T. Prediction of blood volume in normal human adults. Surgery. 51 (2), 224-232 (1962).
- Gross, J. B. Estimating allowable blood loss: corrected for dilution. Anesthesiology. 58 (3), 277-280 (1983).
- Bridwell, K. H., Lenke, L. G., Mcenery, K. W., Baldus, C., Blanke, K. Anterior fresh frozen structural allografts in the thoracic and lumbar spine. Spine. 20 (12), 1410-1418 (1995).
- Jacob, K. C., et al. The effect of the severity of preoperative disability on patient-reported outcomes and patient satisfaction following minimally invasive transforaminal lumbar interbody fusion. World Neurosurg. 159, E334-E346 (2022).
- Ba, Z., et al. Percutaneous endoscopical transforaminal approach versus plf to treat the single-level adjacent segment disease after plf/plif: 1-2 years follow-up. Int J Surg. 42, 22-26 (2017).
- Zhang, H., et al. Percutaneous endoscopic transforaminal lumbar interbody fusion: Technique note and comparison of early outcomes with minimally invasive transforaminal lumbar interbody fusion for lumbar spondylolisthesis. Int J Gen Med. 14, 549-558 (2021).
- Amer, S., Gaby, K., Jean, T., Khalil, K., Mohammad, D. Transforaminal lumbar interbody fusion using banana-shaped and cages: meta-analysis of and outcomes. Eur Spine J. 32, 3158-3166 (2023).
- Xue, Y. D., Diao, W. B., Ma, C., Li, J. Lumbar degenerative disease treated by percutaneous endoscopic transforaminal lumbar interbody fusion or minimally invasive surgery-transforaminal lumbar interbody fusion: A case-matched comparative study. J Orthop Surg Res. 16 (1), 696(2021).
- Zhu, L., et al. Comparison of clinical outcomes and complications between percutaneous endoscopic and minimally invasive transforaminal lumbar interbody fusion for degenerative lumbar disease: A systematic review and meta-analysis. Pain Physician. 24 (6), 441-452 (2021).
- Song, Y. F., et al. Percutaneous endoscopic versus minimally invasive transforaminal lumbar interbody fusion for lumbar degenerative diseases: A meta-analysis. Wideochir Inne Tech Maloinwazyjne. 17 (4), 591-600 (2022).
- Aoki, Y., et al. Influence of pelvic incidence-lumbar lordosis mismatch on surgical outcomes of short-segment transforaminal lumbar interbody fusion. BMC Musculoskelet Disord. 16, 213(2015).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon