Method Article
רומן מיני פתוח Transforaminal Lumbar Interbody Fusion
In This Article
Summary
הפרוטוקול מציג מיני TLIF פתוח חדשני, שיכול להפחית משמעותית את אובדן הדם תוך הניתוח, ולהשיג תוצאות זעיר פולשניות עם התאוששות משופרת.
Abstract
איחוי בין-גופני מותני טרנס-פורמינלי (TLIF) הוא הליך כירורגי יעיל ופופולרי לניהול פתולוגיות שונות בעמוד השדרה, במיוחד מחלות ניווניות. מאז הופעת TLIF, מנתחים נקטו בטכניקות זעיר פולשניות. נכון לעכשיו, ניתן לבצע TLIF באמצעות גישות טרנספורמינליות על ידי ניתוח פתוח, ניתוח זעיר פולשני או אנדוסקופיה מלעורית. מחקר זה מספק תיאור מפורט של TLIF פתוח שונה עם ברגי פדיקל מלעוריים, המכונה TLIF פתוח מיני. המטרה היא להציג את היתכנות ההליך ואת תוצאותיו הראשוניות. ההליך מבוצע מאז ינואר 2021, ומספר המטופלים העומדים בקריטריוני ההכללה עלה על 300. הנתונים שנאספו כוללים זמן ניתוח, אובדן דם, זמן אמבולטורי, רמות המטוקריט וסיבוכים סביב הניתוח. התסמינים הקליניים מוערכים לאחר שבוע, 3 חודשים ו-12 חודשים לאחר הניתוח. ציוני סולם אנלוגי חזותי (VAS) לכאבי גב תחתון ורגליים ומדד הנכות של אוסווסטרי (ODI) מוערכים. הדמיית תהודה מגנטית מתבצעת לפני הניתוח ו-12 חודשים לאחר הניתוח כדי למדוד את אזור החתך של שרירי עמוד השדרה. שיעורי האיחוי הבין-גופי המותני מוערכים באמצעות סריקות CT. ניתן ליישם את ההליך על רוב המחלות הניווניות המותניות הנפוצות בפרקטיקה הקלינית. הנתונים שנאספו כעת מצביעים על כך שזמן הפעולה הממוצע עבור רמה אחת היה 102.3 דקות ו-130.2 דקות עבור פרוצדורות מרובות רמות. אובדן הדם התוך ניתוחי עמד בממוצע על 62.5 מ"ל עבור ניתוחים חד-מפלסיים ו-108.3 מ"ל עבור ניתוחים רב-שכבתיים. ציוני VAS ו-ODI הראו שיפורים משמעותיים לאחר הניתוח (p < 0.001), והשגת הבדלים מינימליים חשובים מבחינה קלינית. שיעורי ניוון שרירי עמוד השדרה היו 2.5% בצד הסימפטומטי ו-1.2% בצד הא-סימפטומטי. שינויים בשטחי חתך ושיעורי אטרופיה אינם מובהקים סטטיסטית (עמ' > 0.05). MO-TLIF יעיל ואפשרי לטיפול במחלות ניווניות מותניות, במיוחד במקרים מרובי רמות, עם נזק מינימלי לשרירים וזמני ניתוח קצרים יותר.
Introduction
מחלה ניוונית מותנית (LDD) נפוצה בקרב האוכלוסייה המבוגרת, ולעתים קרובות מתבטאת בפריצת דיסק מותני והיצרות עמוד השדרה המותני, המתבטאת בכאבי גב כרוניים ותסמינים נוירולוגיים1. מאז הצגתו בשנות ה-80, איחוי בין-גופני מותני טרנס-פורמינלי (TLIF) התפתח ונשאר אחד ההליכים הכירורגיים הקלאסיים והמבוססים ביותר לטיפול במחלות ניווניות מותניות2. בשנת 2002, פולי ועמיתיו הציגו ניתוח זעיר פולשני איחוי בין-גופני מותני טרנספורמינלי (MIS-TLIF)3,4,5. בשנת 2012, אוסמן ועמיתיו דיווחו על שימוש באנדוסקופ חד-ערוצי, על איחוי מותני 6,7. בשנת 2018, קים וצ'וי הציגו אנדוסקופיה דו-פורטלית חד-צדדית (UBE), ויישמו אותה בהצלחה על פרוצדורות TLIF, וקראו לה TLIF (BE-TLIF)8.
האימוץ ההדרגתי של MIS-TLIF ו-PE-TLIF בשנים האחרונות שיפר משמעותית את התוצאות הקליניות ואת שביעות רצון המטופלים בהשוואה לניתוחים מסורתיים9. חלק מהחוקרים אפילו מאמינים שטכניקות אנדוסקופיות יחליפו בסופו של דבר את הניתוח הפתוח. עם זאת, ניתוח פתוח מסורתי גם משתפר ללא הרף והופך פחות פולשני, כאשר TLIF שונה מתגלה כהליך פתוח מקובל10. TLIF שונה כולל חיתוך של הפאשיה הלומבודורסלית לאורך התהליך הקוצני, ניתוק קפדני של השרירים והרצועות המחוברים לתהליך הקוצני והלמינה מתחת לפריוסטאום וחשיפת הפדיקלים החולייתיים ללא דיסקציה נרחבת או נסיגה ממושכת. טכניקה זו משיגה תוצאות זעיר פולשניות דומות בהשוואה לגישת Wiltse11.
בהקשר זה, מחקר זה מציע באופן חדשני התקדמות נוספת בגישה זעיר פולשנית, MINI-OPEN TLIF (MO-TLIF), בסיוע ברגי פדיקל מלעוריים. מחקרים רבים מדווחים כי ניתוח מותני אחורי מוביל לעתים קרובות לניוון שרירי עמוד השדרה לאחר הניתוח, אולי קשור לנסיגה ממושכת של שרירי הגב במהלך הניתוח, הקשורה לכאבי גב תחתון (LBP) ותסמינים רדיקולריים 12,13,14. Mengiardi et al. מצאו כי חדירת שומן מוגברת בשריר המולטיפידוס גורמת לעתים קרובות לכאבי גב תחתון כרוניים7, בעוד ש-Hyun et al. הציעו קשר בין רדיקולופתיה מותנית לניוון עצביםבשרירים 12. מחקרים אחרים הראו כי ניוון שרירי עמוד השדרה קשור קשר הדוק להתרחשות והחמרה של תסמיני מחלה ניוונית מותנית15. הכמות והתפקוד של שרירי עמוד השדרה ממלאים תפקיד מכריע בשמירה על איזון סגיטלי מותני-אגני והם חיוניים ליציבות המותנית לאחר הניתוח16. לכן, ההשפעה על שרירי עמוד השדרה היא שיקול קריטי בבחירת הגישה והטכניקה הכירורגית לאיחוי עמוד השדרה, כאשר גישות אחוריות קדמיות או זעיר פולשניות מפחיתות את הפרעת השרירים17.
מחקר זה מנתח באופן פרוספקטיבי את היעילות הקלינית לטווח קצר ואת השינויים בשרירי עמוד השדרה בחולים עם ניוון מותני חד-רמתי ורב-שכבתי שטופלו ב-MO-TLIF (47 גברים ו-49 נשים בגיל ממוצע של 54.8 ±-17.5 שנים, כפי שמוצג בטבלה 1). הערכנו את יעילות הניתוח, אובדן דם, תוצאות איחוי, ציוני כאב ותפקוד והפרעה בשרירים הפרה-שדרתיים, והשווינו תוצאות אלה עם מטופלים שעברו TLIF שונה באותה תקופה. השוואה זו נועדה לחקור את היתרונות של MO-TLIF בטיפול במחלות ניווניות מותניות, במיוחד השפעתו על שרירי עמוד השדרה.
Protocol
מחקר זה בוצע בהתאם לעקרונות הצהרת הלסינקי. האישור ניתן על ידי ועדת האתיקה של בית החולים המסונף השני של אוניברסיטת סוצ'ו (No. JD-LK2023045-I01). הסכמה מדעת הושגה מכל המשתתפים הבודדים שנכללו במחקר. כל התמונות במאמר קיבלו את הסכמתם המודעת של משתתפי המחקר האנושי.
1. קריטריונים להכללה ואי הכללה
- השתמש בקריטריוני ההכללה הבאים: מאובחן קלינית עם פריצת דיסק מותני ברמה אחת או רב-שכבתית, היצרות עמוד השדרה המותני, חוסר יציבות מותני, או ספונדילוליסטזיס מותני בדרגה I או II; כאבי גב תחתון מתמשכים ו/או כאבי רגליים, חוסר תחושה או חולשה שלא הגיבו לטיפול שמרני במשך 3 חודשים.
- השתמש בקריטריוני ההחרגה הבאים: ניתוח תיקון; נוכחות של עקמת, ספונדיליטיס אנקילוזינג, שברים חדשים בחוליות, גידולים בעמוד השדרה או ממאירויות אחרות; ספונדילוליסטזיס מותני בדרגה III ומעלה; חולים עם הפרעות קרישה.
2. הליך כירורגי
- הכנה לפני הניתוח
- מקם את כל המטופלים שעוברים ניתוח בהרדמה כללית על שולחן ניתוחי עמוד שדרה רדיו-לוסנטי. מקם כרית תמיכה או כרית בגודל מתאים מתחת לאזור בית החזה והאגן כדי להרים את החזה והאגן, בהתאמה. כוונן את הגובה והזווית של התומכים כדי למקסם את החשיפה הבין-גופית ולאפשר לבטן לצנוח בחופשיות כדי למנוע דחיסת וריד נבוב נחות.
הערה: בדרך כלל, לורדוזיס מותני קדמי של 10° עד 15° והטיה מתאימה של האגן נחשבים אופטימליים להשגת החשיפה הטובה ביותר לחלל הבין חולייתי. התאמות עדינות במהלך הניתוח חיוניות לאיזון בין החשיפה הרצויה לבטיחות המטופל. - התחל בזיהוי קטע L5-S1; השתמש במדריך לוקליזציה תחת פלואורוסקופיה C-arm על בסיס תצוגות אנטרופוסטריוריות סטנדרטיות כדי לקבוע את קטע הנגע ואת הקרנת פני השטח של הפדיקלים על גוף המטופל.
- השתמש בעט טוש כדי לסמן חתכים כירורגיים בקו האמצע, הקרנות פני השטח של פדיקלים, כמו גם חתכים של 1 ס"מ בשוליים הצדדיים של בליטות הפדיקל.
- יש לחטא את אתר הניתוח ביודופור בשלושה יישומים נפרדים, ולהאריך את חומר החיטוי לפחות 15 ס"מ מעבר לחתך המתוכנן כדי ליצור שוליים אנטיספטיים נאותים. הקפד לא למרוח או להסיר את הסימונים לפני הניתוח.
- הניחו ארבעה וילונות סטריליים סביב מקום החתך. החל וילונות כירורגיים הן בקצה הצפלד והן בקצה הזנב של השדה הניתוחי. מכסים את אזור הניתוח בווילון סטרילי גדול, מהדקים אותו במקומו.
- מקם את כל המטופלים שעוברים ניתוח בהרדמה כללית על שולחן ניתוחי עמוד שדרה רדיו-לוסנטי. מקם כרית תמיכה או כרית בגודל מתאים מתחת לאזור בית החזה והאגן כדי להרים את החזה והאגן, בהתאמה. כוונן את הגובה והזווית של התומכים כדי למקסם את החשיפה הבין-גופית ולאפשר לבטן לצנוח בחופשיות כדי למנוע דחיסת וריד נבוב נחות.
- הקמת תעלת הגישה הכירורגית
- בצע חתך אורכי של 3 ס"מ לאורך הקו המסומן בגב התחתון עם להב #10 (איור 1). חותכים את העור, הרקמה התת עורית ופאשיה בית החזה עם אלקטרוטומה בתדר גבוה ברצף.
- נתק את שרירי עמוד השדרה לאורך התהליך הקוצני כדי לחשוף את התהליך הקוצני הפגוע, הלמינה וחלק ממפרק הפן עם אלקטרוטומה בתדר גבוה. הנח את מפסק הלמינה בקצה החיצוני של הפן העליון של החוליה התחתונה כדי לחשוף את שדה הניתוח, בדרך כלל להקים את תעלת הגישה תוך 5 דקות.
- דקומפרסיה
- השתמש בסכין עצם אולטראסונית או בסכין עצם רגילה כדי להסיר את התהליך התת-מפרקי העליון וחלק מהתהליך העל-ספיני הנחות. הסר חלק מהרצועה הגחונית כדי לחשוף את הדורה מאטר ושורשי העצבים. בינתיים, שמור על הרצועה הגבית והשומן האפידורלי כדי למזער את ההפרעה לאנטומיה הרגילה של תעלת עמוד השדרה.
- אם נדרשת דקומפרסיה דו צדדית או היצרות נגדית, הטה את שולחן ניתוח עמוד השדרה הרדיו-לוסנט לכיוון הצד הנגדי. הסר את בסיס התהליך הקוצני וכרת את הרצועה ההיפרטרופית עד להגעה לשקע הרוחבי הנגדי. גישה זו משיגה דקומפרסיה יסודית של 270°.
- החזר את שורשי העצבים והשק הדוראלי בעזרת מפסק שורש עצב כדי לחשוף את אזור הניתוח. חתכו את טבעת הפיברוסוס בעזרת אזמל #11. הסר את הגרעין העיסה בעזרת קריסון וגרד את סחוס לוחית הקצה בעזרת רנג'ר עצם כדי לחשוף את לוחית הקצה הגרמית. הרחב ברצף את החלל הבין חולייתי בעזרת אזמל דיסק בין חולייתי ושטוף במי מלח רגילים כדי להשיג המוסטזיס.
- חתוך את התהליכים המפרקיים הכרותים וחלק מהלמינה באמצעות רונג'ר עצם ליצירת שברי עצם בגודל של כ-2 מ"מ2 . ארזו חלק משתלי העצם הללו לכלוב והניחו את השברים הנותרים בחלל הבין חולייתי. מקם את הכלוב במרכז החלל הבין חולייתי.
- השתמש בסכין עצם אולטראסונית או בסכין עצם רגילה כדי להסיר את התהליך התת-מפרקי העליון וחלק מהתהליך העל-ספיני הנחות. הסר חלק מהרצועה הגחונית כדי לחשוף את הדורה מאטר ושורשי העצבים. בינתיים, שמור על הרצועה הגבית והשומן האפידורלי כדי למזער את ההפרעה לאנטומיה הרגילה של תעלת עמוד השדרה.
- סגירת החתך
- ודא שהמיקום של מכשיר האיחוי הבין חולייתי משביע רצון על ידי פלואורוסקופיה רוחבית ואנטריו-אחורית. השתמש בחשפנית עצבית כדי לחקור את השק הדוראלי ושורשי העצבים לניידות טובה, ללא דחיסה וללא היצרות של תעלת עמוד השדרה.
- יש לשטוף את החלל הבין חולייתי בתמיסת מלח. השתמש ב-3-0 תפרים נספגים כדי לסגור את שכבת הפאשיה בטכניקת נעילה ולבצע תפירה רציפה לשכבת השומן. לתפור את העור באמצעות סיכות או תפרים, בהתאם להעדפה ולדרישות הקליניות. הליך זה אינו מצריך מיקום שגרתי של ניקוז.
- מיקום קיבוע פנימי וחתך סגור
- בצע חתך של 1 ס"מ באתרי ההקרנה של רגלי החוליות מעל ומתחת לחלל הבין חולייתי הממוקד (הסמנים נעשו לפני הניתוח).
- בצע את ההליכים הבאים תחת פלואורוסקופיה בזרוע C כדי למנוע הפרות של הפדיקל או נזק לעצבים שמסביב. הכנס מחט טרוקר חדה דרך העור כדי לגשת לפדיקול. הקפידו על מיקום מדויק של המחט בנקודת הכניסה המתוכננת.
- לאחר מיקום נכון של המחט, השתמש בקוטר קטן כדי להגדיל בהדרגה את התעלה הפדיקולרית, מה שמבטיח מספיק מקום לבורג הפדיקל. השתמש במערכת הנחיה ייעודית כדי להכניס את בורג הפדיקל ומוטות החיבור לתעלה המשופעת ולאחר מכן הדק את מכסי הברגים. להשקות את החתך במי מלח כדי להשיג המוסטזיס ביסודיות.
- השתמש ב-3-0 תפרים נספגים כדי לסגור את החתך שכבה אחר שכבה ולכסות בתחבושת. בדוק את פעילות הגפיים התחתונות לאחר הניתוח.
הערה: עבור ניתוחים רב-מפלסיים, חתך קו האמצע האחורי הוא כ-4 ס"מ לשני מקטעים ו-5 ס"מ לשלושה מקטעים (איור 2). ניתן ליצור את ערוץ הגישה הכירורגית באותה שיטה, רק לשנות את מיקום מפסק הלמינה כדי לשחרר דחיסת חללים בין-חולייתיים מרובים. הארכה קלה של החתך הרב-מפלסי יכולה להגדיל את שטח הניתוח, להפוך את ההליך לנוח יותר ולספק חשיפה טובה יותר מבלי להגדיל משמעותית את הטראומה והדימום.
3. הערכה קלינית
- אסוף את הנתונים הבאים לפני הניתוח, תוך כדי הניתוח, שבוע לאחר הניתוח, 3 חודשים לאחר הניתוח ו-12 חודשים לאחר הניתוח. רשום את זמן הניתוח, אובדן דם, זמן אמבולטורי לאחר הניתוח, זמן מעקב, סיבוכים וציוני סולם אנלוגי חזותי (VAS) ומדד הנכות של אוסווסטרי (ODI), הנמצאים בשימוש נרחב לכאבי מותניים וגפיים תחתונות18.
- מדוד את אובדן הדם הנראה לעין במהלך הניתוח באמצעות שקית יניקה מדורגת. הפחיתו את נפח הנוזלים, כגון מי מלח, המשמשים במהלך ההליך. בנוסף, העריכו את נפח הדם הנספג על ידי הגזה על ידי שקילת הגזה הספוגה בדם.
- השתמש בהמטוקריט לפני ואחרי הניתוח (Hct) כדי לחשב את אובדן הדם. קבע את נפח הדם המשוער של המטופל (EBV) באמצעות נוסחת נדלר19:
EBV (מ"ל) = [k1 x גובה (מ')3 + k2 x משקל (ק"ג) + k3] x 1000]
לגברים: k1=0.3669, k2=0.03219, k3=0.6041. לנקבות: k1=0.3561, k2=0.03308, k3=0.1833. - לאחר מכן, חשב את אובדן הדם הכולל (TBL) באמצעות הנוסחה ברוטו20
TBL (mL)=EBV (mL) x (HctPre−HctPost)/HctAve
כאשר HctPre מייצג את ההמטוקריט לפני הניתוח, HctPost הוא ערך ההמטוקריט הנמדד ביום השני לאחר הניתוח, ו-HctAve הוא הממוצע של HctPre ו-HctPost. - השתמש ברדיוגרפיה רוחבית וטומוגרפיה ממוחשבת (CT) כדי להעריך איחוי בין-חולייתי21. בצע הדמיית תהודה מגנטית (MRI) לפני הניתוח ושנה לאחר הניתוח כדי לחקות שטח חתך (CSA) של שרירי עמוד השדרה של מקטעי הנגע. חשב את המאפיינים של חדירת שומן על ידי ImageJ22 (איור 3).
4. ניתוח סטטיסטי
- השווה ציוני VAS ו-ODI לפני ואחרי הניתוח על ידי מבחן t מדגם זוגי. השווה את שטח החתך שנמדד עם MRI T2WI בקטעים תפעוליים לפני ואחרי הפעולה. כל הניתוחים הסטטיסטיים בוצעו באמצעות SPSS. הנתונים מוצגים כממוצע ± סטיית תקן, ו-p < 0.05 נחשב מובהק.
תוצאות
עבור ניתוח ברמה אחת (n = 50), זמן הניתוח הממוצע היה 102.3 דקות (טווח 75-160 דקות) ו-130.2 דקות (טווח 112-185 דקות) עבור ניתוחים רב-שכבתיים (n = 46). אובדן הדם הממוצע תוך ניתוחי עבור ההליך החד-מפלסי היה 62.5 מ"ל (טווח 35-125 מ"ל), ועבור ההליך הרב-שכבתי הוא היה 108.3 מ"ל (טבלה 2). אזורי החתך לפני ואחרי הניתוח (CSA) ורמות חדירת השומן (FI) של שרירי עמוד השדרה הדו-צדדיים מוצגים בטבלה 3.
לפני הניתוח, ה-CSA בצד הדקומפרסיה היה 2088.4 ±-226.7 מ"מ2, ובצד הנגדי הוא היה 2081.8 ±-238.6 מ"מ2, מה שלא הראה הבדל משמעותי. שנה לאחר הניתוח, ה-CSA בצד הדקומפרסיה היה 2077.9 ±-225.5 מ"מ2, ובצד הנגדי הוא היה 2076.1 ±-235.5 מ"מ2. שיעור הניוון בצד הדקומפרסיה היה 2.5%, בעוד שהוא היה 1.2% בצד הנגדי, ללא הבדל מובהק סטטיסטית (p > 0.05).
יחס חדירת השומן בצד הדקומפרסיה היה 22.14% ±-9.21% לפני הניתוח ו-22.09% ±-9.04% לאחר הניתוח. בצד הנגדי, יחס חדירת השומן היה 21.78% ±-8.71% לפני הניתוח ו-22.20% ±-9.19% לאחר הניתוח. לא היו הבדלים מובהקים סטטיסטית בהשוואת CSA לפני ואחרי הניתוח באותו צד או בין צד הדקומפרסיה לצד הנגדי. נתונים מפורטים על הפרעה בשרירי עמוד השדרה מסופקים בטבלה 3 ובטבלה 4.
תוצאות אלו מצביעות על כך שאיבוד הדם תוך ניתוחי ב-MO-TLIF נמוך מזה של TLIF פתוח מסורתי תוך השוואה לזה של BE-TLIF. משך הניתוח קצר משמעותית מזה של BE-TLIF אך דומה לזה של TLIF פתוח מסורתי. יתר על כן, בהתבסס על השלמה מוצלחת של למעלה מ-400 הליכים עד כה, MO-TLIF הפחית משמעותית את פולשניות השרירים, והדגים בקושי עלייה בנזק לשרירים בצד הדקומפרסיה בהשוואה לצד הנגדי.
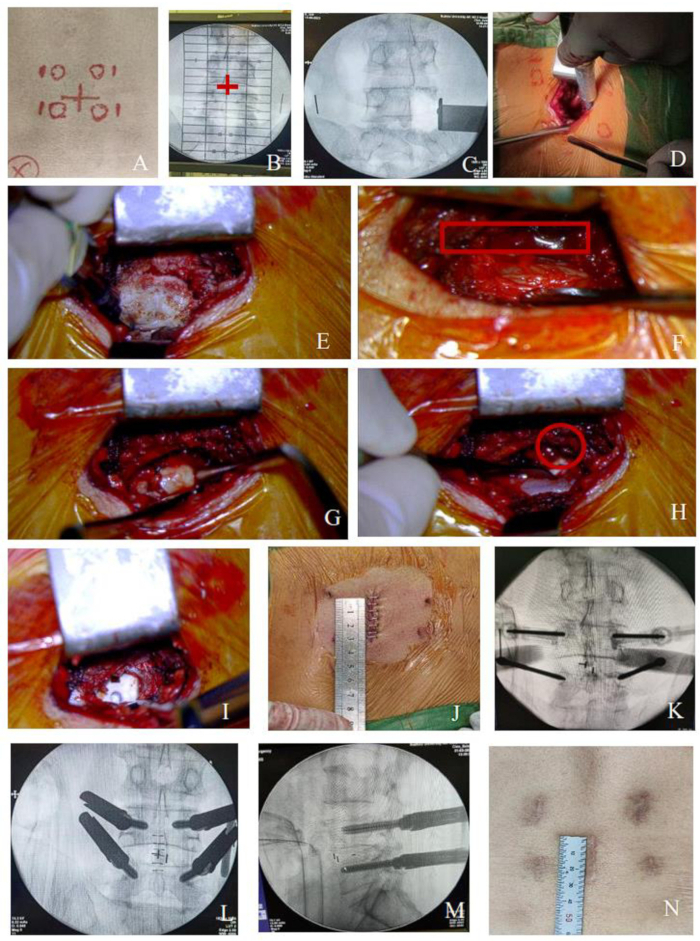
איור 1: נוהל MO-TLIF עבור הנגע החד-מפלסי. (A-B) המרחב הבין חולייתי וההקרנה של הפדיקל נקבעו תחת פלואורוסקופיה C-arm, כפי שהוצג על ידי הצלב האדום. לאחר מכן, סמנו את החתך הניתוחי לאורך התהליך הקוצני בין שני החללים הבין חולייתיים ו-1.5 ס"מ לרוחב הפדיקל סמנו את נקודות הניקוב של ברגי פדיקל מלעוריים. (ג-י) דיאגרמות סכמטיות של השדה הניתוחי בתהליך הדקומפרסיה (שורש העצב הוקף בקו מוצק אדום). (J) חתך מרכזי של 3 ס"מ לנגע חד-מפלסי. (ק-מ) תהליך הנחת בורג מלעורית. (N) החתך לאחר הריפוי. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
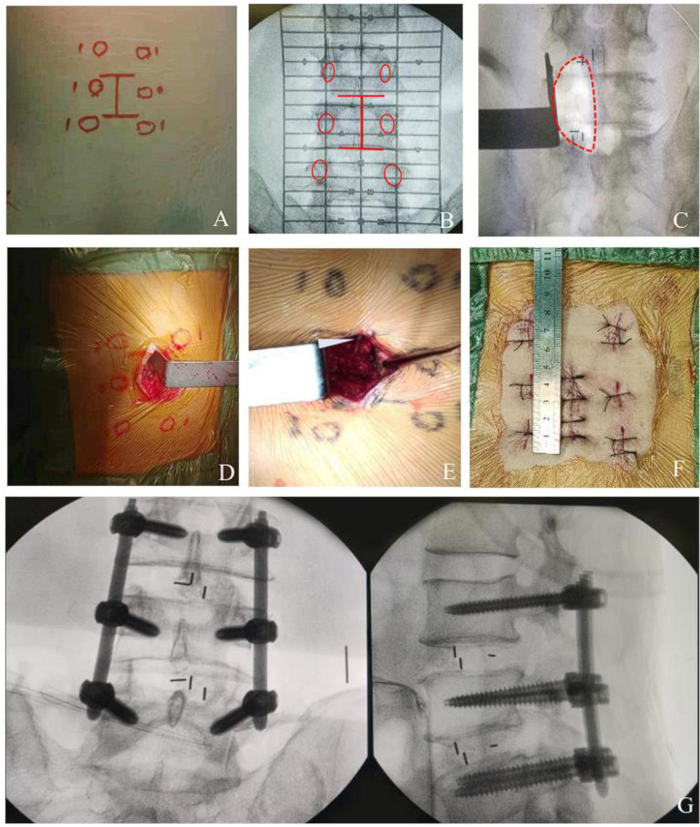
איור 2: נוהל MO-TLIF לנגע רב-שכבתי. (A-B) קו סימון רב-מפלסי על העור. (C-E) שדה כירורגי של דקומפרסיה רב-שכבתית. (F) תצלום לאחר הניתוח שמראה את החתך ב-MO-TLIF כ-4 ס"מ עבור ניתוח דו-מקטעים. (ז) תצלום כפי שהושלם ב-MO-TLIF המציג ברגים וכלובים של פדיקל במקומם. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
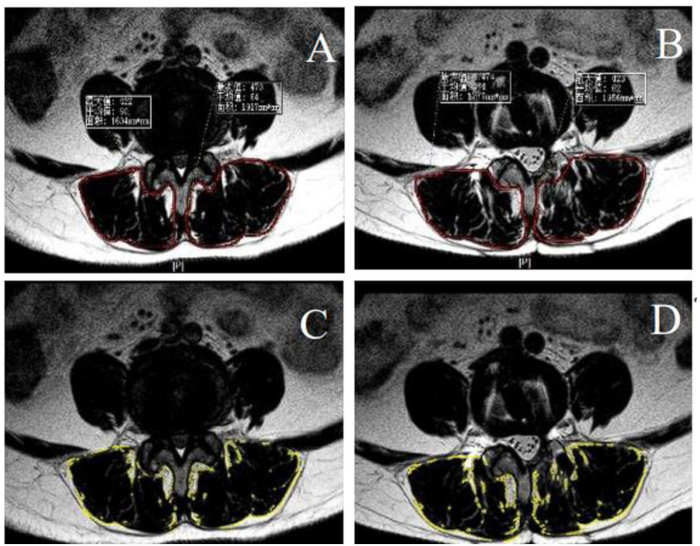
איור 3: חדירת שומן לפני ואחרי הניתוח ואזור חתך של שריר עמוד השדרה. (A-B) אזורי חתך לפני ואחרי הניתוח של שריר עמוד השדרה מוקפים בקו האדום. (ג-ד) חדירת שומן לפני ואחרי הניתוח של שריר עמוד השדרה, חישוב המאפיינים על ידי ImageJ, הוקפו על ידי הקו הצהוב. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
| מאפיינים | ערכים |
| גיל ממוצע (שנים) | 54.8 ± 17.5 |
| מין (M/F) | 47/49 |
| אבחון | |
| ספונדילוליסטזיס מותני | 21 |
| פריצת דיסק מותני עם חוסר יציבות סגמנטלית | 45 |
| היצרות הפתח המותני עם חוסר יציבות סגמנטלית | 30 |
| מדד BMI | 23.9 ± 2.8 |
| רמת פעולה | |
| רמה אחת | |
| L3-4 | 5 |
| L4-5 | 24 |
| L5-S1 | 21 |
| רב-מפלסי | |
| L3-5 | 18 |
| L4-S1 | 24 |
| L3-S1 | 4 |
| תקופת מעקב (חודשים) | 13.2 ± 2.1 |
טבלה 1: מאפיינים דמוגרפיים של חולים.
| מדדי | רמה אחת | רב-מפלסי |
| המטוקריט טרום ניתוחי (%) | 41.6 ± 4.8 | 42.7 ± 7.1 |
| המטוקריט לאחר הניתוח (%) | 38.5 ± 3.4 | 38.8 ± 6.8 |
| איבוד דם תוך ניתוחי (מ"ל) | 62.5 ± 28.2 | 108.3 ± 31.2 |
| אובדן דם כולל משוער (מ"ל) | 213.9 ± 124.8 | 282.8 ± 155.9 |
| זמן פעולה (דקות) | 102.3 ± 17.2 | 130.2 ± 18.3 |
| זמן אמבולציה לאחר הניתוח (ימים) | 1.7 ± 0.4 | 2.0 ± 0.5 |
טבלה 2: נתונים פריאופרטיביים.
| צד | CSA (מ"מ2) | FI (%) |
| לפני הניתוח | ||
| צד דקומפרסיה | 2088.4 ± 226.7 | 22.14 ± 9.21 |
| צד נגדי | 2081.8 ± 238.6 | 22.09 ± 9.04 |
| לאחר הניתוח | ||
| צד דקומפרסיה | 2077.9 ± 225.5 | 21.78 ± 8.71 |
| צד נגדי | 2076.1 ± 235.5 | 22.20 ± 9.19 |
טבלה 3: CSA של שריר עמוד השדרה לפני הניתוח ואחרי הניתוח וחדירת שומן.
| ממוצע ± SD (מ"מ2) | ערך p | |
| צד דקומפרסיה לפני הניתוח - צד נגדי טרום ניתוחי | 6.59 ± 36.65 | 0.081 |
| צד דקומפרסיה לפני הניתוח - צד דקומפרסיה לאחר הניתוח | 10.51 ± 59.68 | 0.088 |
| צד נגדי טרום ניתוחי - צד נגדי לאחר הניתוח | 5.77 ± 30.84 | 0.07 |
| צד נגדי לאחר הניתוח - צד דקומפרסיה לאחר הניתוח | 1.85 ± 80.48 | 0.822 |
טבלה 4: השוואה יעילה של שרירי עמוד השדרה. כל הניתוחים הסטטיסטיים בוצעו באמצעות מבחן t של מדגם זוגי.
Discussion
במהלך העשור האחרון, MIS-TLIF, PE-TLIF ו-BE-TLIF הפכו בהדרגה לחלופות לניתוח TLIF פתוח מסורתי, המציעים יתרונות במונחים של טראומה, אובדן דם והתאוששות לאחר הניתוח23. חלק מהחוקרים אפילו מאמינים שניתוח איחוי מותני בסיוע אנדוסקופי יחליף בסופו של דבר ניתוח פתוח. עם זאת, המחקר שלנו מראה שניתוח TLIF פתוח עשה התקדמות משמעותית גם במונחים של טכניקות זעיר פולשניות. תוך שמירה על הפשטות והישימות הרחבה של הליכים פתוחים מסורתיים, הוא השיג תוצאות קליניות והשפעות זעיר פולשניות הדומות לטכניקות זעיר פולשניות אנדוסקופיות.
לפני הניתוח, אנו מסמנים את הקרנת הפדיקל, נקודות הכניסה של מחט הניקוב, מקטעי המטרה הבין חולייתיים והחתך הכירורגי. עם זאת, אנו ממליצים לאמת את הקטע באמצעות פלואורוסקופיה שוב לפני הדקומפרסיה. הסיבה לכך היא שאפילו שינוי קל בזווית במהלך דיסקציה יכול להוביל לטעויות סגמנטליות, שכן נתקלנו בשני מקרים כאלה במהלך הניתוחים שלנו. לאחר דיסקציה, אזמל עצם אולטראסוני משמש באופן שגרתי לביצוע אוסטאוטומיה וחשיפת תעלת עמוד השדרה. כאשר עוסקים בתעלת עמוד השדרה, רצוי לשמור חלקית על הרצועה כדי להפחית את הידבקות הצלקת, ולהסיר רק את החלקים העבים מדי הדוחסים את העצבים. אם יש צורך בהפחתת לחץ של התעלה המרכזית הנגדית, ניתן לכוונן את זווית מיטת הניתוח כדי להסיר חלק מעצם השורש של התהליך הקוצני, ולהשיג דקומפרסיה בצד הנגדי. הפחתת לחץ לרוחב דו-צדדית עשויה לדרוש דיסקציה דו-צדדית. במהלך דקומפרסיה, מטעמי בטיחות, אין צורך לחשוף במלואו את השורש היוצא; ניתן להשתמש בוו כדי לחקור סביב שורש העצב, ואם יש מספיק מקום, אין צורך במניפולציה נרחבת. לאחר השלמת הדקומפרסיה והאיחוי, ניתן לסגור את החתך הקטן המרכזי, ולמקם ברגי פדיקל מלעוריים, מה שיכול לקצר את זמן הנסיגה על שרירי עמוד השדרה. מבחינת בחירת הכלובים, MO-TLIF יכול להשתמש בכלובי היתוך בגודל זהה ל-TLIF הפתוח המסורתי ללא צורך בכלובים קטנים יותר או ניתנים להרחבה, מה שעוזר להחזיר את גובה הדיסק ומפחית את הסיכון לשקיעת כלוב24. מטא-אנליזה הציעה כי הכלוב הישר תופס שטח גדול יותר של לוחית הקצה מאשר הכלוב בצורת בננה, ובכך יוצר פיזור טוב יותר של הלחץ, מה שעשוי לתרום לשיעור שקיעה נמוך יותר25. מחקר זה מצא רק מקרה אחד של שקיעת כלוב במהלך המעקב. MO-TLIF יכול גם להשיג דקומפרסיה מוגזמת לצד הנגדי, מה שהופך אותו למתאים ללמינטומיה חד צדדית לדקומפרסיה דו-צדדית (ULBD). זה מגדיל למעשה את שטח תעלת עמוד השדרה, אם כי יש צורך בניתוח סטטיסטי נוסף כדי למדוד שיפורים בגובה הבין חולייתי, בזוויות המותניים ובאזור תעלת עמוד השדרה.
בשל גודלו הקטן של החתך המרכזי, הוא אינו מתאים לניתוחי תיקון הדורשים החלפת קיבוע פנימי. עם זאת, גישה זו נותרה ישימה ברוב המקרים האחרים. לדוגמה, בניתוחים הכוללים ארבעה מקטעים, ניתן להשתמש בשני חתכים מרכזיים קטנים, כאשר כל חתך מטפל בשחרור לחץ של שני מקטעים.
ניתן לבצע את טכניקת MO-TLIF בהדמיה ישירה או בסיוע כלים חזותיים כגון זכוכית מגדלת או מיקרוסקופים. במחקר זה, המטופלים שעברו MO-TLIF רב-שכבתי הראו תוצאות טובות, עם זמן ניתוח ממוצע של 108.3 דקות ואיבוד דם ממוצע של 130.2 מ"ל. הדיסקציה התת-פריוסטאלית המוגבלת ונסיגת השרירים המינימלית עשויים להגן על שרירי עמוד השדרה, וכתוצאה מכך תוצאות קליניות דומות והשפעה על השרירים כמו ניתוח איחוי מותני בסיוע אנדוסקופי.
בעתיד הנראה לעין, טכניקות אנדוסקופיות או צינוריות עשויות שלא להחליף לחלוטין גישות כירורגיות פתוחות. MO-TLIF יכול לבצע ניתוח פתוח זעיר פולשני תוך שמירה על היתרונות הייחודיים של ניתוח פתוח, כגון הנוחות של ניתוחים רב-שכבתיים, זמן ניתוח קצר יותר, עקומת למידה חלקה, ללא צורך במכשירים מיוחדים ושימור משאבי מים. מחקר של Zhang et al. מצביע על כך שזמן הניתוח של PE-TLIF הוא 202 ±-31.4 דקות עם איבוד דם של 73 ±-26.4 מ"ל, שהוא פחות משמעותית מאובדן הדם תוך הניתוחי עבור MIS-TLIF (192 ± 18.9 דקות, 129 ± 31.7 מ"ל), אם כי זמן הניתוח ארוך יותר26. לעומת זאת, מחקר של Xue et al. מצא שזמן הניתוח ל-PE-TLIF (140.3 ±-35.6 דקות) קצר יותר מ-MIS-TLIF (170.6 ±-54.8 דקות), כאשר אובדן הדם תוך ניתוחי עבור PE-TLIF (65.6 ±-15.3 מ"ל) נמוך מ-MIS-TLIF (140.5 ±-21.5 מ"ל)27. ההבדלים בזמן הניתוח עשויים להיות קשורים למיומנות המנתח. מטא-אנליזות מראות כי זמן הניתוח הממוצע של PE-TLIF הוא 155 דקות עם איבוד דם ממוצע תוך ניתוחי של 101.1 מ"ל, בעוד של-MIS-TLIF יש זמן ניתוח ממוצע של 181.1 דקות ואיבוד דם תוך ניתוחי של 174 מ"ל28,29.
איבוד הדם תוך ניתוחי עבור MO-TLIF ברמה אחת (64.5 ± 30.2 מ"ל) דומה לזה של PE-TLIF וטוב יותר מ-MIS-TLIF, עם זמן פעולה קצר משמעותית (102.3 ±-17.2 דקות). MO-TLIF הוא יתרון לפעולות מרובות רמות, עם חתך חד-מפלסי של 3 ס"מ המורחב ב-1 ס"מ קרוב או דיסטלי לכל רמה נוספת. גישה זו מאפשרת פעולות דקומפרסיה עם הארכה מינימלית של החתך ועלייה קלה בלבד באיבוד הדם ובזמן הניתוח.
לסיכום, בעוד שלטכניקות אנדוסקופיות זעיר פולשניות יש יתרונות ברורים, ההתפתחות המתמשכת של הליכים פתוחים זעיר פולשניים כמו MO-TLIF ממשיכה להציע יתרונות ייחודיים, תוך שמירה על הרלוונטיות והיעילות שלהם בניתוחי עמוד השדרה.
Disclosures
למחברים אין ניגודי אינטרסים לחשוף.
Acknowledgements
מחקר זה נתמך על ידי קרן מהקרן הלאומית למדעי הטבע של סין בשנת 2021 (מספר פרויקט: 82474251) וקרן מפרויקט המדע והטכנולוגיה של ועדת הבריאות של סוג'ואו בשנת 2024 (מספר פרויקט: LCZX202307).
Materials
| Name | Company | Catalog Number | Comments |
| Absorbable sutures | Suzhou Jiahe | VT401L | |
| Blade | KYUAN | T00100 | |
| C-arm fluoroscopy | Siemens | Siremobile Compact L | |
| High frequency electrotome | Zhejiang Huatong | 20162010692 | |
| Iodophor | Likang High-tech | 31005102 | |
| Lumbar fusion cage | Shandong Weigao | GJXT310417 | |
| Premier posterior spine minimally invasive nail rod system | Shandong Weigao | GJXT310417 | |
| Suture | MERSILK | SA86G | |
| Ultrasonic bone knife | SMTP Technology | XD860A |
References
- Souslian, F. G., Patel, P. D. Review and analysis of modern lumbar spinal fusion techniques. Brit J Neurosurg. 38, 61-67 (2024).
- Mobbs, R. J., Phan, K., Malham, G., Seex, K., Rao, P. J. Lumbar interbody fusion: Techniques, indications and comparison of interbody fusion options including plif, tlif, mi-tlif, olif/atp, llif and alif. J Spine Surg. 1 (1), 2-18 (2015).
- Foley, K. T., Gupta, S. K., Justis, J. R., Sherman, M. C. Percutaneous pedicle screw fixation of the lumbar spine. Neurosurg Focus. 10 (4), E10(2001).
- Zhao, J., Zhang, F., Chen, X., Yao, Y. Posterior interbody fusion using a diagonal cage with unilateral transpedicular screw fixation for lumbar stenosis. J Clin Neurosci. 18 (3), 324-328 (2011).
- Foley, K. T., Lefkowitz, M. A. Advances in minimally invasive spine surgery. Clin Neurosurg. 49, 499-517 (2002).
- Kambin, P. Arthroscopic microdiscectomy. Arthroscopy. 8 (3), 287-295 (1992).
- Osman, S. G. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: A case series report. Int J Spine Surg. 6, 157-166 (2012).
- Kim, J. E., Choi, D. J. Biportal endoscopic transforaminal lumbar interbody fusion with arthroscopy. Clin Orthop Surg. 10 (2), 248-252 (2018).
- Derman, P. B., Albert, T. J. Interbody fusion techniques in the surgical management of degenerative lumbar spondylolisthesis. Curr Rev Musculoskelet Med. 10 (4), 530-538 (2017).
- Meng, F. J., et al. Comparison research of mMO-TLIF via midline approach versus MIS-TLIF via Wiltse approach for thoracolumbar surgery. Orthop J China. 28, 118-122 (2020).
- Li, S. W., et al. Comparison of mMO-TLIF via midline incision versus MIS-TLIF via Wiltse approach in lumbar degenerative disease. Indian J Orthop. 58, 1278-1287 (2024).
- Anand, N., Hamilton, J. F., Perri, B., Miraliakbar, H., Goldstein, T. Cantilever tlif with structural allograft and rhbmp2 for correction and maintenance of segmental sagittal lordosis: Long-term clinical, radiographic, and functional outcome. Spine. 31 (20), E748-E753 (2006).
- Shafaq, N., et al. Asymmetric degeneration of paravertebral muscles in patients with degenerative lumbar scoliosis. Spine. 37 (16), 1398-1406 (2012).
- Laasonen, E. M. Atrophy of sacrospinal muscle groups in patients with chronic, diffusely radiating lumbar back pain. Neuroradiology. 26 (1), 9-13 (1984).
- Hira, K., et al. Relationship of sagittal spinal alignment with low back pain and physical performance in the general population. Sci Rep. 11 (1), 20604(2021).
- Hiyama, A., et al. The correlation analysis between sagittal alignment and cross-sectional area of paraspinal muscle in patients with lumbar spinal stenosis and degenerative spondylolisthesis. BMC Musculoskelet Disord. 20 (1), 352(2019).
- Singh, K., et al. A perioperative cost analysis comparing single-level minimally invasive and open transforaminal lumbar interbody fusion. Spine J. 14 (8), 1694-1701 (2014).
- Phan, K., Rao, P. J., Kam, A. C., Mobbs, R. J. Minimally invasive versus open transforaminal lumbar interbody fusion for treatment of degenerative lumbar disease: systematic review and meta-analysis. Eur Spine J. 24 (5), 1017-1030 (2015).
- Nadler, S. B., Hidalgo, J. H., Bloch, T. Prediction of blood volume in normal human adults. Surgery. 51 (2), 224-232 (1962).
- Gross, J. B. Estimating allowable blood loss: corrected for dilution. Anesthesiology. 58 (3), 277-280 (1983).
- Bridwell, K. H., Lenke, L. G., Mcenery, K. W., Baldus, C., Blanke, K. Anterior fresh frozen structural allografts in the thoracic and lumbar spine. Spine. 20 (12), 1410-1418 (1995).
- Jacob, K. C., et al. The effect of the severity of preoperative disability on patient-reported outcomes and patient satisfaction following minimally invasive transforaminal lumbar interbody fusion. World Neurosurg. 159, E334-E346 (2022).
- Ba, Z., et al. Percutaneous endoscopical transforaminal approach versus plf to treat the single-level adjacent segment disease after plf/plif: 1-2 years follow-up. Int J Surg. 42, 22-26 (2017).
- Zhang, H., et al. Percutaneous endoscopic transforaminal lumbar interbody fusion: Technique note and comparison of early outcomes with minimally invasive transforaminal lumbar interbody fusion for lumbar spondylolisthesis. Int J Gen Med. 14, 549-558 (2021).
- Amer, S., Gaby, K., Jean, T., Khalil, K., Mohammad, D. Transforaminal lumbar interbody fusion using banana-shaped and cages: meta-analysis of and outcomes. Eur Spine J. 32, 3158-3166 (2023).
- Xue, Y. D., Diao, W. B., Ma, C., Li, J. Lumbar degenerative disease treated by percutaneous endoscopic transforaminal lumbar interbody fusion or minimally invasive surgery-transforaminal lumbar interbody fusion: A case-matched comparative study. J Orthop Surg Res. 16 (1), 696(2021).
- Zhu, L., et al. Comparison of clinical outcomes and complications between percutaneous endoscopic and minimally invasive transforaminal lumbar interbody fusion for degenerative lumbar disease: A systematic review and meta-analysis. Pain Physician. 24 (6), 441-452 (2021).
- Song, Y. F., et al. Percutaneous endoscopic versus minimally invasive transforaminal lumbar interbody fusion for lumbar degenerative diseases: A meta-analysis. Wideochir Inne Tech Maloinwazyjne. 17 (4), 591-600 (2022).
- Aoki, Y., et al. Influence of pelvic incidence-lumbar lordosis mismatch on surgical outcomes of short-segment transforaminal lumbar interbody fusion. BMC Musculoskelet Disord. 16, 213(2015).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved