Method Article
マイクロ超音波ガイド下経会陰前立腺生検:クリニックベースの手順
要約
この原稿では、局所麻酔下でマイクロ超音波ガイド下経会陰前立腺生検を実施するための手順を概説しています。
要約
前立腺がんは、男性に最も多くみられる固形悪性腫瘍であり、診断には生検が必要です。この原稿では、局所麻酔下で行われるフリーハンドのマイクロ超音波ガイド下経会陰技術について説明しており、精度を維持し、患者を快適に保ち、有害事象が少なく、使い捨ての必要性を最小限に抑えます。以前のマイクロ超音波ガイド下経会陰技術には、全身麻酔または脊椎麻酔が必要でした。プロトコルに記載されている主要なステップには、(1)局所麻酔の配置、(2)マイクロ超音波イメージング、(3)および超音波面から切り離された麻酔薬/生検針の視覚化が含まれます。この技術を受けた患者100人を対象としたレトロスペクティブ・レビューでは、臨床的に有意ながん検出率が68%であることが示された。疼痛スコアは、患者のサブセット(N = 20)で前向きに収集され、処置上の疼痛スコアの中央値は10人中2人であることが示されました。30日間のグレードIIIの有害事象発生率は3%でした。これらのイベントの1つは、おそらく前立腺生検に関連していました。全体として、マイクロ超音波ガイド下経会陰前立腺生検を実施するためのシンプルで正確かつ安全な技術を紹介します。
概要
前立腺がんは、アメリカ人男性の間で最も一般的な固形悪性腫瘍であり、2022 年には 268,000 件の診断が予測されています1。前立腺がんの診断には前立腺生検が必要ですが、これは従来、生検針を直腸粘膜(経直腸)に通して前立腺に通すことによって行われます。針のガイダンスは、従来の超音波ではがんと良性組織を区別することができないため、体系的な「ブラインド」テンプレートに従います2。米国では、このような生検が年間100万件以上行われています3,4。
過去10年間で、イメージングと技術における2つの大きな進歩により、安全性と精度が向上しました。第一に、直腸粘膜を避けるために経会陰生検の使用を増やすことで、抗生物質を必要とせずに敗血症のリスクが減少しました5,6。第二に、MRIおよびマイクロ超音波(Micro-US)の使用は、従来の(5MHz)超音波ガイダンス5,7,8,9を用いた生検と比較して癌検出率を改善した。
Micro-USは、29MHzの音波、改善された圧電結晶密度、および新しい波処理を利用して、従来の超音波の約200μmと比較して70μmの空間分解能を達成します8。5段階のリッカート尺度(Prostate Risk Identification Using Micro-Ultrasound, PRI-MUS)を用いた評価システムは、マイクロ超音波病変における前立腺がんのリスクを定量化するために使用されます10。生検コアと PRI-MUS 病変の位置は、Micro-US プローブ (ExactImaging、Markham、ON) のハンドルにある加速度計を使用して、正中線に対して追跡されます。生検を追跡する機能により、前立腺がんの位置を3Dで再構築することができます。局所治療や放射線ブーストなどの精密ながん治療は、追跡されたコアによって得られる空間情報によって可能になります。
今日まで、局所麻酔下でのマイクロ超音波ガイド下経会陰前立腺生検を可能にする公開された技術は、コアと病変の空間的配向も保持できません。この原稿は、そのような手法を描写することを目的としています。
プロトコル
説明されている方法は、フロリダ大学(UF)での経験に基づいています。プロトコールとデータの取得は、University Institutional Review Board(IRB)によって承認されました。前立腺生検の適応症には、疑わしい直腸指診(DRE)、前立腺特異抗原(PSA)の上昇、または別のバイオマーカー異常(4K、ExoDxなど)が含まれていました。このプロトコルは、右利きの外科医について説明されています。
1. マイクロ超音波プローブの準備
- マイクロ超音波の「システム操作および安全マニュアル」に従ってプローブを消毒します11。
- プローブカバーの端に約20 mLのアコースティックゲルを置き、気泡を取り除きます。プローブに針ガイドを置き、プローブカバーをプローブの上に置きます(図1A)。
注意: 気泡は、アワのおもちゃのように潤滑剤でプローブカバーを回転させることによって除去されます。遠心力により、潤滑油は遠位方向に変位し、気泡は近位に動きます。 - 圧電結晶の下のプローブネックに輪ゴムを巻き付けて、ゲルの漏れを防ぎます。
- 外科医の好みに応じて生検機器をセットアップします。
注:この調査で使用したセットアップを 図1Bに示します。
2. 患者のポジショニングと麻酔
- 患者を結石切開の位置に置き、肛門をベッドの端に置きます。快適さとプライバシーを向上させるために、頭のサポートと性器のドレープを提供します(図1C)。
注:UFでは、リソトミーポジショニング用のあぶみが好まれます。 - 前に説明した12のように、10mLの2%粘性リドカインゲルを直腸に入れます。
- この間、患者の快適さを確保し、必要な材料を準備してください。
- 肛門が外科医の肘の高さにくるようにベッドの高さを調整します。
- 陰嚢を持ち上げ、会陰を露出させるように患者に指示します(図1C)。
- アコースティックジェルを使用して、直腸指診を行います。病期分類および生検ターゲティングのための明白な異常に注意してください。
- 手袋を交換し、陰嚢の基部から肛門の下まで、会陰皮膚をベタジンまたはクロルヘキシジンで滅菌します。
- 肛門から約10〜15 mmから開始して、10時と2時の位置で会陰軟部組織に麻酔をかけます(図1D)。
注:1%リドカインと1:100,000エピネフリンおよび8.4%重炭酸ナトリウム溶液を1:10の比率で混合した1%リドカインを含む2インチ25G針から始めます(1 mLのNaHCO3:10 mLのリドカイン)。これを以下「リドカイン」といいます。 - 針を直腸と平行に挿入し、針が進むにつれてリドカインを注入します。皮膚とコレス筋膜の間の軟部組織に約3 mL、コレス筋膜の間に約2 mLのリドカインを入れます(図2A)。
注:効率を上げるために、上記の手順はブラインド方式で実行されます。ただし、経験の早い段階では、患者の解剖学的構造が骨盤の形状、臀筋組織、および肥満によって異なるため、超音波ガイダンスの利用を検討してください。
3.マイクロ超音波診断
- プローブに注油し、直腸にそっと挿入し、前立腺中部がビューイングモニターの中心に来るまで進めます。
注:プローブの先端を肛門括約筋を越えて下(仙骨に向かって)向けることにより、S状結腸の輪郭をたどります。この技術を使用すると、膀胱基部を最小限の不快感で視覚化できます。プローブを下向きにしないと、痛みを引き起こします。 - マイクロ超音波画像設定を最適化します。
- イメージングプローブを左手(利き手ではない)で、プローブの最も厚い部分でつかみます。プローブをピッチして上向きに持ち上げ、前立腺の基部が圧電結晶から最大の圧力を受けるようにします。ピッチングとリフティングの動きにより、直腸が圧迫され、視覚化が最適化されます(図1C)。
- 時間補正ゲイン(TCG)スライダーを緩やかな逆の「C」または「J」の形に調整し、画像全体に均一なグレースケールができるまで調整します。
- 前立腺の横方向のエッジがよく視覚化され、前立腺の中心が明るすぎないように、マスターゲインダイヤルを調整します。
注:外側前立腺は、反射された超音波が斜めに戻ることが少ないため、中央腺よりも音響的に暗くなります。 - 泡や直腸粘液が影の原因になっていないことを確認してください。
注意: UFでは、ダイナミックレンジ、深度、およびフォーカスにデフォルト設定が使用されます。ただし、これらは外科医の好みに応じて調整することができます。 - 画像プリセット(小、中、大、 特大)を選択して、前立腺の前立腺脂肪を最小限に抑えた前立腺の視覚化を可能にします。
注:画像の最適化とMicro-USの操作の詳細については、Micro-USの「システム操作および安全マニュアル」11を参照してください。
- Dual/Transverseボタンを押して前立腺の体積計算を行い、前立腺のスイープを行い、矢状長と再構築された軸の高さと幅を測定します。
- 尿道が可視化されるまでプローブを回転させます。尿道の視覚化は、膀胱、頸部、および前立腺の頂点で最適です。プローブを正中線と平行に配置して、膀胱頸部と尿道が同じ平面に見えるようにします(ヨーニュートラル)。
- Micro-USタッチスクリーンの 角度リセット を押して、プローブ加速度計をゼロにします。
- プローブが電気コードと出会うプローブの近位部分に右手を置きます。左手はプローブネックの下に滑り込み、上向きのピッチ位置を支えます(図1C)。
- 患者にじっとしているように伝えます。1 回の動きで、前立腺の右側境界 (時計回り) から前立腺を通って左端までスイープし、~25 秒かかります。 Cine Loop ボタンを押して、スイープを記録します。
注:50mLを超える前立腺には、多くの場合、頂点と基部の別々のスイープが必要です。遷移ゾーンを視覚化するスイープと、周辺ゾーンを視覚化するスイープを Small 設定で記録するのがベスト プラクティスです。
4. 診断評価
- PRI-MUS 病変の移行ゾーンを評価します。
- 遷移ゾーンが評価されたら、 Small image 設定に切り替えて、PRI-MUS 病変の末梢ゾーンを評価します。
注:無料のMicro-US診断ライブラリを使用して練習することを検討してください PRI-MUS病変の特定と等級付けの経験を積むために11。 - 中心角度と ROI が最初と最後に見える角度を記録することで、検出された関心領域 (ROI) の位置に注意してください。
注:UFでは、これらの角度は外科医によって呼び出され、生検スイートのスタッフによって手術ノートに記録されます。 - 融合ソフトウェアを使用する場合は、生検前に注釈が付けられたMRIをロードし、尿道を視覚化しながら Mid-line ボタンを押します(図2B)。
5.前立腺麻酔
- 6インチの20G針を使用して、以前に麻酔した生検管で皮膚を穿刺し、Micro-US視覚化の下で針を挙筋肛門に進めます(図2A)。
- 3 mLの局所麻酔薬を肛門挙筋複合体に入れます(図2A)。
- 20 Gの針を頂端周囲三角形(内側は尿道、外側は肛門挙筋、後方はデノンビリアーズ筋膜に囲まれています)に進めます。5〜7 mLのリドカインを頂端周囲三角形に注入します(図2A)。
注:背側静脈複合体(DVC)の外側の側面は、根尖周囲三角形に垂れ下がっています。したがって、リドカイン注射の前に吸引します。適切な麻酔により、前立腺嚢とDenonvilliers筋膜の間を水素化解剖します。
6.前立腺生検
- 14 G 血管カテーテルまたは 15 G の金属同軸針 (アクセス針) を、以前に麻酔した管から前立腺の頂点の 5 〜 10 mm 以内に挿入します。アクセス針を肛門括約筋の上に通し、肛門挙筋を通すか内側に通します。アクセス針と直腸の間の距離をROIの位置に応じてカスタマイズします。
- 直腸から5 mm上、尿道が見える前立腺中央面から15°〜20°の針の位置を使用して、前立腺全体をサンプリングします(図1D、10時および2時の位置)。
- インソネーション面がアクセスニードルを視覚化するようにプローブを回転させ、アクセスニードルの端に生検針の先端が見えるまで生検ガンを進めます。
- プローブを回転させて生検ターゲット(ROIまたは系統的コア)を視覚化し、次に回転させて生検針先を視覚化します。患者の外部にある生検ガンを調整することにより、ターゲットに向かう針の軌道を調整します。
- 目視下で針を前進させ、針の先端を目的のターゲットに導くために小さな3°〜10°のプローブロール(マイクロロール)を完成させます。生検針は先端を視覚化しながらのみ進め、目的のターゲットをオーバーシュートしないようにします。
注:ターゲットに向かって大きな動きをする場合は、生検針を抜く必要があります。この技術では、プローブは針と平行ではなく、尿道と平行に保たれます(「ヨーイング」)。尿道に対する生検角度を維持することで、がんの位置を正確に再構築し、患者の快適性を最大限に高めることができます。この手法の最も難しい部分は、共鳴面から切り離されたときの針の視覚化です。研修医、フェロー、その他の医師を指導した私たちの経験では、この技術を実装するために必要な筋肉の記憶には、約3時間の練習が必要です。生検の前に必要な筋肉の記憶を構築するために、前立腺ファントムまたはシミュレーター13 で練習することを検討してください。最初に麻酔をかけられた患者にこの技術を実行すると、クリニックベースの診療への移行が容易になります。 - 生検サンプルを採取する前に、それを尿道に転がし、角度が0°の位置から1°〜2°以内にあることを確認してください。フレームまたはシネループをキャプチャして、各生検スローの角度位置を記録します。
注:慣例により、右側(反時計回り)の回転は正の角度で示され、左側(時計回り)の回転は負の角度で示されます。 - ROIを通じて分布する3つの生検コアを取得することから始めます(図2C)。
- 経会陰系統的生検の実施を検討してください(図3)。効率を上げるために、ROIと同側の系統的な生検を開始します。ROIが前方にある場合は、同軸針を下げて、末梢ゾーンの系統的な生検サンプリングを改善します。
注:この研究では、14コアの系統的生検を実施しました(図3)。系統的生検は、次の場合にスキップされる可能性があります: 1) 以前にサンプリングされた ROI と重なる系統的コア、および 2) 1 回のスローで頂点と基部をサンプリングする小さな前立腺。このテンプレートを利用して、頂端生検は、頂端前立腺嚢での投球を開始することによって得られます。塩基生検は、中腺で投球を開始することによって得られます。
7. 手続き終了
- すべての生検を取得したら、同軸針と超音波プローブを取り外します。
- 穿刺部位の止血が達成されるまで、タオルで会陰に圧力をかけ続けます。
- 患者を座位に座らせ、1分後には立位にします。
- 一過性血尿と血精子症を予想するように患者に助言します。.
- ベースラインが制限された尿流の患者に、必要に応じて充填するように処方します。
結果
2021年9月から2022年6月(IRB202200022)にかけての将来的に維持されたデータベースの遡及的分析について説明します。臨床的に重要な前立腺がん(csPCa)は、≥グレードグループ2(グリソン3 + 4 = 7)の前立腺がんと見なされました。がん検出率(CDR)は、≥GG2/総患者数として計算されました。疼痛スコアは、ベースライン時、局所麻酔留置時、直腸プローブ挿入時、および生検中に 1 〜 10 ポイントのリッカート スケールで評価されました。有害事象は、処置後 2 週間で患者と話し合い、カルテレビューで捕捉された事象は、生検から 30 日以内に記録されました。有害事象は、CTEP(Cancer Therapy Evaluation Program)グレードとアトリビューションガイドを使用して評価されました。
局所麻酔下でMicro-USガイド下、クリニックベースの経会陰生検を受けた100人の患者を特定しました。この研究では、患者一人当たりのCDRは68%であった。CDRは、各病変のPI-RAD(Prostate Image Reporting and Data System)およびPRI-MUSスコアによって異なりました(表1)。
疼痛スコアは、後の患者のサブセット(N = 20)で利用可能でした。疼痛スコアの中央値(IQR)は、ベースラインで0(0,1)、局所麻酔投与で2(1,4)、経直腸プローブ留置で2(1,5)、前立腺生検で2(0,5)でした。
有害事象は比較的まれで、グレードIIIの有害事象の発生率は3%でした(表2)。グレードIVやグレードVのイベントはありませんでした。グレードIIのイベントは、主に尿の流れの鈍化を緩和するためのアルファ遮断薬の新しい処方を含んでいました。上記のように、患者は生検の前に症状についてスクリーニングされました。グレードIIIのイベントでは、3人の患者が入院しました。CTEP アトリビューション ガイドによると、症候性低血圧による 1 回の入院は、おそらくリドカイン吸収に続発する前立腺生検に関連していました。患者は、モニタリングから12時間以内に症状が自然に解消しました。さらに2人の患者が生検から30日以内に入院しました(機械的転倒と精神状態の変化)。彼らは偶然にも、おそらく生検に関連している非敗血症性および非症候性のUTIを持っていることがわかりました。言及されたこれらの特定の患者を除いて、敗血症、前立腺炎、膀胱炎、またはその他の感染症の症例はありませんでした。
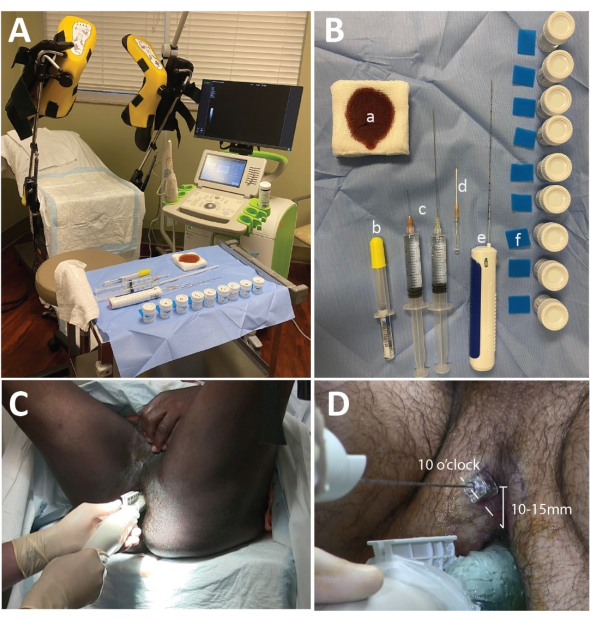
図1:マイクロ超音波セットアップ、生検トレイ、および針の配置 (A)ExactVuマシンを外科医の右側に置いた処置室のセットアップ。(B)(a)ベタジンを浸した4 cm x 4 cmのガーゼパッド、(b)10 mLの2%リドカインゲル、(c)1%リドカインと1:100,000エピネフリンを含む1%リドカインと2 mLの8.4%重炭酸ナトリウム溶液(1 mLのNaHCO3:10 mLのリドカイン)を2×20 mLシリンジに分配し、2インチの25 G針と6インチの20 G針、 (d)14G血管性または同軸金属針、(e)生検ガン、(f)フォーム生検パッド、およびホルマリン容器。(C)診断スイープを実行するための手の位置。左手で前立腺への上向きの圧力を支え、右手でプローブを回転させることに注意してください。(D)同軸針または血管カテーテルの位置:右側の前立腺は10時、左側の前立腺は2時(図示せず)。 この図の拡大版を表示するには、ここをクリックしてください。
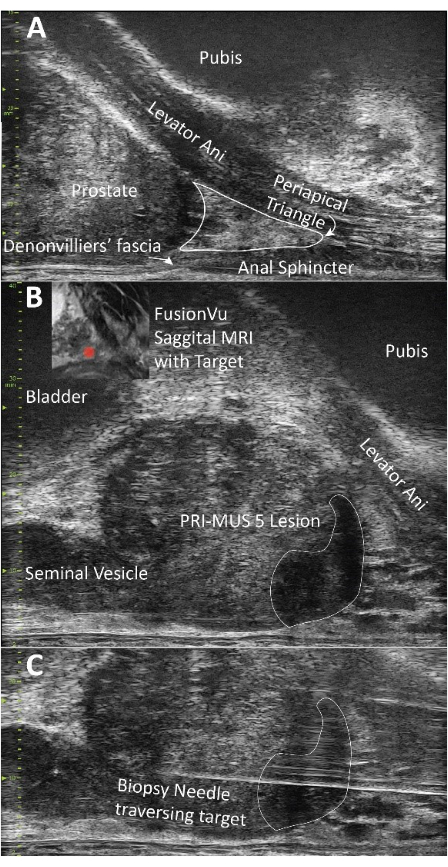
図2:前立腺の解剖学と生検のデモンストレーション (A)挙筋肛門と根尖周囲三角形の視覚化。どちらも、この技術を成功裏に実施するために麻酔をかけるための重要な構造です。(B) PRI-MUS 5 病変のデモンストレーション、解剖学的に生検前 MRI と一致します。(C)ターゲットを横切る生検針の視覚的確認。 この図の拡大版を表示するには、ここをクリックしてください。

図3:提案された技術の体系的な生検テンプレート。 このテンプレートは、Michigan Urologic Surgery Improvement Collaborative(MUSIC)14で利用可能なテンプレートに基づいています。ただし、このテンプレートは 3 つの点で改善されています。(i)前部ゾーンのサンプリングの増加(4コア対2コア)、(ii)3Dモデルを使用したコア位置の視覚的表示の大幅な改善、および(iii)使いやすさを向上させるためにコアの命名法を変更しました。このプロトコルでは、イメージング陰性 (PRI-MUS ≤ 2) 組織内の ROI 生検の後に、体系的な生検が行われます。 この図の拡大版を表示するには、ここをクリックしてください。
| PI-RADS 5 | PIカード4 | PI-RADS 3 | |
| PRIムス5 | 95% (n = 20) | 80% (n = 15) | 100% (n = 1) |
| PRIムース4 | 100% (n = 1) | 69% (n = 13) | 75% (n = 4) |
| PRIムース3 | 0% (n = 0) | 33% (n = 3) | NAの |
表1:PI-RADおよびPRI-MUSスコアによって層別化された臨床的に重要な前立腺がんの検出。 生検時にMRIとマイクロ超音波の両方が利用可能な患者における臨床的に有意な前立腺がん検出率(CDR)。CDR は、PI-RADS (列) と PRI-MUS スコア (行) によって層化されます。これらの基準を満たす患者の数は括弧内に記録されています。
| クラビアン・ディンド・グレード | 発生 |
| グレードI | 4% (n = 4) |
| グレードII | 5% (n = 5) |
| グレードIII | 3% (n = 3) |
| グレードIV | 0% (n = 0) |
| グレードV | 0% (n = 0) |
表2:グレード別の有害事象を経験した患者の割合。 前立腺生検から30日以内に有害事象が認められた患者の割合。グレードIIIの有害事象は非敗血症性事象による入院であり、そのうちの1つはおそらく生検に関連しており、そのうちの2つは生検に関連している可能性があることに注意してください。
ディスカッション
この原稿では、局所麻酔下での Micro-US ガイド下、フリーハンド、経会陰前立腺生検の手順と結果を詳しく説明しています。これは、生検のコア位置と患者の快適さを維持する技術の最初の説明です。私たちの経験では、この手順は正確で、忍容性が高く、有害事象は最小限に抑えられています。
特に、予防的抗生物質が不足しているにもかかわらず、敗血症や前立腺炎の症例は報告されていませんでした。ここで使用したサンプルの結果は、経会陰生検6で予防的抗菌薬の利点が認められなかったNORAPP試験の所見と合併症発生率を裏付けています。
手順の重要な手順は次のとおりです。ステップ2.6とセクション5で述べた消毒と麻酔は、患者の快適性を維持しながら直腸壁ではなく会陰部を横断することにより感染率を減らすための重要な要素です。セクション 4 では、生検ターゲットの ROI を詳しく説明し、前立腺の問題のある領域を効果的にサンプリングしながら、より少ないコアを採取できるようにします。
経会陰生検は、敗血症の発生率がゼロであること15,16、前部腫瘍のサンプリングの精度、抗生物質の使用、およびガイドラインの推奨事項17,18 を考えると、他の方法と比較して人気が高まっています。同時に、Micro-USは、正確ながんイメージングモダリティ、シンプルな融合プラットフォーム、および独立したイメージングバイオマーカーとして認識されています9,19。以前の Micro-US ガイド下経会陰技術は、42% の優れた CDR を報告しました。ただし、この手法では、針ガイドを使用して針と共鳴面を位置合わせしていました。ガイドを使用すると学習曲線が改善される一方で、各生検穿刺が新しい部位20を通過するため、全身麻酔の使用を可能にするために生検を手術室に限定する可能性が高い。CDRは68%と報告されており、このフリーハンド技術の精度はニードルガイドの使用に匹敵することを示しています。
私たちの技術の精度、忍容性、および最小限の有害事象は、特定の制限内で解釈する必要があります。生検針の位置を特定して指示するには、シミュレーターまたはファントムで約 3 時間の実践的な練習が必要です。Micro-US画像の解釈を学習するには、さらに時間がかかる場合があります。標的生検と系統的生検を行うと、17個以上の生検コアが得られ、最大30分の処置時間が必要になることがあります。優れたがん検出率を報告していますが、この技術の成功は、csPCa21 の <15% と計算されたリスクを持つ患者の前立腺生検を省略する私たちの実践に部分的に関連しています。最後に、この研究で使用された系統的生検テンプレートは、前立腺の最もリスクの高い領域をサンプリングしますが、他の経会陰生検テンプレートと比較されたことはありません。これらの制限にもかかわらず、この手法にはいくつかの利点があり、最も顕著なのは、クリニックベースの環境で手順を実行できることです。さらに、micro-USプローブの位置追跡により、外科的摘出術、放射線増強、または局所療法を行う際に使用するために、がんの位置を3Dで再構築することができます。
結論として、Micro-US は前立腺生検の最近の改善を表しています。私たちは、局所麻酔下でクリニックで実施できる経会陰アプローチを示しています。Micro-USの診断能力のさらなる評価と改善が必要ですが、この技術を採用する外科医は、実装が簡単で、正確で、安全であることに気付くでしょう。
開示事項
何一つ。
謝辞
何一つ。
資料
| Name | Company | Catalog Number | Comments |
| 14 ga Angiocatheter | BD Angiocath | BD382269 | |
| Aquasonic | Parker Labs | Aquasonic 100 | |
| Biopsy Needle | Bard | MaxCore | |
| Biopsy Sponge 2 mm x 25.4 mm x 30.2 mm | McKesson | 1019107 | |
| ExactVu Micro-Ultrasound Machine | ExactImaging | ||
| ExactVu Micro-Ultrasound Probe (EV29L) | ExactImaging | ||
| Guaze Sponge McKesson Cotton 12-Ply 4'' x 4'' | McKesson | 762703 | |
| Hypodermic Needle 25 G 1.5 inch | McKesson | 42142523 | |
| Lidocaine 1% with Epinephrine 1:100,000 | NA | ||
| Lidocaine 2% Gel, 20 mL | URO-Jet | 76329301505 | |
| Probe Cover | ExactImaging | ||
| Skin Prep Solution betadine (10%) | McKesson | 1073829 | |
| Spinal Needle 20 G, 6 inch | McKesson | 992546 | |
| TruGuide | Bard | C1616A |
参考文献
- Siegel, R. L., Miller, K. D., Fuchs, H. E., Jemal, A. Cancer statistics, 2022. CA: A Cancer Journal for Clinicians. 72 (1), 7-33 (2022).
- Onur, R., Littrup, P. J., Pontes, J. E., Bianco, F. J. Contemporary impact of transrectal ultrasound lesions for prostate cancer detection. The Journal of Urology. 172 (2), 512-514 (2004).
- Loeb, S., Carter, H. B., Berndt, S. I., Ricker, W., Schaeffer, E. M. Complications after prostate biopsy: Data from SEER-Medicare. The Journal of Urology. 186 (5), 1830-1834 (2011).
- Borghesi, M., et al. Complications after systematic, random, and image-guided prostate biopsy. European Urology. 71 (3), 353-365 (2017).
- Pradere, B., et al. Nonantibiotic strategies for the prevention of infectious complications following prostate biopsy: A systematic review and meta-analysis. The Journal of Urology. 205 (3), 653-663 (2021).
- Jacewicz, M., et al. Antibiotic prophylaxis versus no antibiotic prophylaxis in transperineal prostate biopsies (NORAPP): A randomised, open-label, non-inferiority trial. The Lancet. Infectious Diseases. 22 (10), 1465-1471 (2022).
- Ahmed, H. U., et al. Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer (PROMIS): A paired validating confirmatory study. The Lancet. 389 (10071), 815-822 (2017).
- Kasivisvanathan, V., et al. MRI-targeted or standard biopsy for prostate-cancer diagnosis. The New England Journal of Medicine. 378 (19), 1767 (2018).
- Sountoulides, P., et al. Micro-ultrasound-guided vs multiparametric magnetic resonance imaging-targeted biopsy in the detection of prostate cancer: A systematic review and meta-analysis. The Journal of Urology. 205 (5), 1254-1262 (2021).
- Ghai, S., et al. Assessing cancer risk on novel 29 MHz micro-ultrasound images of the prostate: Creation of the micro-ultrasound protocol for prostate risk identification. The Journal of Urology. 196 (2), 562-569 (2016).
- Exact Imaging E-learning. Exact Imaging Available from: https://elearn.exactimaging.com/learn (2022)
- Siddiqui, E. J., Ali, S., Koneru, S. The rectal administration of lignocaine gel and periprostatic lignocaine infiltration during transrectal ultrasound-guided prostate biopsy provides effective analgesia. Annals of the Royal College of Surgeons of England. 88 (2), 218-221 (2006).
- Zhang, Z., et al. Attitude is everything: Keep probe pitch neutral during side-fire prostate biopsy. A simulator study. BJU International. 128 (5), 615-624 (2021).
- Prostate Biopsy. Michigan Urological Surgery Improvement Collaborative (MUSIC) Available from: https://musicurology.com/programs/prostate/transperinealbiopsy/ (2022)
- Sigle, A., et al. Safety and side effects of transperineal prostate biopsy without antibiotic prophylaxis. Urologic Oncology: Seminars and Original Investigations. 39 (11), (2021).
- Grummet, J. P., et al. Sepsis and "superbugs": Should we favour the transperineal over the transrectal approach for prostate biopsy. BJU International. 114 (3), 384-388 (2014).
- Pilatz, A., et al. European association of urology position paper on the prevention of infectious complications following prostate biopsy. European Urology. 79 (1), 11-15 (2021).
- Meyer, A. R., et al. Transperineal prostate biopsy improves the detection of clinically significant prostate cancer among men on active surveillance. The Journal of Urology. 205 (4), 1069-1074 (2021).
- Avolio, P. P., et al. The use of 29 MHz transrectal micro-ultrasound to stratify the prostate cancer risk in patients with PI-RADS III lesions at multiparametric MRI: A single institutional analysis. Urologic Oncology: Seminars and Original Investigations. 39 (12), 1-7 (2021).
- Rodríguez Socarrás, M. E., et al. Prostate mapping for cancer diagnosis: The Madrid protocol. Transperineal prostate biopsies using multiparametric magnetic resonance imaging fusion and micro-ultrasound guided biopsies. The Journal of Urology. 204 (4), 726-733 (2020).
- Kinnaird, A., et al. A prostate cancer risk calculator: Use of clinical and magnetic resonance imaging data to predict biopsy outcome in North American men. Canadian Urological Association Journal. 16 (3), 161-166 (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved