Method Article
Biopsia de próstata transperineal guiada por microecografía: un procedimiento clínico
En este artículo
Resumen
Este manuscrito describe los pasos para realizar una biopsia de próstata transperineal guiada por microultrasonido bajo anestesia local.
Resumen
El cáncer de próstata es la neoplasia maligna sólida más común en los hombres y requiere una biopsia para su diagnóstico. Este manuscrito describe una técnica transperineal guiada por microultrasonido a mano alzada realizada bajo anestesia local, que mantiene la precisión, mantiene a los pacientes cómodos, tiene pocos eventos adversos y minimiza la necesidad de desechables. Las técnicas transperineales previas guiadas por microecografía requerían anestesia general o raquídea. Los pasos clave descritos en el protocolo incluyen (1) la colocación de la anestesia local, (2) la toma de imágenes de microultrasonido, (3) y la visualización de la aguja anestésica/de biopsia mientras está desacoplada del plano de insonación. En una revisión retrospectiva de 100 pacientes sometidos a esta técnica, se demostró una tasa de detección de cáncer clínicamente significativa del 68 %. Las puntuaciones de dolor se recogieron prospectivamente en un subconjunto de pacientes (N = 20) y mostraron una mediana de puntuación de dolor durante el procedimiento de 2 sobre 10. La tasa de eventos adversos de grado III a 30 días fue del 3%; Probablemente uno de estos eventos estuvo relacionado con la biopsia de próstata. En general, presentamos una técnica sencilla, precisa y segura para realizar una biopsia de próstata transperineal guiada por microecografía.
Introducción
El cáncer de próstata es la neoplasia maligna sólida más común entre los hombres estadounidenses, con 268,000 diagnósticos proyectados en 20221. El diagnóstico del cáncer de próstata requiere una biopsia de próstata, que tradicionalmente se realiza pasando una aguja de biopsia a través de la mucosa rectal (transrectal) hasta la próstata. La guía de la aguja sigue un modelo sistemático "ciego", ya que la ecografía convencional no puede diferenciar el cáncer del tejido benigno2. En los Estados Unidos, se realizan anualmente más de 1 millón de biopsias de este tipo 3,4.
En la última década, dos avances significativos en imágenes y técnicas han mejorado la seguridad y la precisión. En primer lugar, el aumento del uso de biopsias transperineales para evitar la mucosa rectal ha disminuido el riesgo de sepsis sin necesidad de antibióticos 5,6. En segundo lugar, el uso de la resonancia magnética y la microecografía (Micro-US) han mejorado las tasas de detección del cáncer en comparación con la biopsia con guía ecográfica convencional (5 MHz) 5,7,8,9.
Micro-US utiliza ondas acústicas de 29 MHz, una densidad de cristal piezoeléctrico mejorada y un procesamiento de ondas novedoso para lograr una resolución espacial de 70 μm en comparación con los 200 μm de un ultrasonido convencional8. Se utiliza un sistema de clasificación mediante una escala Likert de 5 puntos (Prostate Risk Identification Using Micro-Ultrasound, PRI-MUS), para cuantificar el riesgo de cáncer de próstata en lesiones microecográficas10. El núcleo de la biopsia y las ubicaciones de las lesiones PRI-MUS se rastrean en relación con la línea media utilizando un acelerómetro ubicado en el mango de la sonda Micro-US (ExactImaging, Markham, ON). La capacidad de rastrear biopsias permite la reconstrucción en 3D de las ubicaciones del cáncer de próstata. Los tratamientos de precisión contra el cáncer, como la terapia focal y el refuerzo de radiación, se permiten a través de la información espacial obtenida por los núcleos rastreados.
Hasta la fecha, ninguna técnica publicada que permita la biopsia de próstata transperineal guiada por microecografía bajo anestesia local puede retener también la orientación espacial de los cilindros y las lesiones. Este manuscrito tiene como objetivo delinear dicha técnica.
Protocolo
Los métodos descritos se basan en la experiencia de la Universidad de Florida (UF). El protocolo y la adquisición de datos fueron aprobados por el University Institutional Review Board (IRB). Las indicaciones para la biopsia de próstata incluyeron un tacto rectal (DRE) sospechoso, elevación del antígeno prostático específico (PSA) u otra anomalía de biomarcadores (es decir, 4K, ExoDx). Se describe el protocolo para un cirujano diestro.
1. Preparación de la sonda de microultrasonido
- Desinfecte la sonda según el "Manual de funcionamiento y seguridad del sistema" de microultrasonidos11.
- Coloque alrededor de 20 ml de gel acústico en el extremo de la tapa de la sonda y elimine las burbujas. Coloque una guía de aguja en la sonda y coloque la cubierta de la sonda sobre la sonda (Figura 1A).
NOTA: Las burbujas se eliminan girando la tapa de la sonda con lubricante como con un juguete de cola de zorro. La fuerza centrífuga desplaza la lubricación distalmente mientras que mueve las burbujas proximalmente. - Coloque una banda elástica alrededor del cuello de la sonda debajo de los cristales piezoeléctricos para evitar fugas de gel.
- Configure el equipo de biopsia según las preferencias del cirujano.
NOTA: La configuración utilizada en este estudio se muestra en la Figura 1B.
2. Posicionamiento del paciente y anestesia
- Coloque al paciente en la posición de litotomía con el ano en el borde de la cama. Proporcione soporte para la cabeza y un paño genital para mejorar la comodidad y la privacidad (Figura 1C).
NOTA: En UF, se prefieren los estribos para el posicionamiento de la litotomía. - Coloque 10 mL de gel de lidocaína viscosa al 2% en el recto como se describió anteriormente12.
- Asegurar la comodidad del paciente y la preparación de los materiales necesarios durante este tiempo.
- Ajuste la altura de la cama para que el ano quede a la altura del codo del cirujano.
- Indique al paciente que eleve el escroto y exponga el perineo (Figura 1C).
- Con gel acústico, realice un tacto rectal. Observe anomalías palpables para la estadificación y la focalización de la biopsia.
- Cámbiese los guantes y esterilice la piel perineal con betadine o clorhexidina desde la base del escroto hasta debajo del ano.
- Anestesiar el tejido blando perineal en las posiciones de las 10 y las 2 en punto, comenzando alrededor de 10-15 mm del ano (Figura 1D).
NOTA: Comience con una aguja de 2 pulgadas y 25 g que contenga lidocaína al 1% con una solución de epinefrina 1:100.000 y bicarbonato de sodio al 8,4% mezclada en una proporción de 1:10 (1 mL de NaHCO3: 10 mL de lidocaína). En lo sucesivo, se hace referencia a ella como "lidocaína". - Inserte la aguja paralela al recto e inyecte lidocaína a medida que avanza la aguja. Coloque alrededor de 3 mL de lidocaína en el tejido blando entre la piel y la fascia de Colles y 2 mL entre la fascia de Colles (Figura 2A).
NOTA: Para mayor eficiencia, el paso anterior se realiza a ciegas; Sin embargo, al principio de la experiencia, considere utilizar la guía de ultrasonido, ya que la anatomía del paciente difiere con la forma pélvica, la musculatura glútea y la obesidad.
3. Diagnóstico microecográfico
- Lubrique la sonda, insértela suavemente en el recto y avance hasta que la próstata media esté centrada en el monitor de visualización.
NOTA: Siga el contorno del sigmoide dirigiendo la punta de la sonda hacia abajo (hacia el sacro) una vez más allá del esfínter anal. Con esta técnica, se puede visualizar la base de la vejiga con una molestia mínima. Si no se dirige la sonda hacia abajo, se producirá dolor. - Optimice la configuración de imágenes de microultrasonido.
- Sujete la sonda de imagen con la mano izquierda (no dominante) en la parte más gruesa de la sonda. Incline y levante la sonda hacia arriba para que la base de la próstata reciba la mayor presión de los cristales piezoeléctricos. El movimiento de cabeceo y elevación comprimirá el recto y optimizará la visualización (Figura 1C).
- Ajuste los controles deslizantes de ganancia compensada en el tiempo (TCG) en una forma de "C" o "J" inversa suave hasta que haya una escala de grises uniforme en toda la imagen.
- Ajuste el dial de ganancia principal para que los bordes laterales de la próstata se visualicen bien, pero el centro de la próstata no sea demasiado brillante.
NOTA: La próstata lateral es acústicamente más oscura que la glándula media, ya que menos ondas de ultrasonido reflejadas regresan en ángulo. - Asegúrese de que no haya burbujas o moco rectal que causen sombras.
NOTA: En UF, los ajustes predeterminados se utilizan para el rango dinámico, la profundidad y el enfoque; sin embargo, estos se pueden ajustar según las preferencias del cirujano. - Seleccione un ajuste preestablecido de imagen (pequeño, mediano, grande y extragrande) que permita la visualización de la próstata con un mínimo de grasa prostática anterior.
NOTA: Los detalles de la optimización de la imagen y el funcionamiento de Micro-US están disponibles en el "Manual de funcionamiento y seguridad del sistema" de Micro-US11.
- Realice un cálculo del volumen prostático pulsando el botón Dual/Transversal , realizando un barrido de la próstata y, a continuación, midiendo la longitud sagital y la altura y anchura axiales reconstruidas.
- Gire la sonda hasta que se visualice la uretra. La visualización de la uretra es mejor en el ápice de la vejiga, el cuello y la próstata. Coloque la sonda paralela a la línea media para que el cuello de la vejiga y la uretra sean visibles en el mismo plano (guiñada neutra).
- Presione el restablecimiento de ángulo en la pantalla táctil Micro-US para poner a cero el acelerómetro de la sonda.
- Coloque la mano derecha en la parte proximal de la sonda donde la sonda se encuentra con el cable eléctrico. La mano izquierda se desliza por debajo del cuello de la sonda, apoyando la posición de paso hacia arriba (Figura 1C).
- Dígale al paciente que se quede quieto; En un solo movimiento, barre desde el borde lateral derecho de la próstata (en el sentido de las agujas del reloj) a través de la próstata hasta el borde izquierdo, tomando ~ 25 s. Presione el botón Cine Loop para grabar el barrido.
NOTA: A menudo se requieren barridos separados del ápice y la base para próstatas de más de 50 mL. Se recomienda grabar un barrido que visualice la zona de transición y un barrido en la configuración Pequeño para visualizar la zona periférica.
4. Evaluación diagnóstica
- Evaluar la zona de transición para las lesiones PRI-MUS.
- Una vez que se haya evaluado la zona de transición, cambie a la configuración de imagen pequeña y evalúe la zona periférica para lesiones PRI-MUS.
NOTA: Considere la posibilidad de practicar el uso de la biblioteca diagnóstica gratuita Micro-US para adquirir experiencia en la identificación y clasificación de las lesiones PRI-MUS11. - Anote la ubicación de las regiones de interés (ROI) encontradas registrando el ángulo central y los ángulos en los que el ROI es visible en primer y último lugar.
NOTA: En UF, estos ángulos son indicados por el cirujano y registrados en las notas operatorias por el personal de la sala de biopsias. - Si utiliza el software de fusión, cargue una resonancia magnética anotada previa a la biopsia y presione el botón de línea media mientras visualiza la uretra (Figura 2B).
5. Anestesia prostática
- Con una aguja de 6 pulgadas y 20 G, perfore la piel en el tracto de biopsia previamente anestesiado y avance la aguja hasta el elevador del ano bajo la visualización de Micro-US (Figura 2A).
- Coloque 3 mL del anestésico local en el complejo muscular del elevador del ano (Figura 2A).
- Avance la aguja de 20 G en el triángulo periapical (delimitado por la uretra medialmente, el elevador del ano lateralmente y la fascia de Denonvilliers posterior). Inyecte 5-7 mL de lidocaína en el triángulo periapical (Figura 2A).
NOTA: La cara lateral del complejo venoso dorsal (DVC) cae en el triángulo periapical; Por lo tanto, aspire antes de la inyección de lidocaína. La anestesia adecuada hidrodiseccionará entre la cápsula prostática y la fascia de Denonvilliers.
6. Biopsia de próstata
- Insertar un angiocatéter de 14 G o una aguja coaxial metálica de 15 G (aguja de acceso) a través del tracto previamente anestesiado hasta 5-10 mm del ápice prostático. Pase la aguja de acceso por encima del esfínter anal y a través de ella o medial hasta el elevador del ano. Personalice la distancia entre la aguja de acceso y el recto de acuerdo con la ubicación del ROI.
- Muestrear toda la próstata utilizando una ubicación de la aguja a 5 mm por encima del recto y a 15°-20° desde el plano medio de la próstata donde la uretra es visible (Figura 1D, posiciones de las 10 y las 2 en punto).
- Gire la sonda para que el plano de insonancia visualice la aguja de acceso y avance la pistola de biopsia hasta que la punta de la aguja de biopsia sea visible en el extremo de la aguja de acceso.
- Gire la sonda para visualizar el objetivo de la biopsia (ya sea el ROI o el núcleo sistemático) y, a continuación, gírela hacia atrás para visualizar la punta de la aguja de la biopsia. Ajuste la trayectoria de la aguja hacia el objetivo ajustando la pistola de biopsia externa al paciente.
- Haga avanzar la aguja bajo la visión y complete pequeños rollos de sonda de 3°-10° (micro rodillos) para guiar la punta de la aguja hacia el objetivo previsto. Solo avance la aguja de biopsia mientras visualiza la punta para evitar sobrepasar el objetivo previsto.
NOTA: Es necesario retirar la aguja de biopsia si se realizan movimientos más grandes hacia un objetivo. En esta técnica, la sonda se mantiene paralela a la uretra en lugar de paralela a la aguja ("guiñada"). La preservación del ángulo de la biopsia en relación con la uretra permite una reconstrucción precisa de la ubicación del cáncer y maximiza la comodidad del paciente. La parte más desafiante de esta técnica es visualizar la aguja cuando se desacopla del plano de insonación. En nuestra experiencia instruyendo a residentes, becarios y otros médicos, la memoria muscular necesaria para implementar la técnica requiere alrededor de 3 horas de práctica. Considere la posibilidad de practicar en un maniquí de próstata o en un simulador13 para desarrollar la memoria muscular necesaria antes de una biopsia. La realización de esta técnica inicialmente en un paciente anestesiado facilitará la transición a una práctica clínica. - Antes de obtener una muestra de biopsia, gírela hasta la uretra y asegúrese de que el ángulo esté dentro de 1°-2° de la posición 0°. Registre la posición del ángulo para cada disparo de biopsia capturando un fotograma o un bucle de cine.
NOTA: Por convención, la rotación del lado derecho (en sentido contrario a las agujas del reloj) se indica con un ángulo positivo, mientras que la rotación del lado izquierdo (en el sentido de las agujas del reloj) se caracteriza por un ángulo negativo. - Comience por obtener tres núcleos de biopsia distribuidos a través del ROI (Figura 2C).
- Considerar la realización de una biopsia sistemática transperineal (Figura 3). Para mayor eficiencia, se deben iniciar biopsias sistemáticas ipsilaterales al ROI. Si la ROI es anterior, bajar la aguja coaxial para mejorar la toma de muestras sistemáticas de biopsia de la zona periférica.
NOTA: En este estudio se realizó una biopsia sistemática de 14 punciones (Figura 3). Es probable que se pueda omitir una biopsia sistemática en estos casos: 1) núcleos sistemáticos que se superponen a un ROI muestreado previamente, y 2) próstatas pequeñas donde un solo tiro muestrea el ápice y la base. Utilizando esta plantilla, las biopsias apicales se obtienen comenzando el lanzamiento en la cápsula prostática apical. Las biopsias de base se obtienen iniciando el lanzamiento en la glándula media.
7. Fin del procedimiento
- Después de adquirir todas las biopsias, retire la aguja coaxial y la sonda de ultrasonido.
- Mantenga la presión sobre el perineo con una toalla durante 1-5 minutos hasta que se logre la hemostasia en el lugar de la punción.
- Ayude a los pacientes a sentarse y, después de 1 minuto, a ponerse de pie.
- Aconseje a los pacientes que esperen hematuria y hematospermia transitorias.
- Recetar a los pacientes con alfabloqueantes del flujo urinario restringido basal para que se llenen según sea necesario.
Resultados
Se describe un análisis retrospectivo de nuestra base de datos mantenida prospectivamente desde septiembre de 2021 hasta junio de 2022 (IRB202200022). El cáncer de próstata clínicamente significativo (csPCa) se consideró cáncer de próstata ≥Grupo 2 de grado 2 (Gleason 3 + 4 = 7). La tasa de detección de cáncer (CDR) se calculó como ≥GG2/total de pacientes. Las puntuaciones de dolor se evaluaron en una escala Likert de 1 a 10 puntos al inicio del estudio, en la colocación de la anestesia local, en la inserción de la sonda rectal y durante la biopsia. Los eventos adversos se discutieron con los pacientes a las 2 semanas después del procedimiento, y los eventos capturados por la revisión de la historia clínica se documentaron dentro de los 30 días posteriores a la biopsia. Los eventos adversos se calificaron utilizando la guía de calificación y atribución del CTEP (Programa de Evaluación de Terapias contra el Cáncer).
Se identificaron 100 pacientes que se sometieron a una biopsia transperineal clínica guiada por Micro-US bajo anestesia local. En este estudio, la CDR por paciente fue del 68%. El CDR varió en función de las puntuaciones PI-RADS (Prostate Image Reporting and Data System) y PRI-MUS de cada lesión (Tabla 1).
Las puntuaciones de dolor estaban disponibles en un subconjunto posterior de pacientes (N = 20). La mediana de las puntuaciones de dolor (RIC) fue de 0 (0, 1) al inicio, 2 (1, 4) durante la administración de anestesia local, 2 (1, 5) durante la colocación de la sonda transrectal y 2 (0, 5) durante la biopsia de próstata.
Los eventos adversos fueron relativamente raros, con una incidencia de 3% de eventos adversos de grado III (Tabla 2). No hubo eventos de Grado IV o Grado V. Los eventos de Grado II involucraron principalmente la nueva prescripción de alfabloqueantes para aliviar un flujo urinario más lento. Como se mencionó anteriormente, los pacientes fueron examinados para detectar síntomas antes de la biopsia. Los eventos de grado III implicaron la hospitalización de tres pacientes. De acuerdo con la guía de atribución de CTEP, una hospitalización por hipotensión sintomática probablemente se relacionó con la biopsia de próstata secundaria a la absorción de lidocaína. El paciente experimentó una resolución espontánea de los síntomas dentro de las 12 h posteriores al seguimiento. Dos pacientes adicionales fueron hospitalizados (caída mecánica y alteración del estado mental) dentro de los 30 días posteriores a la biopsia. Incidentalmente, se encontró que tenían infecciones urinarias no sépticas y asintomáticas, posiblemente relacionadas con la biopsia. Aparte de estos pacientes específicos mencionados, no hubo casos de sepsis, prostatitis, cistitis u otras infecciones.
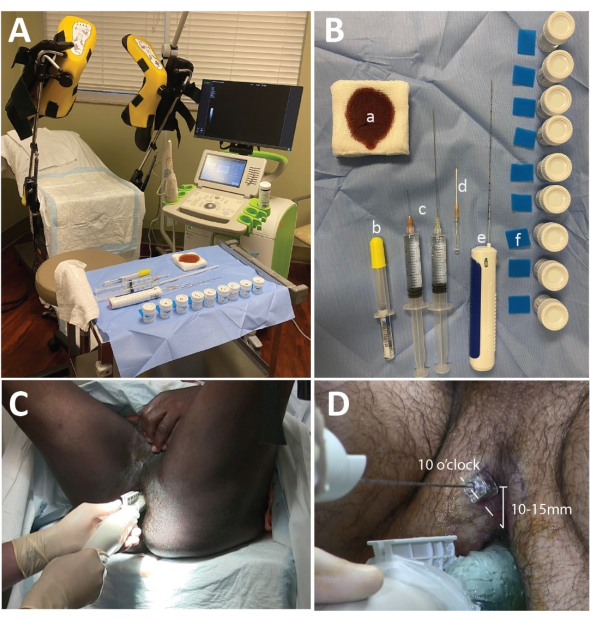
Figura 1: Configuración de microultrasonido, bandeja de biopsia y colocación de la aguja. (A) La configuración de la sala de procedimientos con la máquina ExactVu colocada a la derecha del cirujano. (B) Mesa de biopsia que incluye (a) almohadillas de gasa de 4 cm x 4 cm empapadas en betadine, (b) 10 mL de gel de lidocaína al 2%, (c) lidocaína al 1% con epinefrina 1:100,000 distribuida con 2 mL de solución de bicarbonato de sodio al 8.4% (1 mL de NaHCO3: 10 mL de lidocaína) en 2 jeringas de 20 mL con una aguja de 2 pulgadas y 25 G y una aguja de 6 pulgadas y 20 G, (d) una aguja de angiocath o de metal coaxial de 14 G, (e) una pistola de biopsia, (f) almohadillas de biopsia de espuma y recipientes de formalina. (C) La posición de la mano para realizar el barrido de diagnóstico. Tenga en cuenta que la mano izquierda soporta la presión ascendente sobre la próstata, mientras que la mano derecha gira la sonda. (D) La posición de la aguja coaxial o del angiocatéter: 10 en punto para la próstata del lado derecho y 2 en punto para la próstata del lado izquierdo (no se muestra). Haga clic aquí para ver una versión más grande de esta figura.
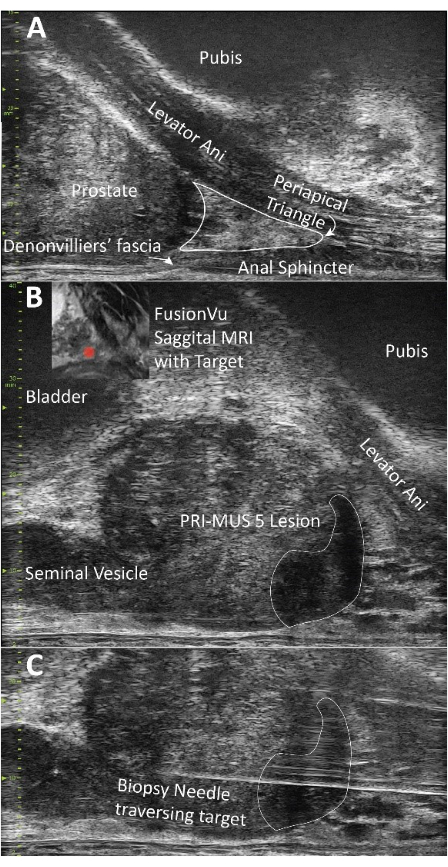
Figura 2: Demostración de la anatomía de la próstata y biopsia. (A) Visualización del elevador del ano y el triángulo periapical; Ambas son estructuras importantes a anestesiar para la implementación exitosa de esta técnica. (B) Demostración de una lesión PRI-MUS 5, anatómicamente concordante con la resonancia magnética previa a la biopsia. (C) Confirmación visual de la aguja de biopsia atravesando el objetivo. Haga clic aquí para ver una versión más grande de esta figura.

Figura 3: Plantilla de biopsia sistemática para la técnica propuesta. Esta plantilla se basa en la plantilla disponible en Michigan Urologic Surgery Improvement Collaborative (MUSIC)14. Sin embargo, esta plantilla es una mejora en tres aspectos. (i) Aumento del muestreo de la zona anterior (4 núcleos frente a 2 núcleos), (ii) Visualización muy mejorada de la ubicación del núcleo utilizando un modelo 3D, y (iii) nomenclatura de núcleo modificada para mejorar la usabilidad. En este protocolo, las biopsias sistemáticas se toman después de la biopsia ROI dentro de tejido negativo para imágenes (PRI-MUS ≤ 2). Haga clic aquí para ver una versión más grande de esta figura.
| PI-RADS 5 | PI-RADS 4 | PI-RADS 3 | |
| PRI-MUS 5 | 95% (n = 20) | 80% (n = 15) | 100% (n = 1) |
| PRI-MUS 4 | 100% (n = 1) | 69% (n = 13) | 75% (n = 4) |
| PRI-MUS 3 | 0% (n = 0) | 33% (n = 3) | NA |
Tabla 1: Detección de cáncer de próstata clínicamente significativo estratificado por las puntuaciones PI-RAD y PRI-MUS. Tasa de detección de cáncer de próstata (CDR) clínicamente significativa entre los pacientes con resonancia magnética y microecografía disponibles en el momento de la biopsia. El CDR está estratificado por las puntuaciones PI-RADS (columna) y PRI-MUS (fila). El número de pacientes que cumplen estos criterios se registra entre paréntesis.
| GRADO CLAVIEN DINDO | INCIDENCIA |
| GRADO I | 4% (n = 4) |
| GRADO II | 5% (n = 5) |
| GRADO III | 3% (n = 3) |
| GRADO IV | 0% (n = 0) |
| GRADO V | 0% (n = 0) |
Tabla 2: Porcentaje de pacientes que presentaron eventos adversos por grado. Porcentaje de pacientes con un evento adverso dentro de los 30 días posteriores a la biopsia de próstata. Tenga en cuenta que los eventos adversos de grado III fueron hospitalizaciones por eventos no sépticos, uno de los cuales probablemente estuvo relacionado con la biopsia y dos de los cuales posiblemente estuvieron asociados con la biopsia.
Discusión
Este manuscrito detalla el procedimiento y los resultados de la biopsia de próstata transperineal guiada por Micro-US a mano alzada bajo anestesia local. Esta es la primera descripción de una técnica que preserva la ubicación del núcleo de la biopsia y la comodidad del paciente. En nuestra experiencia, el procedimiento es preciso, bien tolerado y tiene eventos adversos mínimos.
En particular, no se informaron casos de sepsis o prostatitis a pesar de la falta de antibióticos profilácticos. Los resultados de la muestra utilizada aquí corroboran los hallazgos y la tasa de complicaciones del ensayo NORAPP, que no encontró un beneficio de los antibióticos profilácticos en la biopsia transperineal6.
Los pasos críticos del procedimiento son los siguientes. La desinfección y la anestesia señaladas en el paso 2.6 y la sección 5 son los componentes clave para reducir las tasas de infección al atravesar el perineo en lugar de la pared rectal, manteniendo la comodidad del paciente. En la sección 4 se delinean los ROI de los objetivos de biopsia, lo que permite tomar menos muestras y tomar muestras efectivas de las áreas problemáticas de la próstata.
La biopsia transperineal ha ganado popularidad en comparación con los métodos alternativos dada la tasa cero de sepsis15,16, la precisión de la toma de muestras de tumores anteriores, la administración de antibióticos y las recomendaciones de las guías17,18. Al mismo tiempo, Micro-US está siendo reconocido como una modalidad precisa de imágenes del cáncer, una plataforma de fusión simple y un biomarcador de imágenes independiente 9,19. Las técnicas transperineales guiadas por Micro-US previas informaron una excelente CDR del 42%; Sin embargo, esta técnica utilizaba una guía de aguja para alinear la aguja y el plano de insonación. Si bien el uso de una guía mejora la curva de aprendizaje, es probable que limite la biopsia al quirófano para permitir el uso de anestesia general, ya que cada punción de la biopsia ingresa a través de un nuevo sitio20. Reportamos un CDR del 68%, lo que demuestra que esta técnica a mano alzada tiene una precisión comparable al uso de una guía de aguja.
La precisión, tolerabilidad y eventos adversos mínimos de nuestra técnica deben interpretarse dentro de ciertas limitaciones. Se requieren aproximadamente 3 horas de práctica práctica en un simulador o maniquí para localizar y dirigir la aguja de biopsia. Es posible que se requiera tiempo adicional para aprender la interpretación de la imagen Micro-US. La realización de biopsias dirigidas y sistemáticas puede dar lugar a 17 o más núcleos de biopsia y requerir hasta 30 minutos de tiempo de procedimiento. Si bien reportamos excelentes tasas de detección de cáncer, el éxito de esta técnica se relaciona en parte con nuestra práctica de omitir la biopsia de próstata en pacientes con un riesgo calculado del <15% de csPCa21. Por último, la plantilla de biopsia sistemática utilizada en este estudio toma muestras de las áreas de mayor riesgo de la próstata, pero nunca se ha comparado con otras plantillas de biopsia transperineal. A pesar de estas limitaciones, esta técnica tiene varias ventajas, entre las que destaca la capacidad de realizar el procedimiento en un entorno clínico. Además, el seguimiento de la posición de la sonda micro-US permite la reconstrucción en 3D de las ubicaciones del cáncer para su uso cuando se realiza la extirpación quirúrgica, el refuerzo de radiación o la terapia focal.
En conclusión, Micro-US representa una mejora reciente en la biopsia de próstata. Demostramos un abordaje transperineal que se puede implementar en la clínica bajo anestesia local. Si bien se justifican más evaluaciones y mejoras en la capacidad diagnóstica de Micro-US, los cirujanos que adopten esta técnica la encontrarán fácil de implementar, precisa y segura.
Divulgaciones
Ninguno.
Agradecimientos
Ninguno.
Materiales
| Name | Company | Catalog Number | Comments |
| 14 ga Angiocatheter | BD Angiocath | BD382269 | |
| Aquasonic | Parker Labs | Aquasonic 100 | |
| Biopsy Needle | Bard | MaxCore | |
| Biopsy Sponge 2 mm x 25.4 mm x 30.2 mm | McKesson | 1019107 | |
| ExactVu Micro-Ultrasound Machine | ExactImaging | ||
| ExactVu Micro-Ultrasound Probe (EV29L) | ExactImaging | ||
| Guaze Sponge McKesson Cotton 12-Ply 4'' x 4'' | McKesson | 762703 | |
| Hypodermic Needle 25 G 1.5 inch | McKesson | 42142523 | |
| Lidocaine 1% with Epinephrine 1:100,000 | NA | ||
| Lidocaine 2% Gel, 20 mL | URO-Jet | 76329301505 | |
| Probe Cover | ExactImaging | ||
| Skin Prep Solution betadine (10%) | McKesson | 1073829 | |
| Spinal Needle 20 G, 6 inch | McKesson | 992546 | |
| TruGuide | Bard | C1616A |
Referencias
- Siegel, R. L., Miller, K. D., Fuchs, H. E., Jemal, A. Cancer statistics, 2022. CA: A Cancer Journal for Clinicians. 72 (1), 7-33 (2022).
- Onur, R., Littrup, P. J., Pontes, J. E., Bianco, F. J. Contemporary impact of transrectal ultrasound lesions for prostate cancer detection. The Journal of Urology. 172 (2), 512-514 (2004).
- Loeb, S., Carter, H. B., Berndt, S. I., Ricker, W., Schaeffer, E. M. Complications after prostate biopsy: Data from SEER-Medicare. The Journal of Urology. 186 (5), 1830-1834 (2011).
- Borghesi, M., et al. Complications after systematic, random, and image-guided prostate biopsy. European Urology. 71 (3), 353-365 (2017).
- Pradere, B., et al. Nonantibiotic strategies for the prevention of infectious complications following prostate biopsy: A systematic review and meta-analysis. The Journal of Urology. 205 (3), 653-663 (2021).
- Jacewicz, M., et al. Antibiotic prophylaxis versus no antibiotic prophylaxis in transperineal prostate biopsies (NORAPP): A randomised, open-label, non-inferiority trial. The Lancet. Infectious Diseases. 22 (10), 1465-1471 (2022).
- Ahmed, H. U., et al. Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer (PROMIS): A paired validating confirmatory study. The Lancet. 389 (10071), 815-822 (2017).
- Kasivisvanathan, V., et al. MRI-targeted or standard biopsy for prostate-cancer diagnosis. The New England Journal of Medicine. 378 (19), 1767 (2018).
- Sountoulides, P., et al. Micro-ultrasound-guided vs multiparametric magnetic resonance imaging-targeted biopsy in the detection of prostate cancer: A systematic review and meta-analysis. The Journal of Urology. 205 (5), 1254-1262 (2021).
- Ghai, S., et al. Assessing cancer risk on novel 29 MHz micro-ultrasound images of the prostate: Creation of the micro-ultrasound protocol for prostate risk identification. The Journal of Urology. 196 (2), 562-569 (2016).
- Exact Imaging E-learning. Exact Imaging Available from: https://elearn.exactimaging.com/learn (2022)
- Siddiqui, E. J., Ali, S., Koneru, S. The rectal administration of lignocaine gel and periprostatic lignocaine infiltration during transrectal ultrasound-guided prostate biopsy provides effective analgesia. Annals of the Royal College of Surgeons of England. 88 (2), 218-221 (2006).
- Zhang, Z., et al. Attitude is everything: Keep probe pitch neutral during side-fire prostate biopsy. A simulator study. BJU International. 128 (5), 615-624 (2021).
- Prostate Biopsy. Michigan Urological Surgery Improvement Collaborative (MUSIC) Available from: https://musicurology.com/programs/prostate/transperinealbiopsy/ (2022)
- Sigle, A., et al. Safety and side effects of transperineal prostate biopsy without antibiotic prophylaxis. Urologic Oncology: Seminars and Original Investigations. 39 (11), (2021).
- Grummet, J. P., et al. Sepsis and "superbugs": Should we favour the transperineal over the transrectal approach for prostate biopsy. BJU International. 114 (3), 384-388 (2014).
- Pilatz, A., et al. European association of urology position paper on the prevention of infectious complications following prostate biopsy. European Urology. 79 (1), 11-15 (2021).
- Meyer, A. R., et al. Transperineal prostate biopsy improves the detection of clinically significant prostate cancer among men on active surveillance. The Journal of Urology. 205 (4), 1069-1074 (2021).
- Avolio, P. P., et al. The use of 29 MHz transrectal micro-ultrasound to stratify the prostate cancer risk in patients with PI-RADS III lesions at multiparametric MRI: A single institutional analysis. Urologic Oncology: Seminars and Original Investigations. 39 (12), 1-7 (2021).
- Rodríguez Socarrás, M. E., et al. Prostate mapping for cancer diagnosis: The Madrid protocol. Transperineal prostate biopsies using multiparametric magnetic resonance imaging fusion and micro-ultrasound guided biopsies. The Journal of Urology. 204 (4), 726-733 (2020).
- Kinnaird, A., et al. A prostate cancer risk calculator: Use of clinical and magnetic resonance imaging data to predict biopsy outcome in North American men. Canadian Urological Association Journal. 16 (3), 161-166 (2022).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados