Method Article
الاستئصال التشريحي طفيف التوغل للجزء الثامن من الكبد بناء على منطقة البوابة لعلاج سرطان الخلايا الكبدية
* These authors contributed equally
In This Article
Summary
توضح هذه الدراسة بالتفصيل تقنيات استئصال المقطع S8 بالمنظار ، مع التركيز على الانتقال من الاستئصال الجزئي إلى الاستئصال التشريحي الذي يسترشد بالتنقل في عنيق البوابة. أدى الفهم التشريحي ثلاثي الأبعاد المعزز ، والمهارات المكررة طفيفة التوغل ، وإتقان الموجات فوق الصوتية أثناء الجراحة إلى تحسين الدقة والسلامة الإجرائية ، وتقليل المضاعفات مع تحسين النتائج الجراحية الكبدية من خلال بروتوكولات الاستئصال التشريحي المنهجية.
Abstract
استئصال الكبد هو العلاج الأساسي لسرطان الخلايا الكبدية (HCC) ويصنف إلى استئصال الكبد التشريحي واستئصال الكبد غير التشريحي بناء على مدى الاستئصال. يستخدم استئصال الكبد التشريحي جزء الكبد أو الجزء الفرعي من منطقة البوابة (PT) كوحدة تشريحية أساسية ، حيث يقوم باستئصال PT الحامل للورم بشكل منهجي وإزالة نظام Glisson الذي يوفر ويحدد هذه المنطقة لتعزيز فعالية الأورام. يتبع استئصال الكبد غير التشريحي مبدأ استئصال الأورام الجذري ، مع التركيز على إزالة أنسجة الكبد على بعد أكثر من 1 سم من هامش الورم. مع تعميم مفاهيم الجراحة الدقيقة ، تم تطبيق استئصال الكبد التشريحي طفيف التوغل على أساس PTs على نطاق واسع. ومع ذلك ، لا يزال الاستئصال طفيف التوغل للجزء S8 من الكبد يعتبر أحد أكثر عمليات استئصال الكبد تحديا. نجحنا في إجراء استئصال تشريحي لجزء منطقة البوابة S8 من الكبد باستخدام الموجات فوق الصوتية أثناء الجراحة وتنظير البطن الفلوري وتقنيات تشريح غشاء Lannaec ، مما حقق نتائج سريرية جيدة على المدى القصير.
Introduction
سرطان الخلايا الكبدية ، المعروف باسم سرطان الكبد ، هو أحد أكثر الأورام الخبيثة شيوعا في الصين. في عام 2022 ، كانت هناك 367,700 حالة إصابة جديدة بسرطان الكبد في الصين ، مما يجعلها رابع أعلى حالة من حيث الإصابة. بلغ عدد الوفيات 316,500 ، مما يجعله السبب الرئيسي الثاني للوفيات المرتبطة بالسرطان1. يوفر استئصال الكبد واحدة من أفضل الفرص للبقاء على قيد الحياة على المدى الطويل لدى مرضى سرطان الكبد2. يمكن تصنيف استئصال الكبد إلى استئصال الكبد التشريحي (AR) واستئصال الكبد غير التشريحي (NAR) بناء على مدى الاستئصال. يتضمن الواقع المعزز الاستئصال الكامل لأجزاء الكبد المستقلة تشريحيا أو الأجزاء المدمجة ، جنبا إلى جنب مع الحمة الكبدية داخل فروع الوريد البابي الحاملة للورم ، لتحقيق نتائج أفضل للأورام وتجنب المضاعفات من المناطق الإقفارية أو الاحتقانية المتبقية. تنعكس ميزة AR في شمولية استئصال الورم والحفاظ الكامل على القنوات الكبدية المتدفقة والخارجة للكبدالمتبقي 3. من ناحية أخرى ، يشير NAR ، المعروف أيضا باسم استئصال الكبد غير المنتظم ، إلى استئصال أنسجة الكبد على بعد أكثر من 1 سم من هامش الورم بناء على مبادئ استئصال جذور الأورام. لا تلتزم هذه الطريقة الجراحية بشكل صارم بالتجزئة التشريحية للكبد ولكنها مصممة وفقا لموقع الورم وحجمه ، بهدف الحفاظ على أكبر قدر ممكن من أنسجة الكبد الطبيعية مع ضمان هامش آمن لاستئصال الورم.
مع تقدم مفاهيم الجراحة الدقيقة والفهم الأعمق لتشريح الكبد ، اكتسبت نظرية وممارسة استئصال الكبد التشريحي على أساس منطقة البوابة (PT-AR) اعترافا وترويجا أوليا في السنوات الأخيرة4. يتضمن PT-AR إعادة بناء ثلاثية الأبعاد قبل الجراحة وتحليل الحوض لتحديد منطقة البوابة الحاملة للورم (PT) والتخطيط للجراحة وفقا لذلك. أثناء الجراحة ، يتم استخدام أجزاء الكبد أو الأجزاء الفرعية داخل الحوض كوحدات تشريحية أساسية ، مع كون الملاحة تلطيخ التألق باللون الأخضر الإندوسيانين (ICG) هي الطريقة الأساسية ، والتي تكملها تعريض الأوردة الكبدية التمثيلية بين القطاعات (IHVs). ثم يتم تشريح الكبد على طول الشقوق الفسيولوجية لتحقيق استئصال كامل لحوض البوابة الحامل للورم مع ضمان السلامة والحفاظ الوظيفي على بقايا الكبد المستقبلية (FLR). يعد البزل الموجه بالموجات فوق الصوتية أثناء الجراحة للتلوين الإيجابي للبوابة أو التلوين الرجعي بعد ربط عنيق الكبد المستهدف مطلبا تقنيا أساسيا لتحقيق PT-AR.
يتم الاعتراف باستئصال الكبد بالمنظار لنهجه طفيف التوغل ونتائج التعافي الفائقة عند مقارنته بالجراحة المفتوحة التقليدية. ومع ذلك ، يختلف تعقيد استئصال أجزاء الكبد المختلفة. إن موقع الجزء الثامن من الكبد في أعماق الجزء العلوي من البطن ، بالقرب من الأوردة الكبدية والوريد الأجوف السفلي ، جنبا إلى جنب مع التحدي المتمثل في الوصول المباشر إلى عنيق Glissonean للجزء الثامن ، يجعل استئصال الكبد التشريحي بالمنظار أمرا صعبا بشكل خاص لهذا الجزء5،6،7،8،9.
توضح هذه الدراسة الاستئصال التشريحي الإقليمي الوريدي البابي لجزء الكبد S8 لسرطان الخلايا الكبدية. هدفنا هو تفصيل التقنية والخطوات الرئيسية لهذه الجراحة ، بما في ذلك تقنية البزل الموجه بالموجات فوق الصوتية بالمنظار وتقنية تشريح عنيق الكبد على أساس غشاء Lannaec. من خلال مشاركة هذا البروتوكول ، نأمل في تقديم أدلة تدعم جدوى وسلامة استئصال الكبد التشريحي الإقليمي الوريدي بالمنظار في علاج سرطان الخلايا الكبدية S8 ، مما يؤدي في النهاية إلى تحسين نتائج علاج المرضى.
Protocol
التزمت الدراسة التي تضمنت استئصال الكبد التشريحي بالمنظار للجزء 8 (LALR-S8) بالممارسات الأخلاقية القياسية. حصلت على موافقة من لجنة الأخلاقيات في مستشفى شنتشن الشعبي (LL-KY-2020462). بالإضافة إلى ذلك ، تم الحصول على موافقة خطية مستنيرة من كل مريض ، مما يضمن امتثال البحث لمعايير ومتطلبات أخلاقيات الطب.
1. اختيار المريض
- استخدم معايير التضمين التالية:
- إجراء LALR-S8 على المرضى الذين يعانون من أورام الكبد الحميدة أو الخبيثة والتأكد من خضوعهم لتقييمات القلب والرئة القياسية واختبارات الدم والتقييمات الكيميائية الحيوية. تأكد من عدم وجود موانع للجراحة أو التخدير.
- إجراء التصوير قبل الجراحة ، بما في ذلك تصوير الأوعية المقطعية للبطن ، وإعادة بناء الكبد والأوعية الدموية ثلاثية الأبعاد ، والتصوير بالرنين المغناطيسي المعزز ، بالإضافة إلى حسابات أحجام الكبد المتبقية والقياسية.
- استخدم معايير الاستبعاد التالية: المرضى الذين يعانون من وظائف الكبد المصنفين على أنهم Pugh-Child Class C. أولئك الذين لا يستطيعون تحمل التخدير العام. المرضى الذين يعانون من النقائل داخل الكبد أو خارج الكبد. أولئك الذين خضعوا لعملية جراحية مفتوحة. والمرضى الذين تلقوا عمليات الاستئصال القطعي أو العلاجات الجراحية المشتركة الأخرى.
2. التحضير قبل الجراحة ، الموقف الجراحي ، والتخدير
- التحضير قبل الجراحة
- التاريخ والفحص البدني: تقييم وظائف الكبد ، وملف التخثر ، واختبار تصفية ICG ، والحالة الصحية العامة.
- التصوير: احصل على تصوير مفصل قبل الجراحة (على سبيل المثال ، التصوير المقطعي المحوسب للبطن ، والتصوير بالرنين المغناطيسي ، وإعادة بناء الكبد والأوعية الدموية ثلاثية الأبعاد) لتحديد تشريح الجزء 8 من الكبد والأوعية الدموية (الشكل 1)
- الصيام: تأكد من التزام المريض بتعليمات الصيام ، بدءا من منتصف الليل في اليوم السابق للجراحة.
- الأدوية: قم بإعطاء المضادات الحيوية الوقائية إذا لزم الأمر ومراجعة أي أدوية قد تؤثر على النزيف أو وظائف الكبد.
- الموافقة المستنيرة والتثقيف: شرح الإجراء بالمنظار ، بما في ذلك أساليبه ومخاطره وفوائده ، والحصول على الموافقة المستنيرة.
- الوضع الجراحي
- وضعية الاستلقاء: ضع المريض على طاولة العمليات في وضع الاستلقاء.
- وضع Trendelenburg العكسي: قم بإمالة طاولة العمليات قليلا لتسهيل التعرض والوصول إلى الكبد.
ملاحظة: يساعد هذا الوضع على تحريك الكبد لأعلى وبعيدا عن الجزء العلوي من البطن. - التثبيت: قم بتثبيت المريض على طاولة العمليات لمنع الحركة أثناء العملية.
- تخدير
- التخدير العام: قم بإجراء التخدير العام لضمان بقاء المريض فاقدا للوعي ومرتاحا طوال الجراحة.
- التحريض والصيانة: استخدام عوامل الحث الوريدي (مثل البروبوفول) ومرخيات العضلات (مثل السكسينيل كولين) للتنبيب. الحفاظ على التخدير بالعوامل المستنشقة (مثل سيفوفلوران) والمسكنات التكميلية (مثل الفنتانيل). اضبط عمق التخدير لضمان التخدير الكافي وسلامة المرضى.
- المراقبة: راقب باستمرار معدل ضربات القلب وضغط الدم وتشبع الأكسجين في الدم ومستويات ثاني أكسيد الكربون في نهاية المد والجزر.
3. التقنيات الجراحية
- بعد التخدير بالاستنشاق الوريدي ، ضع المريض في وضع الاستلقاء الجانبي الأيسر بزاوية 30 درجة مع رفع الرأس والساقين منفصلتين. استخدم نهجا من خمسة منافذ لاستئصال الكبد ، مع الحفاظ على ضغط النفخ عند 11-13 مم زئبق ، والضغط الوريدي المركزي عند 3-5 سم H2O ، ومناورة برينجل المطبقة لمدة 10-15 دقيقة من الانسداد متبوعا بتحرير لمدة 5 دقائق.
- قم بعمل شق عمودي 2 سم تحت الحافة اليمنى للسرة ، وافتح طبقات جدار البطن بالتتابع للوصول إلى البطن. أدخل مبزلا مقاس 12 مم لإنشاء التهاب الصفاق الرئوي ، ثم أدخل منظار البطن في تجويف البطن.
- ضع خمسة مبازل على النحو التالي: مبزل واحد 12 مم في المنطقة فوق الإشعاعية للمراقبة ؛ مبزل واحد 5 مم عند الخط الإبطي الأمامي الأيمن ؛ مبزل واحد 12 مم أسفل الترقوة الإنسية اليمنى ؛ مبزل واحد 5 مم أفقيا 2 سم تحت عملية الخنجري ؛ ومبزل واحد 12 مم 2 سم فوق السرة (الشكل 2).
ملاحظة: تشمل الأدوات الجراحية الشائعة المستخدمة في استئصال الكبد الموجات فوق الصوتية بالمنظار أثناء الجراحة والمشرط التوافقي وأجهزة التخثر ثنائية القطب. - استخدم الموجات فوق الصوتية بالمنظار أثناء الجراحة (LUS) لتوجيه البزل ، مع ICG للتلوين الإيجابي للاستئصال التشريحي لجزء الكبد S8:
- تشريح الأربطة المحيطة وتحديد P8: قم بتشريح الأربطة المحيطة بفص الكبد الأيمن واستخدم مسبار LUS لتحديد فرع الوريد البابي للجزء 8 (P8) ، وضبط موضع البزل وزاوية الإبرة حسب الضرورة.
- إدخال مسبار الموجات فوق الصوتية والتلوين الإيجابي باستخدام ICG: أدخل مسبار الموجات فوق الصوتية بالمنظار BK من خلال منفذ المبزل مقاس 12 مم. ثقب P8 بإبرة تصوير الأقنية الصفراوية عبر الكبد عن طريق الجلد (PTC) 21 جم مسترشدة ب LUS. حقن 5-10 مل من ICG بنسبة 1.25٪ من خلال الإبرة لتلطيخ الجزء الثامن ، مما يضمن عدم وجود تدفق رجعي إلى الأجزاء المجاورة (الشكل 3)
- تلطيخ سلبي للاستئصال التشريحي لجزء الكبد S8 عبر نهج الهيلار:
- تشريح عنيق الكبد S8: كشف نقير الكبد الأمامي الأيمن بناء على غشاء Lannaec بين البوابة السادسة والبوابة V10. ثم, تشريح على طول الجانب البطني من عنيق الكبد الأمامي الأيمن ونحو الجانب رأسي على اليسار لفضح العنيق الكبدي S8; تعبئة ورفع هذه السنيق.
- الإرقاء والتلوين السلبي: بعد تشريح النقير ، ضع مشبك وعائي لإرقاء عنيق الكبد S8 (الشكل 4) وتأكد من الخط الإقفاري للجزء S8 ليشمل الورم. حقن 5-10 مل من ICG 1.25٪ من خلال الوريد المحيطي. ابحث عن الجزء الثامن الذي سيتم تحديده بواسطة التألق بعد 5 دقائق (الشكل 5).
- استئصال الكبد مسترشدا بواجهة الفلورسنت: راقب التألق للتأكد من أن المنطقة الملطخة تغطي الورم. قم بعمل شقوق على طول الواجهة بين المناطق الفلورية وغير الفلورية باستخدام مشرط بالموجات فوق الصوتية أو CUSA ، مع الحفاظ على الأوردة الكبدية بين القطاعات (الشكل 6).
ملاحظة: يمكن استئصال كل من الورم والجزء الكبدي أو الجزء الفرعي من PT بالكامل بهذه الطريقة. - الإرقاء والفحص: تحقيق الإرقاء عن طريق الكي الكهربائي أو الخياطة بعد استئصال الآفة. افحص موقع الاستئصال للتأكد من عدم وجود نزيف متبقي أو تسرب للصفراء. على المقطع العرضي ، لاحظ الأوردة المتقاطعة ونهاية الجزء P8 (الشكل 7).
النتائج
بين يناير 2022 وديسمبر 2023 ، خضع ما مجموعه 17 مريضا لاستئصال الكبد من الجزء S8. من بين هذه الحالات ، تضمنت سبع حالات استئصال غير تشريحي ، وست حالات كانت استئصال تشريحي عن طريق نهج متني كبدي ، وأربع حالات كانت استئصال تشريحي في منطقة البوابة. لم تكن هناك فروق ذات دلالة إحصائية في درجات Child-Pugh قبل الجراحة ، وحجم الورم ، ووظيفة احتياطي الكبد بين المجموعات. كان الوقت الجراحي لمجموعة الاستئصال التشريحي PT أطول من الوقت المخصص لمجموعات الاستئصال التشريحي غير التشريحي والنهج المتني الكبدي ، ويرجع ذلك أساسا إلى ثقب البوابة أو تشريح أجزاء الكبد المقابلة الصعبة نسبيا ، والتي تطلبت مزيدا من الوقت. لم تكن هناك فروق يعتد بها في فقدان الدم أثناء الجراحة بين المجموعات ، لكن ذروة مستوى ALT بعد الجراحة كان أقل في مجموعة الاستئصال التشريحي في منطقة البوابة مقارنة بالمجموعتين الأخريين ، على الأرجح لأن هذه المجموعة كانت تحتوي على أنسجة كبد أقل متبقية غير وظيفية. تجاوزت جميع الهوامش الجراحية 1 سم ، مع وجود هوامش أكبر لمجموعة الاستئصال التشريحي PT من المجموعتين الأخريين. لم يحدث تسرب للصفراء على أي حال ، ولم تكن هناك عمليات إعادة عمل غير مخطط لها. تم استخدام تحليل ANOVA أحادي الاتجاه لبيانات العد ، وتم استخدام اختبار الترتيب لبيانات القياس. وترد النتائج المحددة بالتفصيل في الجدول 1.
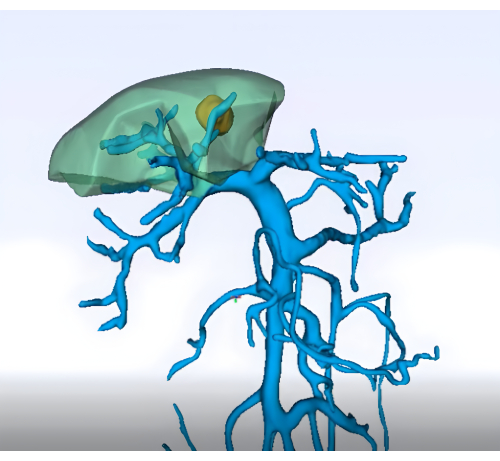
الشكل 1: تحليل ما قبل الجراحة لمنطقة الوريد البابي باستخدام تقنية إعادة البناء ثلاثية الأبعاد. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
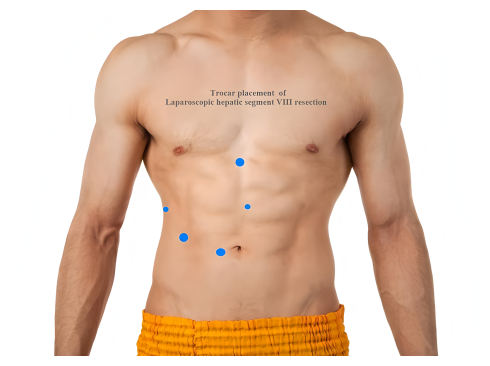
الشكل 2: وضع المبزل لاستئصال الجزء الكبدي الثامن بالمنظار. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
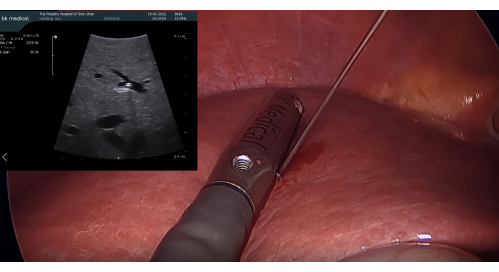
الشكل 3: ثقب P8 بإبرة PTC 21 G مسترشدة بمسبار الموجات فوق الصوتية بالمنظار. اختصار: PTC = تصوير الأقانية الصفراوية عبر الكبد عن طريق الجلد. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
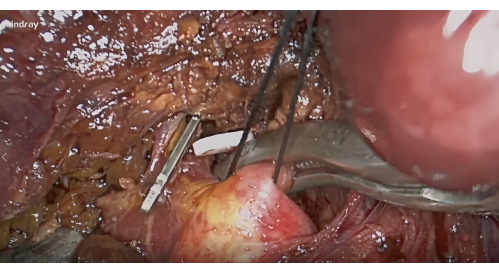
الشكل 4: تشريح العنقيق الكبدية للجزء الثامن على طول غشاء Lannaec والحصار بمشبك الأوعية الدموية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 5: وضع علامة على خط الاستئصال بعد التلوين السلبي. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
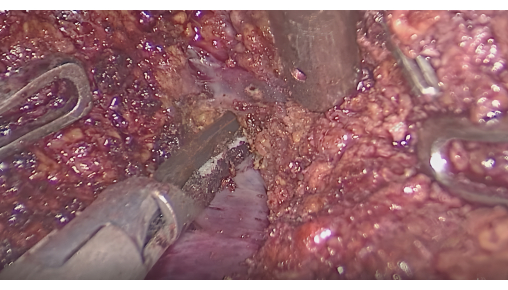
الشكل 6: تشريح حمة الكبد بين الأوردة بين القطاعات. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
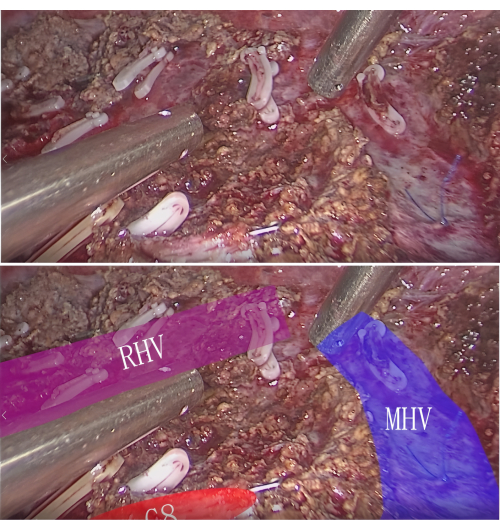
الشكل 7: الوريد بين الأجزاء وجذع P8 في قسم الاستئصال. الرجاء النقر هنا لعرض نسخة أكبر من هذا الشكل.
| الاستئصال غير التشريحي (ن = 7) | الاستئصال التشريحي من خلال نهج متني (ن = 6) | الاستئصال التشريحي القائم على المنطقة الوريدية (ن = 4) | قيمة F / χ2 | قيمة p | |
| درجة الطفل قبل الجراحة | 5.4±0.8 | 5.2±0.4 | 5.3±0.5 | 0.306 | 0.741 |
| حجم الورم (سم) | 3.4±1.5 | 3.1±0.8 | 2.8±0.6 | 0.454 | 0.644 |
| معدل الاحتفاظ ب ICG قبل الجراحة 15 دقيقة (٪) | - | - | - | 0.195 | 0.907 |
| وقت الجراحة (دقيقة) | 189±52 | 201±36 | 268±51 | 3.826 | 0.047 |
| فقدان الدم (مل) | 228±135 | 175±52 | 170±24 | 0.716 | 0.506 |
| الحد الأدنى للهامش الجراحي (سم) | 1.3±0.5 | 1.7±0.3 | 2.0±0.4 | 3.972 | 0.043 |
| ذروة ALT بعد الجراحة (U / L) | 328±109 | 219±45 | 152±38 | 7.045 | 0.008 |
| يوم ما بعد الجراحة 5 مستويات البيليروبين (ميكرومول / لتر) | 17.2±8.2 | 18.1±4.2 | 14.7±4.3 | 0.389 | 0.685 |
| وقت الخروج بعد الجراحة (أيام) | 7.5±1.3 | 6.7±0.8 | 6.3±1.0 | 2.279 | 0.139 |
| تسرب الصفراء بعد الجراحة | 0 | 0 | 0 | - | - |
| إعادة التشغيل غير المخطط لها | 0 | 0 | 0 | - | - |
الجدول 1: مقارنة البيانات السريرية بين المجموعات المختلفة.
Discussion
لا يزال استئصال الجزء S8 من الكبد ، وخاصة الاستئصال التشريحي ، يمثل تحديا كبيرا11. لم يحظ الأساس النظري لاستئصال الكبد التشريحي القائم على عنيق البوابة بقبول واسع النطاق داخل مجتمع جراحة الكبد. وبالتالي ، يواصل جراحو الكبد الصفراوي السعي وراء أدلة سريرية قوية لتقييم القيمة العلاجية لاستئصال الكبد التشريحي بشكل موضوعي. مكنت التطورات الحديثة في إعادة التصور التشريحي الكبدي ، لا سيما فيما يتعلق بكبسولة Laennec ونظرية القطاعات الستة ، من الناحية النظرية التحديد الدقيق وتشريح العنقيق الكبدي الفردي المقابل لأجزاء أو أجزاء فرعية محددة. أدى دمج تنظير البطن الفلوري والتصوير بالموجات فوق الصوتية بالمنظار إلى تسهيل تحقيق استئصال الكبد التشريحي بالمنظار ، مما يسمح بالتصور في الوقت الفعلي لحدود التروية الإقليمية والملاحة أثناء الجراحة. وفقا لمؤتمر إجماع خبراء طوكيو لعام 202112 ، يتم تعريف الاستئصال التشريحي على أنه الإزالة الكاملة لأجزاء الكبد المرتبطة بمناطق أوريد بوابة محددة ، والتي تحددها فروع الوريد البابي الثلاثي. يتميز استئصال الكبد التشريحي بالاستئصال الكامل لأجزاء الكبد المستقلة تشريحيا أو الأجزاء الفرعية أو الأجزاء المركبة11،13. بالمقارنة مع استئصال الكبد غير التشريحي ، يزيل الاستئصال التشريحي في نفس الوقت أجزاء الكبد المقابلة المرتبطة بمنطقة فرع الوريد البابي ذات الصلة ، مما يقلل نظريا من خطر انتشار الورم من خلال تدفق الدم الوريدي البابي في جزء الكبد المصاب ويقلل من مضاعفات ما بعد الجراحة. وبالتالي ، يعتبر حاليا النهج الجراحي المفضل لسرطان الكبد14.
يتم تحديد المستويات بين القطاعات أو القطاعية للكبد من خلال حدود مناطق الوريد البابي. يشار إلى الأوردة الكبدية التي تعبر هذه الطائرات باسم الأوردة بين القطاعات ، والتي تعمل كمعالم مهمة أثناء استئصال الكبد ، مما يسمح بالتعرف الدقيق من خلال التعرض المستمر في مستوىالقطع 15. تتطلب هذه الطريقة خبرة في تصوير الكبد بالموجات فوق الصوتية ، والاستخدام الماهر ل LUS ، وتقنيات الثقب ، والتي تتطلب منحنى تعليمي. بناء على تجربتنا ، يعد التطبيق الماهر للموجات فوق الصوتية أثناء الجراحة أمرا بالغ الأهمية لتعزيز معدلات النجاح الجراحي وسلامة المرضى. يجب أن يبدأ الجراحون على جميع المستويات بالتعرف على التعرف على التصوير بالموجات فوق الصوتية وتفسيره من خلال التدخلات الروتينية بالموجات فوق الصوتية عن طريق الجلد ، وإتقان المهارات التشغيلية الأساسية. بعد ذلك ، يجب أن يتقدموا إلى تطبيق الموجات فوق الصوتية في العمليات الجراحية المفتوحة ، وتعلم كيفية استخدام الموجات فوق الصوتية لتوجيه استئصال الكبد وتقييم أورام الكبد. ستعزز هذه المرحلة من التدريب فهم الجراحين للهياكل التشريحية أثناء الجراحة. في النهاية ، يجب أن يهدف الممارسون إلى إتقان استخدام الموجات فوق الصوتية أثناء الجراحة في إجراءات التنظير البطني لتحقيق دقة أكبر ، خاصة في المواقف ذات التصور المحدود. من خلال عملية التعلم والممارسة التدريجية هذه ، سيصبح الجراحون بارعين في استخدام تقنية الموجات فوق الصوتية في العمليات الجراحية المعقدة ، مما يعزز بشكل كبير السلامة والفعالية.
تهدف تقنية LALR-S8 إلى تحديد موقع إمداد الأوعية الدموية بشكل فعال للجزء S8 وتحديد المستوى بين القطاعات. كان Makuuchi et al. أول من اقترح طريقة لاستهداف الوريد البابي تحت توجيه الموجات فوق الصوتية ، متبوعا بحقن الصبغة لتوضيح نضح جزء الورم3. في عام 2008 ، Aoki et al. كان رائدا في تطبيق تقنية التصوير الفلوري لتوطين الجزء أثناء جراحة الكبد16. حاليا ، أصبحت الطريقة الموجهة بالفلورة ICG تحت LUS تقنية قياسية لتعزيز دقة استئصال الكبد التشريحي بالمنظار17. لا يعالج هذا النهج فقط محدودية الخطوط الإقفارية التي تكون مرئية فقط على سطح الكبد ، ولكنه يوفر أيضا تصورا في الوقت الفعلي لخطوط ترسيم الفلورسنت الواضحة على المستوى بين القطاعات. يتيح نهج Glissonean مع تلطيخ ICG الفلوري استئصال الكبد التشريحي مع زيادة الحفاظ على أنسجة الكبد المتبقية الوظيفية وتقليل النزيف أثناء الجراحة.
اقترح ماكوتشي أن استئصال الكبد التشريحي للجزء S8 يجب أن يتضمن أربع خطوات: (1) تحديد حدود جزء الكبد على السطح باستخدام تقنيات التلوين أو انسداد تدفق الدم. (2) إجراء استئصال حمة الكبد مسترشدا بالموجات فوق الصوتية ، باستخدام الوريد التاريخي لهذا الجزء من الكبد كحد ؛ (3) تحقيق التعرض الكامل للأوردة الكبيرة على سطح قطع الكبد ؛ (4) ربط نظام Glisson بالقرب من جذر الجزءالكبد 3. تتكون فروع الوريد البابي للجزء S8 بشكل أساسي من الفروع البطنية والظهرية. عادة ما يتشقق الفرع الظهري للجزء S8 بالقرب من جذر الوريد البابي الأمامي الأيمن ، بينما يتشقق فرع الوريد البابي للجزء S5 في جانبه النهائي ، مما يستلزم تلطيخ ثقب منفصل للفروع البطنية والظهرية. يوجد فرع بارز من الوريد الكبدي الأوسط (V8) يمتد بين الفرع الظهري للجزء S8 والوريد البابي الأمامي الأيمن ، وهو المسؤول عن التصريف الوريدي من S8. بعد الاستئصال الكلي للجزء S8 ، يمكن رؤية الوريد الكبدي الأوسط والوريد الكبدي الأيمن والوريد الأجوف السفلي على سطح القطع.
من يناير 2022 إلى ديسمبر 2023 ، خضع ما مجموعه 17 مريضا لاستئصال مقطعي الكبد S8. تعافى جميع المرضى وخرجوا دون أي مضاعفات كبيرة. تؤكد خبرتنا في جراحة الكبد على دمج المعرفة النظرية والمهارات العملية ، لا سيما في تعلم التشريح داخل الكبد المفصل ، والتوصية بممارسة التشريح باستخدام كبد الجثث. بالإضافة إلى ذلك ، نؤكد على أهمية إتقان تقنيات التنظير البطني من خلال التدريب على المحاكاة والمشاركة في الإجراءات طفيفة التوغل. يعد الإلمام بالعديد من أدوات التنظير الداخلي ، مثل المشارط التوافقية والموجات فوق الصوتية أثناء الجراحة ، أمرا بالغ الأهمية. علاوة على ذلك ، من الضروري الاستفادة من التدريب في الموقع واستخلاص المعلومات الجراحية لفهم نظرية وتقنيات استئصال الكبد التشريحي ، مع التركيز على زيادة التعقيد الإجرائي تدريجيا وتحقيق التبسيط في النهاية. يعد التطبيق البارع للموجات فوق الصوتية أثناء الجراحة ، والتعاون الوثيق داخل الفريق الجراحي ، والمراجعة الذاتية الشاملة للأداء الجراحي أمرا بالغ الأهمية. تعد آلية الإنقاذ الفعالة أثناء الجراحة أمرا حيويا ، مما يضمن التحويل في الوقت المناسب إلى الجراحة المفتوحة عند الضرورة وتأمين الدعم من كبار الجراحين لتعزيز النجاح الإجرائي.
من تجربتنا ، لدينا الأفكار التالية: (1) إتقان التشريح القطاعي ثلاثي الأبعاد من خلال تدريب الجثث مع التركيز على التشريح المجهري للعنيق Glissonean. (2) صقل مهارات التنظير البطني من خلال التدريبات طفيفة التوغل القائمة على المحاكاة لدقة الأداة. (3) تحسين أجهزة الطاقة (مشرط بالموجات فوق الصوتية / CUSA / ICG المضاء) من أجل التقسيم المتني الآمن. (4) تنفيذ التعلم متعدد الوسائط ، والجمع بين تحليل الفيديو واستخلاص المعلومات من الحالة لتحسين استراتيجية الواقع المعزز. (5) تعزيز تآزر الفريق من خلال التحكم في CVP الذي يديره طبيب التخدير والمساعدة الجراحية الماهرة. (6) إنشاء بروتوكولات الإنقاذ التي تحدد عتبات التحويل المفتوحة ومسارات تصعيد الجراحين الكبيرين.
ومع ذلك ، فإن هذه الدراسة لها بعض القيود ، لأنها لا تتضمن سوى حالات قليلة. بالإضافة إلى ذلك ، فإن الدراسة بأثر رجعي ، واختيار المريض محدود. هناك حاجة إلى دراسات مستقبلية مصممة بدقة أكبر لمقارنة مزايا وعيوب تقنيات استئصال الكبد طفيفة التوغل المختلفة. سنشارك خبراتنا على الفور عند الحصول على بيانات أكثر موثوقية.
Disclosures
ليس لدى المؤلفين أي تضارب في المصالح أو روابط مالية للإفصاح عنها.
Acknowledgements
تم دعم هذا العمل بمنح من مشروع صندوق البحوث الأساسية والتطبيقية لمقاطعة قوانغدونغ (رقم 2023A1515220114) ؛ المشروع الرئيسي للعلوم والتكنولوجيا للجنة ابتكار العلوم والتكنولوجيا في بلدية شنتشن ، (رقم KJZD20230923114120038) ، صندوق بناء الانضباط الطبي الرئيسي في شنتشن (رقم SZXK015) ؛ ومشروع بناء التخصص السريري الرئيسي في مقاطعة ووطني في قوانغدونغ ومشروع بناء التخصص السريري الرئيسي الوطني.
Materials
| Name | Company | Catalog Number | Comments |
| Bipolar electric coagulation forceps | Mindray | Seal 7 | For blood vessel coagulation and division |
| Fluorescence Endoscopic camera system | Mindray | R1 | An endoscopic camera system with 4K fluorescence imaging |
| Intraoperative Ultrasonic imaging system | ALOKA | UST-5418 | With the four-directional flexible linear array ultrasonic laparoscopic transducer, the intraoperative ultrasound support ultrasonic elastography, contrast ultrasound, and magnetic navigation guided puncture |
| Intraoperative Ultrasonic imaging system | Mindray | LAP13-4Cs | Four-directional flexible linear array ultrasonic laparoscopic transducer which supports support ultrasonic elastography and contrast ultrasound |
| SPSS 20.0 | statistical analysis software | ||
| Ultrasonic scalpel | Johnson & Johnson | ETHICON GEN11 | For blood vessel coagulation and division |
References
- Zheng, R. S., et al. Cancer incidence and mortality in China, 2022. Chinese Journal of Oncology. 46 (3), 221-231 (2024).
- Qin, S. Primary liver cancer diagnosis and treatment Expert Panel of the Chinese Ministry of Health Guidelines on the diagnosis and treatment of primary liver cancer (2011 edition). Chin Clin Oncol. 1 (1), 10(2012).
- Makuuchi, M., Hasegawa, H., Yamazaki, S. Ultrasonically guided subsegmentectomy. Surg Gynecol Obstet. 161 (4), 346-350 (1985).
- Wang, X., Cao, J., Li, J. Anatomic liver resection based on portal territory with margin priority for hepatocellular carcinoma. JAMA Surg. 159 (6), 710-711 (2024).
- Urade, T., et al. Laparoscopic anatomical liver resection using indocyanine green fluorescence imaging. Asian J Surg. 43 (1), 362-368 (2020).
- Fuks, D., Aldrighetti, L., Jiao, L. R., Wakabayashi, G., Limongelli, P. Laparoscopic management of hepatocellular carcinoma: A critical reappraisal. Surg Laparosc Endosc Percutan Tech. 27 (4), 203-205 (2017).
- Morimoto, M., et al. Minimally invasive anatomic liver resection: Results of a survey of world experts. J Hepatobiliary Pancreat Sci. 29 (1), 33-40 (2022).
- Goh, E. L., Chidambaram, S., Ma, S. Laparoscopic vs open hepatectomy for hepatocellular carcinoma in patients with cirrhosis: A meta-analysis of the long-term survival outcomes. Int J Surg. 50, 35-42 (2018).
- Ban, D., et al. A novel difficulty scoring system for laparoscopic liver resection. J Hepatobiliary Pancreat Sci. 21 (10), 745-753 (2014).
- Sugioka, A., Kato, Y., Tanahashi, Y. Systematic extrahepatic Glissonean pedicle isolation for anatomical liver resection based on Laennec's capsule: proposal of a novel comprehensive surgical anatomy of the liver. J Hepatobiliary Pancreat Sci. 24 (1), 17-23 (2017).
- Xie, Q., Gao, F. A commentary on 'approaches of laparoscopic anatomical liver resection of segment 8 for hepatocellular carcinoma: a retrospective cohort study of short-term results at multiple centers in China'. Int J Surg. 111 (1), 1646-1647 (2023).
- Ciria, R., et al. Study group of Precision Anatomy for Minimally Invasive Hepato-Biliary-Pancreatic surgery (PAM-HBP surgery). A snapshot of the 2020 conception of anatomic liver resections and their applicability on minimally invasive liver surgery. A preparatory survey for the Expert Consensus Meeting on Precision Anatomy for Minimally Invasive HBP Surgery. J Hepatobiliary Pancreat Sci. 29 (1), 41-50 (2022).
- Morimoto, M., et al. and Study group of Precision Anatomy for Minimally Invasive Hepato-Biliary-Pancreatic surgery (PAM-HBP surgery). Glissonean approach for hepatic inflow control in minimally invasive anatomic liver resection: A systematic review. J Hepatobiliary Pancreat Sci. 29 (1), 51-65 (2022).
- Fuks, D., Aldrighetti, L., Jiao, L. R., Wakabayashi, G., Limongelli, P. Laparoscopic management of hepatocellular carcinoma: A critical reappraisal. Surg Laparosc Endosc Percutan Tech. 27 (4), 203-205 (2017).
- Monden, K., et al. Landmarks and techniques to perform minimally invasive liver surgery: A systematic review with a focus on hepatic outflow. J Hepatobiliary Pancreat Sci. 29 (1), 66-81 (2022).
- Kang, L. -M., Zhang, F. -W., Yu, F. -K., Xu, L. Pay attention to the application of indocyanine green fluorescence imaging technology in laparoscopic liver cancer resection. World J Clin Cases. 12 (23), 5288-5293 (2024).
- Cassinotti, E., et al. European Association for Endoscopic Surgery (EAES) consensus on Indocyanine Green (ICG) fluorescence-guided surgery. Surg Endosc. 37 (3), 1629-1648 (2023).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved