Method Article
تجربة عشوائية وثلاثية التعمية وذات شواهد متوازية لتحفيز التيار المباشر عبر الجمجمة لإعادة التأهيل المعرفي بعد السكتة الدماغية
* These authors contributed equally
In This Article
Summary
تقدم هذه الدراسة بروتوكولا جديدا لتحفيز التيار المباشر عبر الجمجمة (tDCS) جنبا إلى جنب مع التحفيز المعرفي لمعالجة الإهمال المكاني بعد السكتة الدماغية. تضمن البيانات الأولية من المريض التجريبي جدوى الإجراء وتشير إلى الفعالية المحتملة ، مما يوفر أساسا لتجربة سريرية متوازية ثلاثية التعمية ومضبوطة في المستقبل.
Abstract
غالبا ما تؤدي السكتة الدماغية في نصف الكرة الأيمن إلى إهمال نصف مكاني ، وهي حالة معوقة يمكن أن تعيق عملية التعافي بشكل كبير. تم ربط الوجود المزمن للإهمال بنتائج أسوأ في كل من المجالات المعرفية والحركية. كعامل مساعد للتدخلات النفسية العصبية التقليدية ، اكتسب تحفيز التيار المباشر عبر الجمجمة (tDCS) - وهي تقنية غير جراحية تعدل الاستثارة العصبية من خلال التيارات الكهربائية منخفضة الكثافة - اهتماما لقدرته على تعزيز اللدونة القشرية ودعم التحسين الوظيفي لدى الأفراد المصابين.
في هذه الدراسة ، نقترح بروتوكول تدخل مشترك يهدف إلى تقليل أعراض الإهمال النصفي المكاني بعد السكتة الدماغية. يتكون من بروتوكول tDCS الكاثودي جنبا إلى جنب مع برنامج إعادة تأهيل عصبي محوسب مصمم خصيصا لإعادة تأهيل الإهمال النصفي المكاني.
تتمثل استراتيجية التعديل العصبي في تقليل فرط نشاط نصف الكرة الأرضية غير التالف بناء على نموذج التنافس بين نصفي الكرة الأرضية. يتكون التدخل من أسبوعين ، 10 جلسات (من الاثنين إلى الجمعة) ، 45 دقيقة لكل منها ، من tDCS والتحفيز المعرفي التقليدي المطبق بشكل متزامن. يتم تطبيق tDCS بواسطة جهاز عالي الوضوح (HD- tDCS) ذو 8 قنوات لمدة 20 دقيقة وبكثافة 2 مللي أمبير. يتم وضع الكاثود فوق القشرة الجدارية الخلفية اليسرى (P3 بعد نظام 10/20 لوضع قطب كهربية الدماغ [EEG]) ، ويتم وضع أقطاب الإرجاع في C3 و CP5 و CP1 و Pz و PO3 و PO7 و P7. تم إجراء تقييم عصبي ووظيفي في خط الأساس وبعد انتهاء التدخل.
الهدف الأساسي من هذه الدراسة هو وصف بروتوكول التصميم التجريبي المتوازي والعشوائي ثلاثي التعمية. ولضمان جدوى البروتوكول وفعاليته المحتملة، يقدم وصف شامل للإجراءات المطبقة على مشارك تجريبي واحد.
قد يؤدي دمج استراتيجيات التعديل العصبي tDCS في عمليات إعادة التأهيل المعرفي إلى تقصير أوقات التدخل وتحسين الحالة الوظيفية ونوعية حياة المرضى.
Introduction
السكتة الدماغية هي السبب الأكثر شيوعا للإعاقة في العالم لدى البالغين والسبب الثاني للوفاة بعد مرض القلب الإقفاري1. يصاب معظم المرضى الذين نجوا من السكتة الدماغية بحالات سريرية غير متجانسة للغاية ودرجات مختلفة من الإعاقة. ما بين 55٪ و 75٪ من مرضى السكتة الدماغية يعانون من قيود حركية تستمر بعد 6 أشهر من الإصابة2. بالإضافة إلى العواقب الجسدية ، فإن التعديلات المعرفية متكررةجدا 3. يؤثر هذا العجز سلبا على أداء أنشطة الحياة اليومية ، مما يحد من الاستقلال الوظيفي ونوعية حياة المرضى والأقارب4،5. يعد الإهمال النصفي المكاني من بين أكثر حالات ضعف الانتباه شيوعا بعد السكتة الدماغية ، حيث يحدث في حوالي 25٪ إلى 50٪ من الحالات6،7،8 ويرتفع إلى ما يصل إلى 80٪ في الأفراد المصابين بسكتات دماغية في نصف الكرة الأيمن9،10.
يشير الإهمال النصفي المكاني إلى صعوبة في حضور نصف الحقل المقابل إلى المنطقة المصابة ، كونه هذا عدم الانتباه المركزي (حذف الأشياء الموجودة في النصف الأيسر من الفضاء) أو الأناني (المريض لا يهتم بالأجزاء اليسرى من جسده). من الناحية الوظيفية ، يولد الإهمال صعوبات شديدة في استقلالية المريض ، سواء في الأنشطة الأساسية (مثل الاستمالة ، والملابس ، والأكل ، وما إلى ذلك) والأنشطة المفيدة للحياة اليومية (على سبيل المثال ، إدارة الأموال أو وسائل النقل العام أو المشي المستقل). علاوة على ذلك ، ارتبط وجود هذا التغيير بأوقات أطول في الاستشفاء وإعادة التأهيل ، وزيادة خطر السقوط ، وضعف التعافي الحركي ، وانخفاض احتمالية العودة إلى المنزل بعد الخروج من المستشفى11،12.
تم تنفيذ العديد من الاستراتيجيات لعلاج الإهمال النصفي المكاني. ضمن مناهج إعادة التأهيل التقليدية ، يمكننا التمييز بين الأساليب من أعلى إلى أسفل ومن أسفل إلى أعلى. الفرق الرئيسي بينهما هو مستوى المشاركة النشطة ووعي الشخص في المهام. ضمن هذه الأساليب ، كانت الإجراءات الأكثر استخداما حتى الآن هي التدريب على المسح البصري والتكيف المنشوري ، على التوالي13. تقنيات إعادة التأهيل الأخرى في الإهمال النصفي المكاني مع استخدام موقع مركزي واسع الاستخدام ، وتحفيز البصريات ، والسعرات الحرارية ، والدهليزية ، واهتزاز الرقبة ، والعلاجات الدوائية13،14،15،16. ومع ذلك ، فإن هذه العلاجات لها بعض القيود: مدة نتائجها محدودة للغاية ، ولها قابلية تطبيق منخفضة في المراحل الحادة أو تحت الحادة لأن شدة المرضى في هذه المراحل تتداخل مع تعاونهم في الأنشطة التي سيتمتنفيذها 17.
تحفيز التيار المباشر عبر الجمجمة (tDCS) هو تقنية تعديل عصبي آمنة غير جراحية قادرة على تعديل النشاط القشري عن طريق إحداث تيار كهربائي ضعيف في الدماغ يغير النشاط القشري ، ويمكن استخدامه لاستكمال إعادة التأهيل النفسي العصبي للإهمال النصفي المكاني. يعدل tDCS التنشيط العصبي التلقائي استجابة للمدخلات من مناطق الدماغ الأخرى. علاوة على ذلك ، يحفز tDCS تغييرات متشابكة بلاستيكية تشبه التقوية طويلة المدى (LTP) أو الاكتئاب طويل المدى (LTD) وحتى تستمر إلى ما بعد مدةالتحفيز 18.
عن طريق tDCS ، يمكن تعديل النشاط القشري عن طريق تطبيق تيار كهربائي منخفض الكثافة يتدفق من الأنود إلى الكاثود. يعدل tDCS نشاط الدماغ من خلال التأثير على عتبة جهد الفعل ، أو زيادته أو تقليله ، ولكن دون التسبب في إمكانات الفعل18. بشكل عام ، يؤدي الأنود إلى زيادة استثارة منطقة الدماغ التي يقع عليها ، بينما يحفز الكاثود تثبيط القشرية. لا تحتوي هذه التقنية على دقة مكانية عالية ، ولكن تم التغلب على هذا القيد من خلال ظهور أجهزة tDCS جديدة تسمى المواقع المتعددة أو عالية الوضوح (HD- tDCS). تسمح هذه الأجهزة بتكوينات مختلفة للأقطاب الكهربائية ، مثل تكوين حلقة كاثودية حول الأنود (أو العكس) من أجل زيادة أو تقليل الاستثارة القشرية في منطقة معينة من الدماغ. تعمل حلقة الكاثود بطريقة مشابهة لأقطاب الإرجاع ، مما يحد من منطقة التحفيز. بهذه الطريقة ، يتم تحقيق تحفيز أكثر تركيزا. أثبت tDCS فعاليته كنهج علاجي للتعافي الحركي بعد السكتة الدماغية19 ، وهناك بعض الأدبيات العلمية ذات النتائج الواعدة في إعادة تأهيل الإهمال النصفيالمكاني 20.
تجادل الفرضية الأكثر قبولا للإهمال النصفي المكاني بأنه يمكن تفسيرها بناء على نموذج التنافس في نصف الكرة الأرضية ، الذي اقترحه كينزبورن في عام 197721،22. وفقا لهذا النهج ، في الحالة القاعدية ، يثبط كلا نصفي الكرة الأرضية بعضهما البعض باستمرار بطريقة متبادلة. يحدث الإهمال المكاني النصفي بسبب عدم التوازن بينهما. بعد الإصابة ، لا يستطيع نصف الكرة التالف تثبيط نشاط نصف الكرة الأرضية المحفوظ بشكل فعال. ينتج عن هذا فرط النشاط المرضي في نصف الكرة الأرضية السليم بسبب عدم وجود تثبيط يمارسه التالف ، مما يقلل ، أكثر من ذلك ، من النشاط العصبي لنصف الكرة المصاب بسبب زيادة التثبيط الذي يمارس عليه23. لذلك ، فإن الخلل الوظيفي الذي يكمن وراء الإهمال النصفي المكاني ناتج عن نقص نشاط نصف الكرة التالف وفرط نشاط النصف السليم24.
مع هذا النموذج كخلفية نظرية ، يتم اقتراح استراتيجيات مختلفة لتحفيز الدماغ غير الغازية تهدف إلى تحسين أعراض الإهمال النصفي المكاني. يتم التعامل مع هذه الاستراتيجيات لتقليل فرط نشاط نصف الكرة الأرضية السليم ، أو زيادة نشاط نصف الكرة الأرضية المصاب ، أو مزيج من كليهما25،26.
أظهرت العديد من الدراسات إمكانات tDCS في تقليل أعراض الإهمال النصفي المكاني من خلال تطبيق كل من الأنودال17،27،28،29 والكاثودية17،29 tDCS في نصف الكرة الأرضية المصاب أو غير التالف ، على التوالي ، أو مزيج من كل من28،30،31،32. على الرغم من النتائج الواعدة ، هناك حاجة إلى مزيد من الأدلة التجريبية لمعرفة المعلمات الدقيقة ل tDCS لتحقيق أفضل النتائج ، وهو أمر ضروري لمعرفة ما إذا كان tDCS البؤري أكثر فعالية من مونتاج tDCS التقليدي. على حد علمنا ، تم تطوير جميع الأبحاث السابقة باستخدام tDCS التقليدية ، حيث كانت الدراسة الحالية هي الأولى التي استخدمت HD-tDCS لإعادة تأهيل الإهمال النصفي المكاني.
تشكل التدخلات القائمة على تحفيز الدماغ غير الجراحي نهجا سريريا واعدا للغاية بالنظر إلى النتائج المحدثة والآثار الضارة المحدودة وفقا للتحليلات والتلوية المختلفة والمراجعات33،34،35،36،37. بالإضافة إلى ذلك ، يعد tDCS تقنية آمنة للغاية ومحمولة ومنخفضة التكلفة ، ولهذا السبب زاد استخدامها كأولوية في الإعدادات السريرية والبحثية. كما أن سهولة تجميعه وقابليته للنقل يسمح باستخدام الجهاز في وقت واحد مع أداء أي نشاط آخر ، مثل إعادة التأهيل البدني أو المعرفي أو الأنشطة الوظيفية. وبالتالي ، هناك ما يبرر المزيد من الدراسات العشوائية الخاضعة للرقابة والعمى مع أحجام عينات أكبر للتحقق من صحة بروتوكولات tDCS التي تعزز تأثيرات مناهج التدخل التقليدية.
Protocol
تمت الموافقة على هذا المشروع من قبل لجنة أخلاقيات البحث السريري في 12 de Octubre Hospital (المرجع Nº CEIm: 19/180) ، وهو مسجل في www.clinicaltrials.gov (المعرف: NCT04458974). يوافق الباحثون على احترام جميع التشريعات الحالية المعمول بها فيما يتعلق بالبحوث السريرية وحماية البيانات (إعلان WMA في هلسنكي ، 2004 ؛ اللائحة (الاتحاد الأوروبي) 2016/679 والقانون الأساسي 3/2018 بشأن حماية البيانات الشخصية؛ القانون 41/2002 بشأن استقلالية المريض). وفقا للائحة (الاتحاد الأوروبي) 2016/679 بشأن حماية البيانات الشخصية، سيتم التعامل مع أي بيانات يتم جمعها من المشاركين بسرية تامة. يتبع بروتوكول tDCS إرشادات السلامة الدولية ل tDCS38.
ملاحظة: الهدف الأساسي من هذه الدراسة هو وصف بروتوكول تدخل tDCS لتجربة سريرية متوازية وعشوائية ثلاثية التعمية. ولتحقيق ذلك، يقدم وصف شامل للإجراءات، وترد في هذه الورقة نتائج طلب تجريبي للمشاركين. يتكون بروتوكول التدخل من برنامج من 10 جلسات يجمع بين tDCS الكاثودية (20 دقيقة ، 2 مللي أمبير) مع برنامج إعادة التأهيل النفسي العصبي المحوسب المصمم لتحسين الإهمال النصفي المكاني. يتم إجراء التقييمات العصبية النفسية والوظيفية في خط الأساس وبعد نهاية التدخل. يوضح الشكل 1 الجدول الزمني للبروتوكول. يوضح الشكل تقييم خط الأساس، والوصف التفصيلي للتدخل، والتقييم التالي للدراسة بعد التدخل. كانت مشاركة المريض طوعية بعد إبلاغه بالغرض من الدراسة والتوقيع على نموذج موافقة خطية مستنيرة. يجوز للمشارك الانسحاب من الدراسة في أي وقت. يفي المشارك في هذه الدراسة بجميع معايير التضمين والاستبعاد الموضحة في الجدول 1.
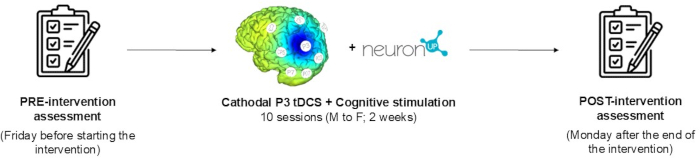
الشكل 1: الجدول الزمني للبروتوكول. يتم وصف جميع مراحل الدراسة: تقييم خط الأساس ، والوصف التفصيلي للتدخل ، والتقييم بعد التدخل. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
1. معايير الإدراج والاستبعاد
- التأكد من أن المشارك التجريبي في هذه الدراسة يستوفي معايير التضمين والاستبعاد التالية (الجدول 1).
| معايير الاشتمال: |
| السكتة الدماغية النزفية أو الإقفارية في نصف الكرة الأيمن |
| السكتة الدماغية بعد 3 إلى 12 شهرا من الحدث (بغض النظر عما إذا كانوا قد تلقوا إعادة تأهيل سابقة أم لا) |
| من 18 إلى 89 سنة |
| دراسة التصوير العصبي |
| غياب السكتات الدماغية السابقة |
| القدرة الوظيفية التي تسمح للمريض بالبقاء جالسا ونشطا لمدة ساعة واحدة (درجة مؤشر بارثيل أكبر من 5 في بند النقل بين الكرسي والسرير ؛ يمكن تسجيل هذا العنصر من 0 إلى 15 ، حيث يكون 0 يعتمد تماما و 15 مستقلا تماما). |
| الهيمنة اليدوية اليمنى |
| درجات الإهمال في اثنين على الأقل من الاختبارات التي تم إجراؤها لتقييم الإهمال البصري المكاني |
| توقيع موافقة مستنيرة من قبل المريض أو الوصي القانوني عليه |
| معايير الاستبعاد: |
| مشاكل الأمراض الجلدية (الصدفية والتهاب الجلد في فروة الرأس أو الوجه) |
| وجود غرسات أو أجزاء معدنية في الرأس باستثناء الحشوات. |
| أجهزة تنظيم ضربات القلب أو مضخات الأدوية أو المحفزات (المبهم أو الدماغي أو عبر الجلد) أو التحويلات البطينية أو مقاطع تمدد الأوعية الدموية. |
| وجود ضربات سابقة |
| مرض عصبي غير السكتة الدماغية الموصوف في معايير الاشتمال |
| تم تقييم الضعف الإدراكي الشديد باستخدام فحص الحالة العقلية المصغرة (MMSE) (فولشتاين ، 1975) ، باستثناء المرضى الذين لديهم درجات أقل من 24 (درجة MMSE بين 0 و 30 ، كونها 0 ضعف إدراكي شديد و 30 بدون ضعف إدراكي) |
| صعوبات لغوية كبيرة لا تسمح بالفهم السليم للأنشطة أو تحد بشدة من التعبير |
| تاريخ من تعاطي الكحول أو المخدرات |
| الاكتئاب النشط المعتدل أو الشديد |
| مشاكل طبية غير خاضعة للرقابة (أمراض في المرحلة الحادة دون علاج طبي أو دوائي مع فعالية مثبتة أو أمراض ذات مخاطر وشيكة على الحياة) |
| الحمل أو الحمل المشتبه به الذي سيتم فحصه عن طريق اختبار الحمل في بداية الدراسة لدى المرضى في سن الإنجاب ومع التوصية باستخدام وسائل منع الحمل حتى نهاية التدخل |
الجدول 1: معايير الإدراج والاستبعاد. يفي المشارك التجريبي في هذه الدراسة بجميع معايير التضمين والاستبعاد الموضحة في هذا الجدول.
2. المواد
ملاحظة: تم وصف جميع المواد المستخدمة في جميع مراحل الدراسة بدقة.
- طقم جهاز tDCS
- لتطبيق tDCS ، استخدم جهاز HD-tDCS ذو 8 قنوات وأقطاب كهربائية موصى بها (انظر الشكل 2). لتسهيل التجميع ، ضع قاعدة بلاستيكية في الموقع المطلوب على غطاء النيوبرين (باتباع نظام EEG 10/20). بمجرد وضعه ، ضع الجل الموصل ثم قم بتجميع القطب.
- منصة إعادة التأهيل العصبي المحوسبة
ملاحظة: لتنفيذ التحفيز المعرفي ، يتم استخدام منصة إعادة التأهيل العصبي المحوسبة عبر الإنترنت (انظر الشكل 3). تسمح المنصة بتصميم وتطبيق كل جلسة من برنامج التدخل ، وتكييف صعوبة المهام بشكل فردي.- قم بإنشاء مستخدم جديد لكل مريض من خلال النقر على إدارة المستخدم وإضافة مستخدم جديد. قم بالاسم باستخدام رمز الدراسة لتخصيص البرنامج المعرفي بشكل فردي.
- لتصميم المهام ، قم بالوصول إلى منطقة العمل / الجلسات / الجلسات الرقمية وانقر على تاريخ انعقاد الجلسة.
- أدخل اسم الدورة، على سبيل المثال، الجلسة 1. حدد رمزا ولونا لتلك الجلسة وانقر فوق الزر إنشاء .
- انقر فوق الأنشطة المراد تضمينها في البرنامج.
- تحقق من ظهور مهام كل جلسة على الجانب الأيسر من الشاشة.
- في كل منها ، قم ببرمجة المعلمات التالية: الوقت (7 دقائق) وابدأ من النتيجة الأخيرة (أشر فقط إلى نعم في الجلسات 3-10).
- أشر إلى الحفظ.
- كرر الخطوات 2.2.3-2.2.7 لتصميم كل جلسة من الجلسات العشر لبرنامج التحفيز المعرفي.

الشكل 2: طقم جهاز tDCS. (1) غطاء النيوبرين ، (2) جهاز tDCS ، (3) أقطاب كهربائية ، (4) كابلات ، (5) مشبك الأذن ، (6) جل موصل ؛ (7) حقنة لإدارة الجل الموصل تحت الأقطاب الكهربائية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
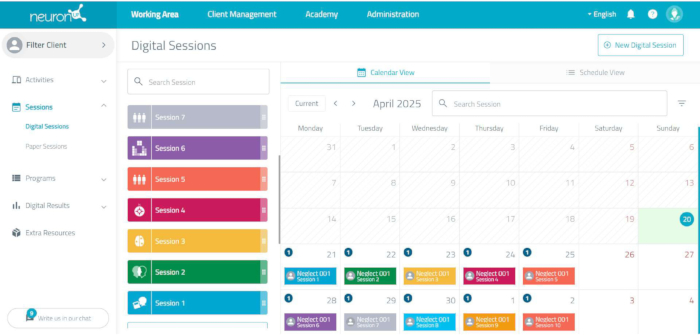
الشكل 3: جدولة جلسة منصة إعادة التأهيل العصبي. من خلال النقر على كل جلسة، يتم عرض المهام، بما في ذلك مدة كل مهمة والمدة الإجمالية للجلسة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
3. وصف بروتوكول التقييم: التقييم العصبي النفسي والوظيفي قبل التدخل:
ملاحظة: بمجرد توقيع المشارك على الموافقة المستنيرة ، يتم إجراء تقييم عصبي ووظيفي. يتم التقييم يوم الجمعة قبل بدء برنامج التحفيز ويستمر 50 دقيقة. خلال هذه الجلسة ، يتم تقييم الأداء المعرفي العام ، ويتم إجراء الاختبارات النفسية العصبية التي تركز على تقييم عمليات الانتباه والإهمال النصفي المكاني ، جنبا إلى جنب مع المقاييس الوظيفية. في جلسة إعلامية قبل التقييم الأول ، يتم تزويد المشارك بجميع التفاصيل اللازمة حول هدف الدراسة وإجراءاتها ومدة الجلسة والآثار السلبية المحتملة. يتم الحصول على الموافقة الموقعة قبل الشروع في التقييم والتدخل. يتم إبلاغ المشارك أيضا بخيار الانسحاب من الدراسة في أي وقت.
- فحص الحالة العقلية المصغر (MMSE) (5 دقائق)
ملاحظة: مقياس منظم بسيط. يسجل 30 نقطة كحد أقصى ، ويتم تجميع العناصر في 5 أقسام تقيم التوجه والذاكرة الفورية والانتباه والحساب والذاكرة المؤجلة واللغة والبناء. تتراوح النتائج من 0-30 نقطة ، مع نقطة القطع عند 24. تشير الدرجات التي تقل عن 24 إلى ضعف الإدراك.- اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار. تأكد من أن النتيجة الإجمالية هي ≥24 نقطة للمتابعة.
- إدارة اختبار التقسيم الخطي (5 دقائق)
ملاحظة: يتم تقديم ثمانية عشر سطرا في ورقة بحجم A4 منظمة في 3 مجموعات من 6: مجموعة واحدة تقع بشكل أساسي على يسار الورقة ، وواحدة في وسط الورقة ، وواحدة بشكل أساسي على يمين الورقة. يطلب من المرضى تحديد النقاط المركزية لكل سطر. يتم قياس انحراف علامة المريض عن المركز الحقيقي للخط لكل سطر ويبلغ متوسطه للخطوط ال 18.- ضع المهمة في المنتصف أمام المشارك ، مع الإشارة إلى الجانبين الأيمن والأيسر للمشارك على الورقة. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- إدارة اختبار الأجراس (5 دقائق)
ملاحظة: أداة تهدف إلى تقييم المسح البصري الأفقي في وجود مشتتات. تضمنت المهمة تحديد الأشكال على شكل جرس مرتبة بطريقة شبه عشوائية. تم عرضها في سبعة أعمدة عمودية ، يحتوي كل منها على خمسة أجراس. فيما يتعلق بوضعها على الورقة ، ظهرت ثلاثة أعمدة على اليسار ، وواحد في الوسط ، وثلاثة على اليمين.- ضع المهمة في المنتصف أمام المشارك ، مع الإشارة إلى الجانبين الأيمن والأيسر للمشارك على الورقة. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- اختبارات فرعية لرسم الصور من إدارة اختبار برشلونة (5 دقائق)
ملاحظة: يتكون من نسخة من 6 أشكال: دائرة ، مربع ، مثلث ، صليب ، مكعب ، ومنزل. يتم التحكم في وقت التنفيذ. يتم تسجيل كل رقم على النحو التالي: 3 نقاط للتكاثر المثالي ، 2 نقطة للتغيير المنفصل ، 1 نقطة للتغيير المعتدل ، 0 نقطة للتغيير الخطير. الحد الأقصى للدرجة هو 18. يكافأ ب 3 أو 2 أو 1 نقطة ، اعتمادا على الوقت الذي يقضيه في التنفيذ.- ضع المهمة في المنتصف أمام المشارك ، مشيرا إلى الصور التي تظهر. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- الاختبارات الفرعية للإلغاء من إدارة اختبار برشلونة (5 دقائق)
- ضع المهمة في المنتصف أمام المشارك ، مع الإشارة إلى الجانبين الأيمن والأيسر للمشارك على الورقة. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- إدارة امتداد الأرقام للأمام والخلف (5 دقائق).
- اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- قم بإدارة مهمة الأرقام المباشرة أولا. ثانيا ، قم بإدارة مهمة الأرقام العكسية بعد ذلك.
- اختبار قصير للانتباه (BTA) (5 دقائق)
- إدارة الجزء الأول من المهمة شفهيا (عد الأرقام التي تظهر في التسلسل). بعد ذلك مباشرة ، قم بتطبيق الجزء الثاني من الاختبار (عد الحروف التي تظهر في التسلسل)
- لا تسمح باستخدام الملاحظات أو العد على الأصابع.
- إدارة اختبار الوجه (5 دقائق)
- قدم ورقة اختبار الوجه. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- قم بتنشيط ساعة الإيقاف وإنهاء المهمة بعد 3 دقائق. احسب عدد المحفزات المميزة بشكل صحيح.
- إدارة اختبار الإدراك البصري الخالي من المحركات (MVPT-4) (15 دقيقة)
ملاحظة: يقيم اختبار الاختيار من متعدد المكون من 36 عنصرا 5 أبعاد فرعية للإهمال البصري المكاني: التمييز البصري ، والتمييز بين الشكل السفلي ، والعلاقة المكانية ، والإغلاق البصري ، والذاكرة البصرية. يتم استخدام معلمات مختلفة لتحديد سلوك الاستجابة اليسرى (سلوك الاستجابة اليسرى / اليمنى ، والنتيجة الإجمالية ، والأداء الأيسر / الأيمن ، ووقت معالجة الإدراك البصري). تتراوح درجات الاستجابات على الجانب الأيسر من 0 إلى 21 ، مع وجود قيم أقل تشير إلى إهمال بصري مكاني أكثر حدة.- ضع دفتر الواجب المنزلي أمام المريض. اشرح الاختبار للمشارك واطلب من المشارك اتباع تعليمات الاختبار.
- المقاييس الوظيفية
ملاحظة: إجراء مقابلات مع المريض وأفراد الأسرة / مقدم الرعاية لمعرفة الحالة الوظيفية للمريض وتأثير الإهمال على أنشطة الحياة اليومية.- قم بإدارة مقياس مؤشر بارثيل (5 دقائق) لأحد أفراد الأسرة أو مقدم الرعاية الأساسي وتسجيل الردود في ورقة الإجابات.
ملاحظة: يقيس مؤشر بارثيل قدرة الشخص على أداء عشرة أنشطة أساسية للحياة اليومية ، والحصول على تقدير كمي لدرجة استقلاليته. - قم بإدارة مقياس كاثرين بيرجيو (CBS) (5 دقائق) لأحد أفراد الأسرة أو مقدم الرعاية الأساسي وتسجيل الردود في ورقة الإجابات.
ملاحظة: يعتمد هذا الاستبيان على الملاحظة المباشرة لأداء المريض في 10 مواقف واقعية محاكاة سريريا ، بما في ذلك مهام مثل الاستمالة وارتداء الملابس واستخدام الكراسي المتحركة. تتم مقارنة تقييم المريض بتقييم أحد أفراد الأسرة / مقدم الرعاية الأساسي. ينتج عن هذا الاستبيان درجة تتراوح بين 0 و 30 ، حيث تعكس الدرجات الأعلى شدة أكبر للإهمال البصري المكاني. .
- قم بإدارة مقياس مؤشر بارثيل (5 دقائق) لأحد أفراد الأسرة أو مقدم الرعاية الأساسي وتسجيل الردود في ورقة الإجابات.
4. وصف بروتوكول التدخل
- تكوين جهاز التدخل
ملاحظة: قم بتعيين معلمات تحفيز HD-tDCS في البرنامج. قبل أيام من بدء التدخل ، يجب برمجة الجهاز بالمعلمات التي سيتم تطبيقها في التدخل ، أي المدة ، والشدة ، والقطبية ، والحالة (النشطة مقابل الزائفة) ، والمونتاج ، ونوع الأقطاب الكهربائية ، وموقع التحفيز ، ومواضع الأقطاب الكهربائية المرتجعة ، والنسبة المئوية للعودة الكهربائية إلى كل منها (انظر النقطة 5). تأكد من أن الجهاز يحتوي على بطارية كافية لإكمال الجلسة بأكملها.- افتح البرنامج، وحدد محرر البروتوكول، ثم أضف بروتوكولا جديدا.
- أدخل اسم البروتوكول. اضبط مدة المنحدر: الخطوات: (على اليسار).
- قم بتأكيد المنحدر وإجمالي وقت التحفيز. تشير إلى التكثيف: 30 والمنحدر: 30.
- في قسم مدة التحفيز الإجمالية ، حدد 20 دقيقة. اضبط إعدادات التحفيز والقطب: التصميم (يمين).
- اضبط قطبية التحفيز في الكاثود. قم بإعداد كل قطب كهربائي بشكل مستقل. ابدأ بالقطب النشط ، P3.
- حدد القطب الكهربائي P3 واسحبه إلى المربع الموجود على اليمين. حدد التحفيز والكاثودال. حدد 2000 ميكرو أمبير.
- حدد واسحب إلى اليسار ، واترك مسافة بين بقية الأقطاب الكهربائية واحدة تلو الأخرى. في هذه الحالات ، تكون جميعها أقطاب كهربائية عائدة وتقوم بنفس الإجراء ، مما يشير إلى النسبة المئوية للعائد في كل قطب.
ملاحظة: من المهم ملاحظة أن مجموع النسبة المئوية للعائد يجب أن يصل إلى 100. في هذه الدراسة ، كانت نسب العائد هي CP1 و PO3 و PO7 و P7 و CP5 و C3: 10٪ و PZ: 40٪ (انظر الشكل 4 والشكل 5). تم تصميم هذا المونتاج لتقليل فرط النشاط المرضي للقشرة الجدارية الخلفية في نصف الكرة الأرضية المقابل للآفة. - انقر فوق الزر "إنهاء" بمجرد اكتمال جميع الخطوات.
- تقييم المريض قبل التدخل
- تقييم الحالة العام.
- قبل وبعد كل جلسة tDCS ، قم بتقييم الحالة العامة من خلال طرح الأسئلة التالية: هل تشعر أنك على ما يرام؟ هل لديك صداع؟ هل تعاني من ألم في الرقبة؟ هل شربت الكحول بالأمس أم اليوم؟ هل تعاطيت المخدرات بالأمس أم اليوم؟ هل تناولت القهوة أو الشاي أو الشوكولاتة في آخر 5 ساعات؟ هل نمت جيدا الليلة الماضية؟ متى كانت آخر مرة أكلت فيها منذ ساعات؟
- تقييم المقاييس التناظرية البصرية (VAS) للإرهاق والمزاج.
- تقييم مستوى التعب العقلي والمزاج باستخدام اثنين من VAS المدارين ذاتيا. ردا على هذه الأسئلة ، اطلب من المشارك تقديم درجة بين 1 و 10 ، مشيرا إلى ما يشعر به فيما يتعلق بالأسئلة: ما مدى تعبك الآن؟، حيث 1 تعني لست متعبا على الإطلاق ، 10 تعني التعب الشديد ، وكيف هو مزاجك الآن؟، حيث 1 تعني حزينا جدا و 10 تعني سعيدا جدا.
- تقييم الحالة العام.
- مونتاج tDCS عالي الدقة
- قبل البدء في تجميع جهاز tDCS ، تحقق من توفر جميع المواد الضرورية وأن جهاز tDCS يحتوي على بطارية كافية لإجراء جلسة التحفيز.
- الجزء السفلي من البلاستيك من وضع القطب الكهربائي
- حدد في غطاء النيوبرين المواضع التالية: ضع قطب الكاثود النشط في P3 ؛ ضع أقطاب الإرجاع في C3 و CP5 و CP1 و Pz و PO3 و PO7 و P7 (انظر الشكل 5 والشكل 6).
- ضع الجزء السفلي من القطب في كل منطقة من المناطق المحددة من الغطاء. ضع الغطاء على رأس المشارك ، واضبط تشيكوسلوفاكيا بناء على القياسات التي تم إجراؤها مسبقا.
- وضع غطاء النيوبرين tDCS
- اجلس المشارك في وضع مريح على كرسي.
- ارتد غطاء النيوبرين (انظر الشكل 6) ، وحدد الحجم الذي يناسب رأس الهدف. تجنب اختيار غطاء كبير لأنه يجب أن يكون مشدودا على الرأس. اضبط الغطاء بعصابة الرأس حتى يتناسب بشكل مريح مع الرأس.
- حدد موقع نقطة تشيكوسلوفاكيا ومناطق التحفيز الخاصة بالبروتوكول.
- قم بقياس المسافة بين nasion و inion وبين نقاط الأذن باستخدام متر. حدد موقع نقطة تشيكوسلوفاكيا في منتصف كلا الموقعين.
- وضع هلام موصل كهربائيا
- افصل الشعر الموجود أسفل القطب عن مكان التحفيز. تأكد من الاتصال الجيد بين القطب الكهربائي والجلد ؛ استخدم جسما ممدودا يسمح بإزالة الشعر من داخل الأقطاب الكهربائية دون تعديل موضع الغطاء الذي تم قياسه مسبقا.
- تأكد من جفاف فروة الرأس دون أي تحضير إضافي آخر. قم بإزالة دبابيس الشعر أو العناصر المعدنية الأخرى (عصابات الرأس ، المشابك ، إلخ).
- لا تنظف الجلد بالكحول أبدا لأنه قد ينتج عنه تآكل باستخدام tDCS.
- إدخال ، باستخدام حقنة ذات طرف بلاستيكي نهائي ، كمية كافية من الجل الموصل للكهرباء في قاعدة كل قطب.
تنبيه: يمكن استخدام الجل الكهربائي فقط. لا تستخدم أبدا الماء أو المحلول الملحي في هذا النوع من الأقطاب الكهربائية لأنه قد يسبب التآكل. - قم بإزالة أكبر قدر ممكن من الشعر بمساعدة الطرف البلاستيكي للحقنة.
- فحص المعاوقة
ملاحظة: يقيس زر فحص المعاوقة مقاومة جميع القنوات النشطة والخلفية قبل التحفيز. يجب استخدامه قبل بدء أي بروتوكول تحفيز. يتم عرض مستويات المعاوقة كأشرطة مرمزة بالألوان أسفل كل رمز قناة تحفيز، مع الإشارة إلى اللون الأخضر إلى القيم المقبولة. لا يمكن أن يبدأ برنامج التحفيز إلا بعد ظهور جميع القنوات باللون الأخضر. أثناء التحفيز ، تتم مراقبة المعاوقة كل ثانية ، وإذا تجاوز أي قطب كهربائي 20 كيلو واط في أي لحظة ، مقاطعة البروتوكول تلقائيا.- قم بتشغيل الجهاز. افتح برنامج جهاز tDCS على الكمبيوتر.
- حدد الاتصال المستخدم مع الجهاز. حدد خيار الفحص بحثا عن الجهاز.
- حدد التحقق من المقاومة.
- إذا ظهرت جميع الأقطاب الكهربائية باللون الأخضر، فاضغط على زر التشغيل وسيبدأ برنامج التحفيز.
- إذا ظهر أي قطب كهربائي أحمر بعد الانتهاء من فحص المعاوقة ، فأعد وضع الجل على هذا القطب ، وقم بإزالة أي شعر ، وأعد فحص المعاوقة حتى تظل جميع الأقطاب الكهربائية خضراء.
- منصة إعادة التأهيل العصبي المحوسبة
ملاحظة: صمم جلسات التدخل العشر مسبقا على منصة إعادة التأهيل العصبي وقم بإعداد المنصة لها (انظر النقطة 2.2). تتكون كل جلسة من أربع مهام ، تستغرق كل منها 7 دقائق. وترد المهام المدرجة في كل جلسة في الجدول 2. عند جدولة كل جلسة ، من الضروري الاختيار من بين معلمات كل مهمة: المدة الزمنية لكل مهمة: 7 دقائق ، المدة الإجمالية للجلسة (28 دقيقة) ، اللغة ، تضمين تقييم المستخدم بعد كل نشاط ، تضمين تأكيد نهاية كل نشاط في نهاية كل مهمة ، وعدم وجود زر مستمر في كل مهمة ، حيث يجب القيام بالمهام بالتتابع واحدة تلو الأخرى (الشكل 7).- الوصول إلى منصة إعادة التأهيل العصبي المحوسبة.
- قم بالوصول إلى الجلسة المخطط لها مسبقا (انظر الخطوة 2.2) واضغط على زر البدء. قدم أربعة أنشطة تحفيز مختلفة مدة كل منها 7 دقائق بالتتابع.
ملاحظة: تبلغ مدة جلسة التحفيز المعرفي 30 دقيقة. بعد إجمالي وقت المحاكاة (30 دقيقة) ، تتوقف الأنشطة. يستمر التحفيز المعرفي لمدة 5 دقائق أخرى بعد نهاية تحفيز tDCS.
- برنامج تحفيز tDCS (20 دقيقة)
- قم بتنشيط بدء تحفيز tDCS بالضغط على زر التشغيل في برنامج التحكم tDCS بعد 4 دقائق و 20 ثانية من بدء مهمة إعادة التأهيل العصبي المحوسبة.
- بعد 30 ثانية من المنحدر الصاعد ، يبدأ التحفيز النشط أو الخدعة. تطبيق تحفيز tDCS (20 دقيقة) بشكل متزامن على مهمة إعادة التأهيل العصبي المحوسبة. بعد 20 دقيقة ، يبدأ منحدر الهبوط ويستمر لمدة 30 ثانية. بعد هذا الوقت ، يتوقف تحفيز tDCS.
- تقييم المريض بعد التدخل.
- استبيان الآثار الجانبية.
- قم بتطبيق تعديل استبيان الأحاسيس المتعلقة بالتحفيز الكهربائي عبر الجمجمة39 (الجدول 3) مع 9 أسئلة حول وجود أعراض مختلفة مثل الصداع أو الحرقان في فروة الرأس أو الحكة أو الإحساس بالوخز تحت الأقطاب الكهربائية.
- في كل عنصر ، قم بتقييم شدة الأعراض على مقياس من 1-4 وعلاقته ب tDCS على مقياس من 1-5 (انظر الجدول 3).
- موازين تناظرية بصرية للإرهاق والمزاج
- قم بتطبيق نفس المقياس المستخدم قبل جلسة التحفيز لتقييم التعب والمزاج بعد التدخل (انظر الخطوة 4.2.2).
- استبيان الآثار الجانبية.
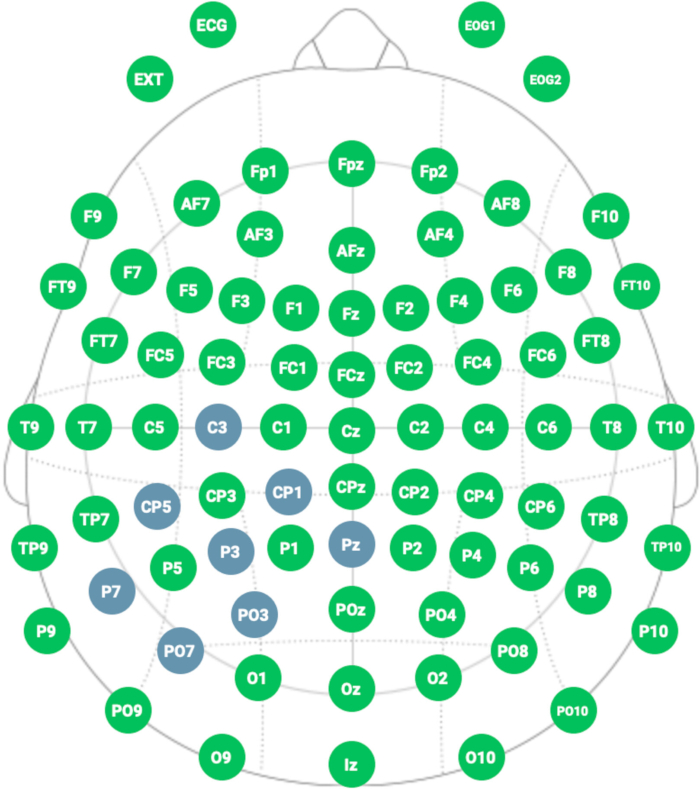
الشكل 4: مونتاج HD- tDCS التمثيلي. يوضح اللون الأزرق موقع الأقطاب الكهربائية التي تتبع النظام الدولي 10-20 لوضع القطب. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
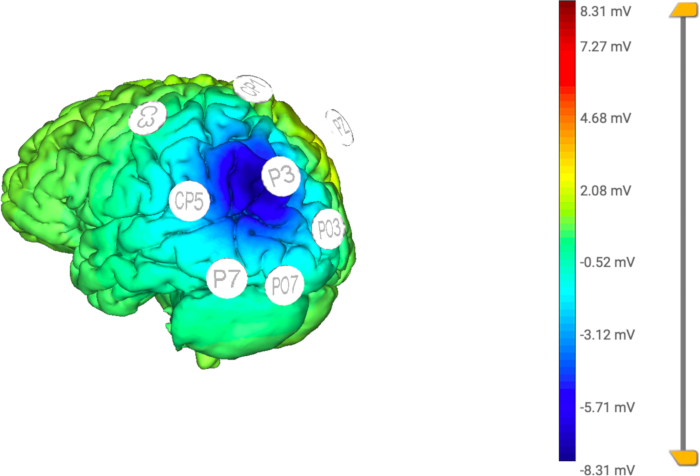
الشكل 5: النموذج الحسابي ل HD- tDCS المطبق. يتركز توزيع التيار الكهربائي في القطب المركزي (النشط) (P3) ، مما يحد من التحفيز إلى منطقة معينة بواسطة أقطاب الإرجاع (C3 ، CP5 ، CP1 ، Pz ، PO3 ، PO7 ، P7). الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 6: غطاء النيوبرين لتحفيز HD- tDCS. يحتوي الغطاء على فتحات لوضع أقطاب كهربائية باتباع نظام التصنيف 10/20 لمخطط كهربية الدماغ. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 7: جدولة المهام. المعلمات التي سيتم تحديدها عند برمجة كل مهمة في منصة إعادة التأهيل العصبي المحوسبة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
| حجز | جلسة | مهام منصة إعادة التأهيل العصبي | مدة |
| أنا | 1 و3 و6 و8 | · رسائل مخفية | 7 دقائق لكل مهمة. |
| · مجموع الأرقام | |||
| · شوربة الرسائل | |||
| · البحث عن الأشكال المطابقة | |||
| الثاني | 2 و4 و7 و9 | · نسخ مصفوفات الحروف | |
| · ولفيرين الصغير | |||
| · العثور على الأرقام المفقودة | |||
| · مقارنة النصوص | |||
| الثالث | 5 و 10 | · مقارنة النص | |
| · مجموع الأرقام | |||
| · الشره الصغير | |||
| · ابحث عن محفزات متتالية |
الجدول 2: المهام المدرجة في كل جلسة من جلسات التدخل العشر. يتم تضمين جميع المهام في منصة إعادة التأهيل العصبي المحوسبة.
| هل لديك أي من الأحاسيس أو الأعراض التالية؟ | تقدير الخطورة (1–4) | إذا وجدت: العلاقة مع tDCS؟ |
| 1-غائب | 1-لا شيء | |
| 2-خفيف | 2-جهاز التحكم عن بعد | |
| 3-معتدل | 3-ممكن | |
| 4-شديد | 4-محتمل | |
| 5-نهائي | ||
| صداع | ||
| آلام الرقبة أو عنق الرحم | ||
| ألم فروة الرأس | ||
| حرق فروة الرأس | ||
| الأحاسيس تحت القطب الكهربائي (وخز ، حكة ، حرقان ، ألم) | ||
| احمرار الجلد | ||
| خدر | ||
| مشكلة التركيز | ||
| تقلبات مزاجية حادة | ||
| أخرى (تحديد) | ||
| تعليقات إضافية | ||
الجدول 3: استبيان الآثار الجانبية tDCS. يتم توفير قائمة بالآثار الضارة التي قد تظهر بعد تطبيق التحفيز. يتم تسجيل وجود أو عدم وجود كل من هذه التأثيرات مباشرة بعد تطبيق التحفيز. تكييف استبيان الأحاسيس المتعلقة بالتحفيز الكهربائي عبر الجمجمة39.
5. إزالة tDCS
- بمجرد انتهاء برنامج تحفيز tDCS ومهام إعادة التأهيل العصبي المحوسبة ، أغلق برنامج tDCS.
- افصل جهاز tDCS.
- قم بإزالة الكبل الذي يربط tDCS بالأقطاب الكهربائية.
- قم بإزالة الغطاء من رأس المريض.
- قم بإزالة الأقطاب الكهربائية من غطاء النيوبرين.
- نظف شعر المريض.
- بعد إزالة غطاء النيوبرين ، قم بإزالة الجل المتبقي بمساعدة ورق / منشفة واغسله بالماء.
- قم بتنظيف غطاء النيوبرين tDCS والقطب الكهربائي.
- اغسل الغطاء بالماء لإزالة الجل المتبقي بعد كل جلسة واتركه يجف.
- اغسل الأقطاب الكهربائية بالماء ، وتجنب فركها ، وجففها برفق بقطعة قماش جافة. لا تستخدم أبدا الصابون أو الكحول أو غيرها من المنتجات لتنظيف الأقطاب الكهربائية.
6. التقييم العصبي النفسي والوظيفي بعد التدخل
- في يوم الاثنين، بعد الانتهاء من المداخلة، اتبع نفس الإجراء المتبع في التقييم الأولي، وإدارة نفس مهام التقييم والاستبيانات (انظر القسم 3).
النتائج
الهدف الأساسي من الدراسة الحالية هو وصف بروتوكول تدخل tDCS لتجربة سريرية متوازية وعشوائية ثلاثية التعمية. لدراسة جدوى التدخل ، تم تطبيق البروتوكول على مشارك واحد. النتائج موضحة في هذه الورقة.
طبقنا بروتوكول التدخل الكامل على رجل يبلغ من العمر 57 عاما بمستوى تعليمي عال (درجة الصحافة) أصيب بسكتة دماغية في العقد القاعدية اليمنى قبل تسعة أشهر واستوفى جميع معايير الاشتمال للمشاركة في الدراسة.
تظهر نتائج ما قبل التدخل وبعده (انظر الجدول 4 والشكل 8) لجميع المهام التي تم إجراؤها. في تقييم ما بعد التدخل لوحظت تغيرات كمية في 6 من المتغيرات ال 13 المقاسة، 4 منها مرتبطة ارتباطا مباشرا بالإهمال.
| تقييمات | ||
| ما قبل التدخل | ما بعد التدخل | |
| اختبار MMSE | 29 | 29 |
| اختبار الأجراس | 21 | 25* |
| اختبار الإلغاء | 24 | 28* |
| اختبار الرسومات | 12 | 12 |
| اختبار التقسيم | 19.95 | 3.47* |
| اختبار BTA | 11 | 9 |
| وجوه يضرب | 11 | 9 |
| أخطاء الوجه | 3 | 2* |
| اختبار الأرقام المباشرة | 11 | 10 |
| اختبار الأرقام العكسية | 9 | 8 |
| حر من المحركات | 26 | 29* |
| اختبار بارثيل | 25 | 30* |
| سي بي اس | 20 | 20 |
الجدول 4: نتائج تقييمات ما قبل التدخل وبعده. تظهر نتائج التقييم العصبي النفسي والوظيفي قبل التدخل وبعده في درجات مباشرة. *تحسينات كمية في الأداء في تقييم ما بعد التدخل مقارنة بخط الأساس. ** تشير القيم البعيدة عن الدرجة 0 إلى أداء أسوأ وإهمال أكبر.
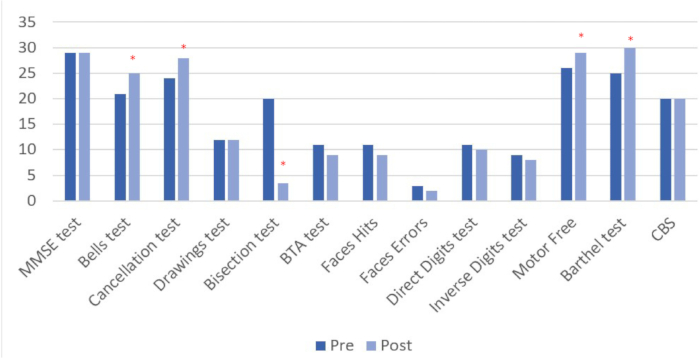
الشكل 8: نتائج تقييم ما قبل التدخل وبعده. تشير القيم الأعلى إلى التغيير الإيجابي ، باستثناء اختبار تقسيم الخط ، حيث يتم تمثيل التحسن بدرجات أقل. تظهر النتائج في الدرجات المباشرة. *تحسينات كمية في الأداء في تقييم ما بعد التدخل مقارنة بخط الأساس. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
تم حساب النسبة المئوية للتحسن بين تقييم ما قبل العلاج وبعده. لوحظ تحسن سريري في اختبارات الإهمال النصفي المكاني المحددة: اختبار الأجراس ، واختبار الإلغاء ، والتقسيم الخطي ، واختبار الإدراك البصري الخالي من المحرك ، ومقياس مؤشر بارثيل. من ناحية أخرى ، لوحظت تغييرات سلبية في المهام الانتباهية الأخرى (اختبار الأرقام ، اختبار الانتباه القصير ، اختبار الوجه). أخيرا ، لم تظهر أي تغييرات في MMSE أو نسخة الرسومات أو مقياس كاثرين بيرجيجو الوظيفي (CBS) (انظر الشكل 9).
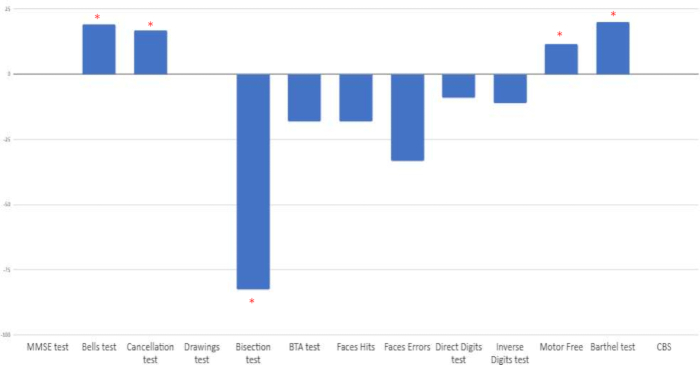
الشكل 9: النسبة المئوية للتغير بين تقييم خط الأساس وما بعد التدخل. تظهر النتائج بالنسب المئوية. تشير الدرجات الإيجابية إلى التغيير الإيجابي ، باستثناء اختبار تقسيم الخط ، حيث يتم تمثيل التحسن بدرجات سلبية. * النسبة المئوية للتحسن الإيجابي عند مقارنة تقييمات ما قبل التدخل وبعده. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
تم تنفيذ إجراءات الدراسة في غرف فسيحة مجهزة للتنفيذ الصحيح لجلسات التقييم والتدخل والامتثال لتدابير السلامة والنظافة.
أما بالنسبة للمريض ، فلم يظهر التعب في أي من جلسات ما قبل التقييم وبعده ، لذلك لم يكن من الضروري الراحة في أي منها. تم تقييم العلاج من قبل المريض على أنه ممتع ومحفز ، مما أدى إلى تحسين الالتزام بالعلاج والتعاون النشط طوال العملية. لذلك ، يعتبر أن البروتوكول سيكون له جدوى عالية ، وسنواصل الدراسة باتباع الإجراء المعمول به.
من حيث الانزعاج والآثار الجانبية ، لم يعاني المشارك من أي آثار جانبية معتدلة أو شديدة تتعلق بتطبيق tDCS.
Discussion
الإهمال النصفي المكاني هو نتيجة معرفية متكررة للسكتة الدماغية ، وعندما يستمر ، فإنه يميل إلى التأثير سلبا على فعالية عملية إعادة التأهيل. يمكن تحسين فعالية وكفاءة الأساليب العلاجية المتاحة من خلال تضمين تقنيات تحفيز الدماغ غير الغازية في إعادة التأهيل العصبي ، والبحث عن تأثير تآزري 40،41. وبالتالي ، من خلال tDCS ، يمكننا تعزيز فعالية التدخل التقليدي ، وتحقيق قدر أكبر من التعافي ، وأوقات إعادة التأهيل الأقصر ، ونتائج وظيفية أفضل في إعادة تأهيل مريض السكتة الدماغية مقارنة بالتدخل التقليدي بمعزل عن غيره. زادت الأبحاث حول إمكانات tDCS في الاضطرابات العصبية والنفسية بشكل كبير في العقد الماضي42،43،44،45،46،47،48،49.
بالإضافة, تكلفة tDCS ميسورة التكلفة, والجهاز محمول, مما يجعله قابلا للتطوير بدرجة كبيرة, السماح بتطبيقه في كل من العيادات الخارجية وإعدادات المستشفيات, مع التدريب المهني المطلوب50.
لقد وجدنا تحسنا بعد العلاج في أربعة من الاختبارات الثلاثة عشر التي تم إجراؤها (اختبار الأجراس ، اختبار الإلغاء ، تقسيم الخط ، اختبار الإدراك البصري الخالي من الحركة). ترتبط الاختبارات التي لاحظنا فيها هذه التغييرات الإيجابية بالأداء المرتبط بالإهمال النصفي المكاني. من ناحية أخرى ، لوحظ الاستقرار في أداء بعض الاختبارات المتعلقة بالأداء المعرفي العام والعمليات الانتباهية و / أو الذاكرة العاملة (MMSE ، الرسومات ، CBS). لوحظ انخفاض في أداء بعض المهام الأخرى (BTA ، الوجوه ، الأرقام المباشرة والعكسية).
فيما يتعلق بالمقاييس الوظيفية ، كان هناك دليل على التحسن ، أبلغ عنه مقدم الرعاية الأساسي وتم تقييمه بواسطة مقياس مؤشر بارثيل. كما تم إدارة المقياس الوظيفي للجنة المجتمع المركزي، الذي يرتبط ارتباطا مباشرا بتأثير الإهمال على الحياة اليومية، وفي هذه الحالة، لم يثبت أي تغيير، وظل مستقرا فيما يتعلق بالتقييم السابق. في هذه الدراسة ، وجدنا فوائد العلاج المشترك لبعض المجالات المعرفية ولكن ليس للآخرين. تتوافق هذه النتائج مع فكرة أن العلاج يمكن أن يكون أكثر فائدة لبعض مجالات الانتباه51،52،53،54،55،56،57. تظهر بعض الدراسات كيف تؤدي بروتوكولات tDCS المحددة إلى تغييرات دائمة في الاستثارة والنشاط القشري58. ولكي يتسنى تحليل الإبقاء على التغييرات بعد أسبوع، سيكون من المستحسن إجراء تقييم جديد بعد فترة زمنيةأطول 57 54 55 و56 53.
tDCS عالي الوضوح أو عالي الدقة ، المستخدم في هذه الدراسة ، هو نسخة محسنة تقنيا من tDCS تسمح بزيادة بؤرة التحفيز باستخدام حلقة من أقطاب كهربائية عائدة حول أنود أو كاثود لزيادة أو تقليل ، على التوالي ، الاستثارة القشرية بطريقة أكثر تركيزا59. بناء على هذه البؤرة العالية والتحمل السابق وتأثيرات دراسة HD-tDCS التي أجراها Borckardt et al.60 ، زاد استخدام HD-tDCS في السنوات الأخيرة.
تشير دراسات النمذجة إلى أن تكوين القطب الكهربائي هذا يولد أعلى شدة مجال كهربائي (EF) أسفل القطب المستهدف ، مع تقييد تدفق تيار الدماغ بنصف قطر إعداد الحلقة 4 × 1 ، وبالتالي ، مجال كهربائي أكبر في الهدف المحدد مقارنة بوضع القطب التقليدي60،61،62. تساهم الأقطاب الكهربائية العائدة في عزل المنطقة المستهدفة ، مما يسمح بتحفيز أكثر تركيزا للدماغ وإنتاج تأثيرات طويلة الأمد من tDCS63 التقليدية.
بالإضافة إلى ذلك ، وفقا لبعض الدراسات ، فإن HD-tDCS له تأثيرات طويلة الأمد. في الآونة الأخيرة ، كانت الأبحاث السريرية تهتم بهذا البروتوكول. على حد علمنا ، تم إجراء ست دراسات فقط مع HD-tDCS في الأمراض العصبية ، وثلاث تجارب معشاة للتحكم ، وتقريرين مفتوحي التسمية ، وتقرير حالة واحد (راجع المراجعة49).
على الرغم من عدم وجود إجماع كامل على المجالات التشريحية المتعلقة بالإهمال المكاني ، يبدو أن هناك بعض الاتفاق على بعض المجالات المحددة. يبدو أن القشرة الجدارية الخلفية هي المنطقة الرئيسية للتغيير64،65،66 ، وداخل هذه المنطقة ، التلفيف الزاوي64،65،67،68،69 ، والتلم داخل الجداري64،69،70 ، والتقاطع الصدغي69،71والتلفيف فوق الهامشي65، 72،73،74.
بالنظر إلى أن فائدة HD-tDCS مقارنة ب tDCS التقليدية تزيد من الدقة في هدف التحفيز وبناء على معرفة الموقع الدقيق لوجود الإهمال النصفي المكاني ، يمكننا أن نتوقع الحصول على فوائد أكبر من التحفيز البؤري مقارنة بالتحفيز الأكثر عمومية أو المنتشر. وفي الوقت نفسه ، فإن التكوين الأكثر استخداما في دراسات علم الأعصاب هو 4 × 1 مونتاج75،76،77،78،79. في دراستنا ، استخدمنا تكوينا 7 × 1 بهدف زيادة بؤرة التحفيز بشكل أكبر ، كونها أول دراسة تستخدم هذا المونتاج في إعادة التأهيل السريري للإهمال. لذلك ، يجب إجراء مزيد من البحث في هذه الحالة السريرية وغيرها لتحديد تفوق أو فعالية مونتاج HD-tDCS هذا على مونتاج HD الآخر و tDCS التقليدية.
فيما يتعلق بالشدة ، يتم تطبيق 2 مللي أمبير في هذا البروتوكول ، كما هو الحال في معظم الدراسات التي أجريت على tDCS ، بغض النظر عن المونتاج أو التكوين المستخدم. سيكون من المثير للاهتمام مقارنة نفس البروتوكول بكثافة أقل وأعلى في مزيد من الدراسات لمعرفة تأثير الشدة المطبقة المختلفة.
يجب أن تؤخذ بعض التوصيات المفيدة المتعلقة بالسلامة واستكشاف الأخطاء وإصلاحها الفنية في الاعتبار مع البروتوكول الحالي. في كل مريض ، وخاصة في مرضى السكتة الدماغية ، يجب تقييم مشكلات السلامة بدقة. على الرغم من أن tDCS في مرضى السكتة الدماغية آمن وجيد التحمل80 ، إلا أن المرضى وعائلاتهم لديهم أحيانا شكوك حول هذا الموضوع. وبالتالي ، يجب تسليم المعلومات المفهومة مسبقا ومناقشتها مع المريض والأقارب ، مما يضمن فهمهم للإجراء ويمكنهم التخلي عن البروتوكول وقتما يريدون.
من ناحية أخرى ، في هذا البروتوكول ، تم النظر في الموقع الدقيق للآفة وتسجيلها لأننا على استعداد لمقارنة تأثير البروتوكول على الإهمال النصفي المكاني بعد الآفات القشرية (على سبيل المثال ، الشريان الدماغي الأوسط الأيمن) 69 وبعد الآفات تحت القشرية (على سبيل المثال ، العقد القاعدية) 81. في هذا السياق ، من الأهمية بمكان تقييم فعالية التقنية في ضوء عدم التجانس في مواقع الآفة. على وجه التحديد ، نحتاج إلى تحليل الاختلافات في الفعالية فيما يتعلق بالآفات القشرية مقابل الآفات تحت القشرية.
فيما يتعلق بمرحلة السكتة الدماغية ، عند تطبيق التحفيز (الحاد أو تحت الحاد أو المزمن) ، من المهم معرفة اللحظة التي يمكن أن يكون فيها التدخل أكثر فائدة. في هذه الدراسة ، استخدمنا كمعيار إدراج بعد 3 إلى 12 شهرا من الإصابة (المرحلة تحت الحادة). ومع ذلك ، ركزت مراجعة منهجية سابقة على الجوانب الحركية بعد السكتة الدماغية ، وأظهرت النتائج تحسنا في المراحل المزمنة ولكن ليس في المرحلة الحادة (خلال الأيام الثلاثة الأولى من ظهور الأعراض)82. من الضروري إجراء مزيد من التحقيق لاستكشاف فوائد tDCS على التغيرات المعرفية بعد السكتة الدماغية وتحديد العوامل التي تتنبأ بفعاليته المثلى عبر مراحل التعافي المختلفة.
تدعم المعرفة الحالية حول HD-tDCS كنهج علاجي في الأمراض العصبية قدرتها على التحمل والفعالية السريرية. إلى جانب ذلك ، هناك حاجة إلى مزيد من البحث العشوائي الخاضع للرقابة لمعرفة المعلمات المثلى في كل مرض وكل مريض من أجل إثبات فعالية تقنية تحفيز الدماغ غير الغازية هذه في الاضطرابات العصبية وما بعدها.
Disclosures
المؤلفون ليس لديهم ما يكشفون عنه.
Acknowledgements
نشكر NeuronUp (www.neuronup.com) على دعمها وتعاونها المتفاني في هذا المشروع.
Materials
| Name | Company | Catalog Number | Comments |
| 10 electrode cable | Neuroelectrics | NE017 | |
| Barthel Index | N/A | Mahoney, F. I., Barthel, D. W. Functional evaluation: The Barthel Index. Md State Med J. 14, 61–65 (1965). | |
| Copy of drawings subtest | N/A | https://test-barcelona.com/es/tienda.html | J. Peña Casanova, Programa integrado de exploración neuropsicológica: test Barcelona revisado?: TBR. Barcelona: Masson. |
| Curved Syrenge | Neuroelectrics | NE014 | |
| Electrode Gel | Neuroelectrics | NE016a | |
| Line bisection test | N/A | Schenkenberg, T., Bradford, D. C., Ajax, E. T. Line bisection and unilateral visual neglect in patients with neurologic impairment. Neurology. 30 (5) 509–517 (1980). | |
| Mini-mental state examination (MMSE) | N/A | Folstein, M. F., Folstein, S. E., McHugh, P. R. “Mini-mental state”. A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. 12 (3) 189–198 (1975). | |
| Neoprene headcap | Neuroelectrics | NE019-M | |
| Saline Solution | Neuroelectrics | NE033 | |
| Satrstim Necbox | Neuroelectrics | NE012 | |
| Starstim tES-EEG System | Neuroelectrics | ||
| Teastboard Cable | Neuroelectrics | NE039 | |
| Testboard Head | Neuroelectrics | NE038 | |
| The Bell Test | N/A | https://strokengine.ca/en/assessments/bells-test/ | L. Gauthier, F. Deahault and Y. Joanette, The Bells Test: A quantitative and qualitative test for visual neglect (Vol. 11). |
| The Catherine Bergego Scale | N/A | Azouvi, P. et al. Behavioral assessment of unilateral neglect: study of the psychometric properties of the Catherine Bergego Scale. Arch Phys Med Rehabil. 84 (1) 51–57 (2003). | |
| The motor-free visual perception test (MVPT) | N/A | https://www.wpspublish.com/mvpt-4-motor-free-visual-perception-test-4 | Colarusso, R. P., Hammill, D.D. The Motor Free Visual Perception Test (MVPT-3). Navato, CA: Academic Therapy Publications (2003). |
| USB Bluetooth Dongle | Neuroelectrics | NE031 | |
| USB charging Cable | Neuroelectrics | NE043 | |
| USB Power Adapter & Power Supply Plug | Neuroelectrics | NE013 & NE013a, NE013b, NE013c | |
| USB Stick with Manuals & NIC SW | Neuroelectrics | NE015 |
References
- Sun, J. -H., Tan, L., Yu, J. -T. Post-stroke cognitive impairment: epidemiology, mechanisms and management. Ann Transl Med. 2 (8), 80(2014).
- Abo, M., et al. comparative study of NEURO versus CIMT in poststroke patients with upper limb hemiparesis: the neuro-verify study. Int J Stroke. 9 (5), 607-612 (2014).
- Mijajlović, M. D., et al. Post-stroke dementia - a comprehensive review. BMC Med. 15 (1), 11(2017).
- Kerkhoff, G., Schenk, T. Rehabilitation of neglect: an update. Neuropsychologia. 50 (6), 1072-1079 (2012).
- Jehkonen, M., et al. Predictors of discharge to home during the first year after right hemisphere stroke. Acta Neurol Scand. 104 (3), 136-141 (2001).
- Buxbaum, L. J., et al. Hemispatial neglect: subtypes, neuroanatomy, and disability. Neurology. 62 (5), 749-756 (2004).
- Nijboer, T. C. W., Kollen, B. J., Kwakkel, G. Time course of visuospatial neglect early after stroke: a longitudinal cohort study. Cortex. 49 (8), 2021-2027 (2013).
- Ringman, J. M., Saver, J. L., Woolson, R. F., Clarke, W. R., Adams, H. P. Frequency, risk factors, anatomy, and course of unilateral neglect in an acute stroke cohort. Neurology. 63 (3), 468-474 (2004).
- Parton, A., Malhotra, P., Husain, M. Hemispatial neglect. J Neurol Neurosurg Psychiatry. 75 (1), 13-21 (2004).
- Stone, S. P., Patel, P., Greenwood, R. J., Halligan, P. W. Measuring visual neglect in acute stroke and predicting its recovery: the visual neglect recovery index. J Neurol Neurosurg Psychiatry. 55 (6), 431(1992).
- Chen, P., Hreha, K., Kong, Y., Barrett, A. M. Impact of spatial neglect on stroke rehabilitation: evidence from the setting of an inpatient rehabilitation facility. Arch Phys Med Rehabil. 96 (8), 1458-1466 (2015).
- Wilkinson, D., Sakel, M., Camp, S. -J., Hammond, L. Patients with hemispatial neglect are more prone to limb spasticity, but this does not prolong their hospital stay. Arch Phys Med Rehabil. 93 (7), 1191-1195 (2012).
- Gammeri, R., Iacono, C., Ricci, R., Salatino, A. Unilateral spatial neglect after stroke: current insights. Neuropsychiatr Dis Treat. 16, 131-152 (2020).
- Muñoz-Marrón, E., Redolar-Ripoll, D., Zulaica-Cardoso, A. New therapeutic approaches in the treatment of neglect: transcranial magnetic stimulation. Rev Neurol. 55 (5), 297-305 (2012).
- Cicerone, K. D., et al. Evidence-based cognitive rehabilitation: systematic review of the literature from 2009 through 2014. Arch Phys Med Rehabil. 100 (8), 1515-1533 (2009).
- Pizzamiglio, L., et al. Cognitive rehabilitation of the hemineglect disorder in chronic patients with unilateral right brain damage. J Clin Exp Neuropsychol. 14 (6), 901-923 (1992).
- Yi, Y., et al. The effect of transcranial direct current stimulation on neglect syndrome in stroke patients. Ann Rehabil Med. 40 (2), 223-229 (2016).
- Fregni, F., Pascual-Leone, A. Technology insight: noninvasive brain stimulation in neurology-perspectives on the therapeutic potential of rTMS and tDCS. Nat Rev Neurol. 3 (7), 383-393 (2007).
- Lefaucheur, J. -P., et al. Evidence-based guidelines on the therapeutic use of transcranial direct current stimulation (tDCS). Clin Neurophysiol. 128 (1), 56-92 (2017).
- González-Rodriguez, B., Serradell-Ribé, N., Viejo-Sobera, R., Romero-Muñoz, J. P., Marron, E. M. Transcranial direct current stimulation in neglect rehabilitation after stroke: a systematic review. J Neurol. 269 (12), 6310-6329 (2022).
- Kinsbourne, M. A model for the mechanism of unilateral neglect of space. Trans Am Neurol Assoc. 95, 143-146 (1970).
- Kinsbourne, M. Hemi-neglect and hemisphere rivalry. Adv Neurol. 18, 41-49 (1977).
- Koch, I. Instruction effects in task switching. Psychon Bull Rev. 15 (2), 448-452 (2008).
- Corbetta, M., Kincade, M. J., Lewis, C., Snyder, A. Z., Sapir, A. Neural basis and recovery of spatial attention deficits in spatial neglect. Nat Neurosci. 8 (11), 1603-1610 (2005).
- Hummel, F. C., Cohen, L. G. Noninvasive brain stimulation: a new strategy to improve neurorehabilitation after stroke. Lancet Neurol. 5 (8), 708-712 (2006).
- Miniussi, C., et al. Efficacy of repetitive transcranial magnetic stimulation/transcranial direct current stimulation in cognitive neurorehabitation. Brain Stimul. 1 (4), 326-336 (2008).
- Bornheim, S., Maquet, P., Croisier, J., Crielaard, J., Kaux, J. Motor cortex transcranial direct current stimulation (tDCS) improves acute stroke visuo-spatial neglect: a series of four case reports. Brain Stimul. 11 (2), 459-461 (2018).
- Sunwoo, H., et al. Effects of dual transcranial direct current stimulation on post-stroke unilateral visuospatial neglect. Neurosci Lett. 554, 94-98 (2013).
- Ladavas, E., et al. A-tDCS on the ipsilesional parietal cortex boosts the effects of prism adaptation treatment in neglect. Restor Neurol Neurosci. 33 (5), 647-662 (2015).
- Turgut, N., Miranda, M., Kastrup, A., Eling, P., Hildebrandt, H. tDCS combined with optokinetic drift reduces egocentric neglect in severely impaired post-acute patients. Neuropsychol Rehabil. 28 (4), 515-526 (2018).
- Smit, M., et al. Transcranial direct current stimulation to the parietal cortex in hemispatial neglect: a feasibility study. Neuropsychologia. 74, 152-161 (2015).
- Brem, A. -K., Unterburger, E., Speight, I., Jancke, L. Treatment of visuospatial neglect with biparietal tDCS and cognitive training: a single-case study. Front Syst Neurosci. 8, 180-180 (2014).
- Cappon, D., Jahanshahi, M., Bisiacchi, P. Value and efficacy of transcranial direct current stimulation in the cognitive rehabilitation: a critical review since 2000. Front Neurosci. 10, 157(2016).
- Fan, J., Li, Y., Yang, Y., Qu, Y., Li, S. Efficacy of noninvasive brain stimulation on unilateral neglect after stroke: a systematic review and meta-analysis. Am J Phys Med Rehabil. 97 (4), 261-269 (2018).
- Kashiwagi, F. T., et al. Noninvasive brain stimulations for unilateral spatial neglect after stroke: a systematic review and meta-analysis of randomized and nonrandomized controlled trials. Neural Plast. , (2018).
- Salazar, A. P. S., et al. Noninvasive brain stimulation improves hemispatial neglect after stroke: a systematic review and meta-analysis. Arch Phys Med Rehabil. 99 (2), 355-366 (2018).
- Zebhauser, P. T., Vernet, M., Unterburger, E., Brem, A. -K. Visuospatial neglect-a theory-informed overview of current and emerging strategies and a systematic review on the therapeutic use of noninvasive brain stimulation. Neuropsychol Rev. 29 (4), 397-420 (2019).
- Bikson, M., et al. Safety of transcranial direct current stimulation: evidence based update 2016. Brain Stimul. 9 (5), 641-661 (2016).
- Antal, A., et al. Low intensity transcranial electric stimulation: safety, ethical, legal regulatory and application guidelines. Clin Neurophysiol. 128 (9), 1774-1809 (2017).
- Sathappan, A. V., Luber, B. M., Lisanby, S. H. The dynamic duo: combining noninvasive brain stimulation with cognitive interventions. Prog Neuropsychopharmacol Biol Psychiatry. 89, 347-360 (2019).
- Draaisma, L. R., Wessel, M. J., Hummel, F. C. Noninvasive brain stimulation to enhance cognitive rehabilitation after stroke. Neurosci Lett. 719, 133678(2020).
- David, M. C. M. M., Moraes, A. A., de Costa, M. L., da Franco, C. I. F. Transcranial direct current stimulation in the modulation of neuropathic pain: a systematic review. Neurol Res. 40 (7), 557-565 (2018).
- Dondé, C., et al. Transcranial direct-current stimulation (tDCS) for bipolar depression: a systematic review and meta-analysis. Prog Neuropsychopharmacol Biol Psychiatry. 78, 123-131 (2017).
- Gowda, S. M., et al. Efficacy of pre-supplementary motor area transcranial direct current stimulation for treatment resistant obsessive compulsive disorder: a randomized, double blinded, sham controlled trial. Brain Stimul. 12 (4), 922-929 (2019).
- Kang, N., Summers, J. J., Cauraugh, J. H. Transcranial direct current stimulation facilitates motor learning post-stroke: a systematic review and meta-analysis. J Neurol Neurosurg Psychiatry. 87 (4), 345-355 (2016).
- Narayanaswamy, J. C., et al. Successful application of add-on transcranial direct current stimulation (tDCS) for treatment of SSRI resistant OCD. Brain Stimul. 8 (3), 655-657 (2015).
- Osoegawa, C., et al. Noninvasive brain stimulation for negative symptoms in schizophrenia: an updated systematic review and meta-analysis. Schizophr Res. 197, 34-44 (2018).
- Vacas,, et al. Noninvasive brain stimulation for behavioural and psychological symptoms of dementia: a systematic review and meta-analysis. Int J Geriatr Psychiatry. 34 (9), 1336-1345 (2019).
- Parlikar, R., et al. High definition transcranial direct current stimulation (HD-tDCS): a systematic review on the treatment of neuropsychiatric disorders. Asian J Psychiatry. 56, 102542(2021).
- Fried, P. J., et al. Training in the practice of noninvasive brain stimulation: recommendations from an IFCN committee. Clin Neurophysiol. 132 (3), 819-837 (2021).
- Cappa, S. F., et al. EFNS guidelines on cognitive rehabilitation: report of an EFNS task force. Eur J Neurol. 12 (9), 665-680 (2005).
- Sturm, W., Willmes, K., Orgass, B., Hartje, W. Do specific attention deficits need specific training. Neuropsychol Rehabil. 7 (2), 81-103 (1997).
- Verveer, I., Remmerswaal, D., Van der Veen, F. M., Franken, I. H. A. Long-term tDCS effects on neurophysiological measures of cognitive control in tobacco smokers. Biol Psychol. 156, 107962(2020).
- Katz, B., et al. Individual differences and long-term consequences of tDCS-augmented cognitive training. J Cogn Neurosci. 29 (9), 1498-1508 (2017).
- Gu, J., et al. The effect and mechanism of transcranial direct current stimulation on episodic memory in patients with mild cognitive impairment. Front Neurosci. 16, 811403(2022).
- Zhou, Y., et al. Efficacy and safety of transcranial direct current stimulation (tDCS) on cognitive function in chronic schizophrenia with tardive dyskinesia (TD): a randomized, double-blind, sham-controlled, clinical trial. BMC Psychiatry. 23 (1), 623(2023).
- Au, J., et al. Enhancing working memory training with transcranial direct current stimulation. J Cogn Neurosci. 28 (9), 1419-1432 (2016).
- Stagg, C. J., Antal, A., Nitsche, M. A. Physiology of transcranial direct current stimulation. J ECT. 34 (3), 144-152 (2018).
- Da Silva Machado, D. G., et al. Acute effect of high-definition and conventional tDCS on exercise performance and psychophysiological responses in endurance athletes: a randomized controlled trial. Sci Rep. 11, 13911(2021).
- Borckardt, J. J., et al. A pilot study of the tolerability and effects of high-definition transcranial direct current stimulation (HD-tDCS) on pain perception. J Pain. 13 (2), 112-120 (2012).
- Villamar, M. F., et al. Technique and considerations in the use of 4x1 ring high-definition transcranial direct current stimulation (HD-tDCS). J Vis Exp. (77), e50309(2013).
- Effects of electrode configurations and injected current intensity on the electrical field of transcranial direct current stimulation: a simulation study. Mackenbach, C., Tian, R., Yang, Y. Annu Int Conf IEEE Eng Med Biol Soc, , 3517-3520 (2020).
- Bikson, M., Datta, A., Rahman, A., Scaturro, J. Electrode montages for tDCS and weak transcranial electrical stimulation: role of "return" electrode's position and size. Clin Neurophysiol. 121 (12), 1976-1978 (2010).
- Chambers, C. D., Stokes, M. G., Mattingley, J. B. Modality-specific control of strategic spatial attention in parietal cortex. Neuron. 44 (6), 925-930 (2004).
- Chambers, C. D., Payne, J. M., Mattingley, J. B. Parietal disruption impairs reflexive spatial attention within and between sensory modalities. Neuropsychologia. 45 (8), 1715-1724 (2007).
- Chambers, C. D., Mattingley, J. B. Neurodisruption of selective attention: insights and implications. Trends Cogn Sci. 9 (11), 542-550 (2005).
- Rushworth, M. F., Ellison, A., Walsh, V. Complementary localization and lateralization of orienting and motor attention. Nat Neurosci. 4 (6), 656-661 (2001).
- Hillis, A. E., et al. Anatomy of spatial attention: insights from perfusion imaging and hemispatial neglect in acute stroke. J Neurosci. 25 (12), 3161-3167 (2005).
- Mort, D. J., et al. The anatomy of visual neglect. Brain. 126 (9), 1986-1997 (2003).
- Mannan, S. K., et al. Revisiting previously searched locations in visual neglect: role of right parietal and frontal lesions in misjudging old locations as new. J Cogn Neurosci. 17 (2), 340-354 (2005).
- Vallar, G. Extrapersonal visual unilateral spatial neglect and its neuroanatomy. Neuroimage. 14 (1 Pt 2), S52-S58 (2001).
- Oliveri, M., Vallar, G. Parietal versus temporal lobe components in spatial cognition: setting the mid-point of a horizontal line. J Neuropsychol. 3 (2), 201-211 (2009).
- Committeri, G., et al. Neural bases of personal and extrapersonal neglect in humans. Brain. 130 (Pt 2), 431-441 (2007).
- Doricchi, F., Tomaiuolo, F. The anatomy of neglect without hemianopia: a key role for parietal-frontal disconnection. Neuroreport. 14 (17), 2239-2243 (2003).
- Fiori, V., Nitsche, M. A., Cucuzza, G., Caltagirone, C., Marangolo, P. High-definition transcranial direct current stimulation improves verb recovery in aphasic patients depending on current intensity. Neuroscience. 406, 159-166 (2019).
- Karvigh, S. A., Motamedi, M., Arzani, M., Roshan, J. H. N. HD-tDCS in refractory lateral frontal lobe epilepsy patients. Seizure. 47, 74-80 (2017).
- Meiron, O., et al. Antiepileptic effects of a novel noninvasive neuromodulation treatment in a subject with early-onset epileptic encephalopathy: case report with 20 sessions of HD-tDCS intervention. Front Neurosci. 13, (2019).
- Reckow, J., et al. Tolerability and blinding of 4x1 high-definition transcranial direct current stimulation (HD-tDCS) at two and three milliamps. Brain Stimul. 11 (5), 991-997 (2018).
- Motes, M. A., et al. High-definition transcranial direct current stimulation to improve verbal retrieval deficits in chronic traumatic brain injury. J Neurotrauma. 37 (1), 170-177 (2020).
- Russo, C., Souza Carneiro, M. I., Bolognini, N., Fregni, F. Safety review of transcranial direct current stimulation in stroke. Neuromodulation. 20 (3), 215-222 (2017).
- Hochstenbach, J., Van Spaendonck, K. P., Cools, A. R., Horstink, M. W., Mulder, T. Cognitive deficits following stroke in the basal ganglia. Clin Rehabil. 12 (6), 514-520 (1998).
- Marquez, J., Van Vliet, P., McElduff, P., Lagopoulos, J., Parsons, M. Transcranial direct current stimulation (tDCS): does it have merit in stroke rehabilitation? A systematic review. Int J Stroke. 10 (3), 306-316 (2015).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved