É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Criobiópsia pulmonar transbrônquica para diagnóstico de doenças pulmonares intersticiais e lesões pulmonares periféricas - uma abordagem passo a passo
Neste Artigo
Resumo
A criobiópsia pulmonar transbrônquica (TBLC) para o diagnóstico de doença pulmonar intersticial e lesões pulmonares periféricas é um procedimento diagnóstico seguro e de alto rendimento. Descrevemos uma abordagem passo a passo para conduzir TBLC para as diferentes indicações mencionadas com um broncoscópio flexível, o que pode ser útil para broncoscopistas novatos que realizam TBLC.
Resumo
A criobiópsia pulmonar transbrônquica (TBLC) é um procedimento invasivo cada vez mais implementado durante a última década como uma alternativa à biópsia pulmonar (BLS) de cirurgia torácica videoassistida para o diagnóstico de doenças pulmonares intersticiais (DPIs). A indicação para TBLC tem sido principalmente subclassificar um subtipo específico de DPI quando isso não pode ser alcançado com base em uma discussão anterior da equipe multidisciplinar. Embora a BLS seja considerada o padrão-ouro para estabelecer um diagnóstico histológico, a TBLC tem sido gradualmente sugerida como a modalidade diagnóstica histológica de primeira escolha em pacientes com DPIs não classificadas devido a um rendimento diagnóstico comparável ao da BLS, mas superior à BLS em termos de complicações, incluindo mortalidade. Nos últimos anos, o TCLB guiado por ultrassom endobrônquico radial (R-EBUS) e broncoscopia eletromagnética de navegação (ENB) para lesões pulmonares periféricas também foram descritos como procedimentos seguros, o que pode melhorar o rendimento diagnóstico em comparação com as biópsias com fórceps. Ainda assim, as propriedades diagnósticas do TBLC dependem da qualidade do desempenho do procedimento. Este artigo tem como objetivo descrever a abordagem gradual para a realização de TBLC com um broncoscópio flexível para as diferentes indicações mencionadas, o que pode ser útil para broncoscopistas novatos que realizam TBLC.
Introdução
As doenças pulmonares intersticiais (DPIs) constituem um grupo de doenças pulmonares agudas e crônicas que afetam um ou mais de todos os componentes do parênquima pulmonar que formam o interstício, como brônquios, alvéolos, tecido conjuntivo e vasos sanguíneos e linfáticos. Apesar de serem doenças raras, os mais de 200 subtipos diferentes de DPIs representam uma categoria heterogênea de doenças com diferentes características clínicas, radiológicas e cito-histológicas. As DPIs geralmente se manifestam como inflamação, fibrose ou uma combinação de ambas, que são as causas subjacentes para os sintomas percebidos usuais pelos pacientes, como tosse seca, dispneia aos esforços e fadiga 1,2.
As DPIs são categorizadas como pneumonia intersticial idiopática (PII), pneumonia intersticial de etiologia conhecida (por exemplo, doença do tecido conjuntivo, doença pulmonar intersticial, DPI induzida por drogas e pneumoconiose relacionada ao trabalho), afecção intersticial granulomatosa (por exemplo, sarcoidose e pneumonia por hipersensibilidade) e DPIs órfãs (por exemplo, múltiplas doenças pulmonares císticas e pneumonia eosinofílica)1. Essa categorização e posterior subtipagem diagnóstica são fundamentais para determinar o tratamento e o acompanhamento ideais, além de permitir o prognóstico. No entanto, como o quebra-cabeça diagnóstico pode ser desafiador, recomenda-se a interpretação das informações clínicas (incluindo anamnese, disposição e exposições potenciais) e paraclínicas disponíveis, como tomografia computadorizada de alta resolução (TCAR) de tórax, fisiologia pulmonar e autoimunologia obtidas com base em uma discussão de equipe multidisciplinar (MDD) 3,4,5. Se um diagnóstico confiante de TDM não for possível obter 6,7, a amostragem histológica para aumentar a probabilidade de um diagnóstico definitivo do subtipo de DPI é indicada pelo uso de criobiópsia pulmonar transbrônquica (TBLC)8,9. Em pacientes bem selecionados, a CPBT é considerada um procedimento invasivo seguro com acurácia diagnóstica próxima à da biópsia pulmonar (BLS) de cirurgia torácica videoassistida, que ainda é considerada o padrão-ouro histológico para o diagnóstico histológico de DPI 10,11,12,13,14. O procedimento TBLC é realizado como uma broncoscopia sistemática, aplicando-se crioprobes especiais para amostragem histológica e com orientação fluoroscópica recomendada. Recomenda-se que a TBLC seja realizada em centros terciários de DPI usando um ambiente de MDD e por pneumologistas intervencionistas familiarizados com o manejo de complicações da TBLC, que passaram por treinamento em um centro dedicado com experiência em TBLC 9,10,11,15,16,17.
A TBLC também ganhou atenção recentemente como um procedimento a ser combinado com a ultrassonografia endobrônquica radial (R-EBUS) para o diagnóstico de DPI18,19. Além disso, a TBLC foi combinada com R-EBUS e broncoscopia de navegação eletromagnética (ENB) para o diagnóstico de lesões pulmonares periféricas (LPP) para melhorar o rendimento diagnóstico quando comparada às biópsias transbrônquicas convencionais20,21. No entanto, essa abordagem relativamente nova para o diagnóstico de PPL ainda não foi implementada como um procedimento padrão e, portanto, justifica mais evidências nessa área específica. O objetivo do presente relato é descrever uma abordagem gradual para a realização de TBLC com um broncoscópio flexível em um ambiente clínico para as indicações mencionadas.
Protocolo
Os autores vêm de dois centros TBLC dinamarqueses (Hospital Universitário de Odense e Hospital Universitário de Aarhus) que realizam pesquisas de acordo com os princípios da Declaração de Helsinque. A aprovação ética não foi necessária, pois o estudo era de natureza observacional. Todos os pacientes incluídos para fins de pesquisa assinaram o termo de consentimento livre e esclarecido. É importante enfatizar que a abordagem stepwise descrita para a condutância TBLC está relacionada ao uso de um broncoscópio flexível e é baseada em uma combinação de recomendações de diretrizes internacionais, declarações de especialistas, revisões do estado da arte e experiências dos dois centros TBLC 9,10,11,15,16,17,22,23,24 ,25.
1. Considerações sobre pré-TBLC
- Certifique-se de que a TBLC seja indicada, o que se justifica em pacientes nos quais a integração de informações de TCAR, bioquímica e autoimunologia em um TDM anterior envolvendo pneumologistas e radiologistas não foi capaz de estabelecer um diagnóstico confiável de DPI.
- Selecione os pacientes apropriados, evitando as contraindicações descritas na Tabela 1.
| Contra-indicações relativas | Contra-indicações absolutas |
| Capacidade vital forçada (CVF) < 50% do valor previsto | Trombocitopenia < 50 x 109/L ou INR > 1,5 |
| A capacidade de difusão do monóxido de carbono para o pulmão (DLCO) < 35% do valor previsto | Diátese hemorrágica não corrigida |
| A pressão arterial pulmonar sistólica > 50 mmHg (por exemplo, estimativa baseada em um ecocardiograma) | Declínio progressivo e clínico devido ao aumento do risco de complicações em pacientes com função pulmonar comprometida |
| Índice de massa corporal > 35 kg/m2 |
Tabela 1: Contraindicações para TBLC. Contra-indicações relativas e absolutas para a condutância TBLC. Abreviatura: TBLC = criobiópsia pulmonar transbrônquica.
2. Preparação pré-TBLC
- Revise a TCAR e as sugestões do radiologista torácico para planejar a partir de qual amostragem histológica dos segmentos brônquicos (BS) é mais acessível de acordo com a manifestação radiológica da doença.
- Teste se o sistema funciona antes do desempenho do TBLC.
- Pressione o botão de capacidade do tanque de gás (dióxido de carbono (CO2) ou óxido nitroso (NO)) no painel de configurações para verificar o volume do gás no cilindro.
- Coloque a criossonda em uma bandeja e observe a sonda enquanto pressiona o pedal do pedal por 5 a 10 s. Procure uma bola de gelo na ponta da sonda que indique que ela está funcionando corretamente (Figura 1).
- Use anestesia geral (GA) ou sedação profunda sob TBLC e considere a pré-medicação com ácido tranexâmico de 0.5-1 g para reduzir o risco de sangramento.
- Coloque um tubo endotraqueal luminal duplo (TET) especial de 7,5-8,5 mm de tamanho na traqueia.
NOTA: O TET possui um canal principal que permite o acesso ao broncoscópio enquanto o paciente está ventilado e possui um canal lateral menor que serve como canal de trabalho para o cateter bloqueador brônquico.- Pulverize continuamente com anestesia local (por exemplo, spray de lidocaína 10%) para reduzir a tosse. Consulte também a etapa 3.5.
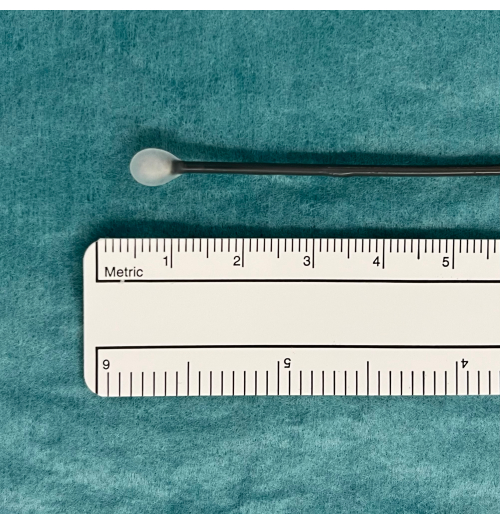
Figura 1: Uma bola de gelo como indicação de equipamento TBLC utilizável. Um pedal ativa a difusão do gás CO2 do tanque e o congelamento induzido. Isso é testado em água, onde uma bola de gelo aparecerá na ponta da criossonda se estiver funcionando corretamente. Abreviatura: TBLC = criobiópsia pulmonar transbrônquica. Clique aqui para ver uma versão maior desta figura.
3. Condutância TBLC
- Introduzir um broncoscópio flexível através do TET e realizar o procedimento de broncoscopia.
NOTA: Um broncoscópio rígido é usado em alguns centros TBLC para intubar a traqueia. Se a traqueia for intubada por um broncoscópio rígido, um broncoscópio flexível pode ser passado através do broncoscópio rígido.- Introduza a criossonda flexível através do canal de trabalho do broncoscópio e no BS selecionado.
NOTA: As criogravas ocorrem como sondas de uso único (1.1, 1.7 e 2.4 mm) e sondas reutilizáveis (1.9 e 2.4 mm). - Use fluoroscopia para garantir que a colocação da ponta da criossonda esteja a aproximadamente 10 mm da parede do tórax, correspondendo ao BS selecionado (Figura 2).
- Introduza um cateter bloqueador brônquico (por exemplo, um balão de Fogarty) no canal lateral do TET luminal duplo e coloque-o no óstio BS selecionado (Figura 3).
- Encha o cateter bloqueador brônquico para avaliar a adequação da colocação e bloqueio para possível sangramento que ocorra distalmente em relação ao balão (Figura 4).
- Desinfle o cateter bloqueador brônquico se o balão estiver bem colocado.
- Fixe a colocação do balão fixando o cateter bloqueador brônquico com um pean.
- Use pequenas quantidades de spray de lidocaína ou solução salina no respectivo TET e seu canal lateral para reduzir qualquer atrito experimentado devido à introdução da criossonda no TET e do cateter balão no canal lateral do TET.
- Quando as etapas 3.1.1-3.1.3 forem executadas satisfatoriamente, pise no pedal de congelamento por 3-6 s, dependendo do tamanho da criossonda, para explorar a lei de Joule-Thompsons para congelar o tecido do parênquima pulmonar a aproximadamente -45-79 ° C para CO2 e -89 ° C para NO.
- Retraia o broncoscópio flexível que contém a criossonda em um movimento rápido enquanto mantém o pedal de congelamento pressionado para continuar o congelamento e evitar que a biópsia caia durante a retração.
- Durante a manobra descrita na etapa 3.1.5, peça a uma pessoa que não seja o broncoscopista que mantenha o balão inflado para bloquear o local da biópsia distal do óstio BS selecionado para controlar o sangramento potencial.
- Introduza a criossonda flexível através do canal de trabalho do broncoscópio e no BS selecionado.
- Continue a etapa 3.1.6 até que pelo menos duas biópsias de dois BS do mesmo lobo sejam obtidas.
- Colocar as biópsias em soro fisiológico e, quando todas as biópsias forem obtidas, fixá-las em formol (4%) (Figura 5).
- Envie as biópsias para exame patológico antes do TDM.
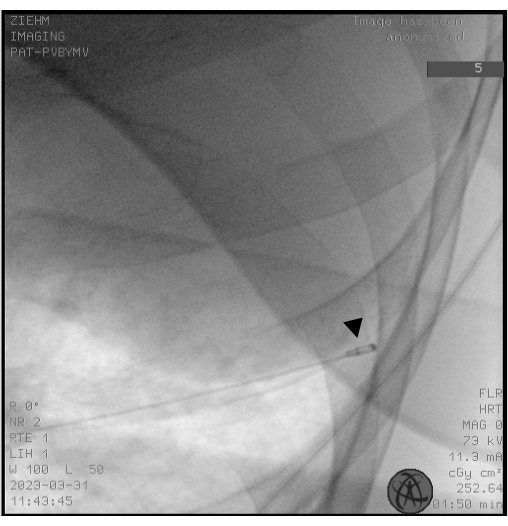
Figura 2: Fluoroscopia. A fluoroscopia é usada para garantir a colocação correta da criossonda antes do congelamento. A ponta da criossonda aparece como a cabeça de uma baqueta (ponta de seta preta). Clique aqui para ver uma versão maior desta figura.
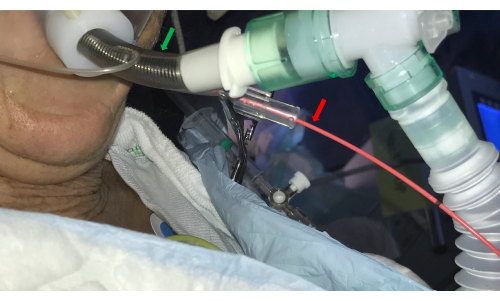
Figura 3: Tubo endotraqueal. Um tubo endotraqueal de dupla luminal (seta verde) permite o acesso às vias aéreas pelo broncoscópio e, simultaneamente, controla o sangramento pela introdução de um cateter-balão no canal lateral (seta vermelha). Clique aqui para ver uma versão maior desta figura.

Figura 4: Insuflação do cateter-balão. Insuflação do cateter balão para garantir o bloqueio e evitar possíveis sangramentos distais do balão distribuindo-se para outras partes do lobo após a realização de uma criobiópsia pulmonar transbrônquica. Clique aqui para ver uma versão maior desta figura.
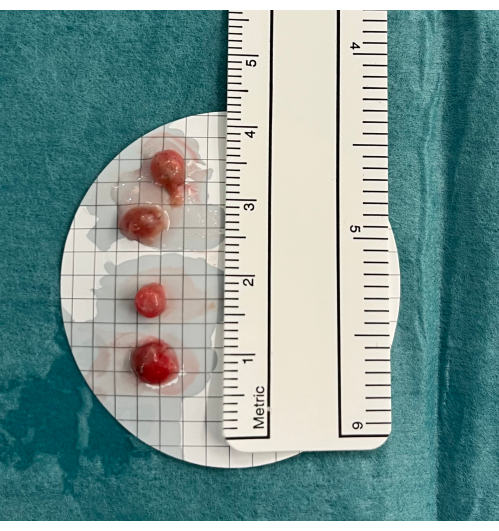
Figura 5: Biópsias. As criobiópsias pulmonares transbrônquicas são colocadas em solução salina fria antes da fixação em formaldeído. Clique aqui para ver uma versão maior desta figura.
4. Procedimentos pós-TBLC
- Após cada biópsia, reintroduza o broncoscópio no BS e esvazie o balão para observar se ocorre sangramento.
- Volte a inflar o balão se for observado sangramento (Figura 6). Se o balão estiver na posição correta e bloquear o BS, aguarde alguns minutos para que o sangramento pare e, em seguida, continue o procedimento TBLC.
- Se ainda for observada hemorragia após o passo 4.1.1., instale solução salina gelada distalmente ao balão.
- Em caso de hemorragia contínua após o passo 4.1.2. ou falha do balão em que o sangue é derramado em outros BSs, use uma combinação de sucção, solução salina gelada administrada endobrônquica com ou sem adrenalina e ácido tranexâmico.
- Se o sangue coagulado bloquear as vias aéreas, use a criossonda para abrir as vias aéreas novamente, congelando a ponta da criossonda no coágulo sanguíneo e retraindo-o através do TET.
- Se o sangramento permanecer descontrolado, troque o TET por um que permita a ventilação do pulmão não biopsiado e o bloqueio do brônquio principal no pulmão com sangramento e transfira o paciente para uma unidade de terapia intensiva.
- Realize um ultrassom pulmonar focalizado (FLUS) após TBLC, enquanto o paciente ainda está sedado para identificar os indicativos de um pneumotórax iatrogênico (PTX).
- Considere a inserção de um dreno pleural guiado por FLUS com um cateter pigtail (Fr 7-16) se as observações do FLUS indicarem uma alta probabilidade de PTX. A drenagem pleural é indicada se o FLUS indicar um tamanho crescente de PTX e, especialmente, se o estado clínico do paciente estiver se deteriorando.
- Adie a extubação em 5-10 min se o FLUS revelar um PTX pequeno e o paciente estiver clinicamente estável. Se o tamanho do PTX progredir a partir de agora ou o paciente se tornar clinicamente instável, insira um dreno pleural antes da extubação.
- Extubar o paciente após a etapa 4.2 ou 4.2.2 se não houver indicação de PTX ou progresso do tamanho da PTX e o paciente permanecer clinicamente estável.
- Observe o paciente em uma sala de recuperação após TBLC. Pouco antes de o paciente clinicamente estável ir para casa, certifique-se de que o PTX de início tardio não esteja presente por FLUS repetido ou por uma radiografia de tórax.
- Discuta a apresentação das características histológicas das biópsias em um MDD subsequente com pneumologistas, radiologistas e patologistas em conjunto com outros detalhes para concluir um subtipo de DPI com alta probabilidade diagnóstica.
- Informe o paciente sobre a conclusão do TDM da etapa 4.5 no ambulatório e planeje o possível tratamento e acompanhamento.
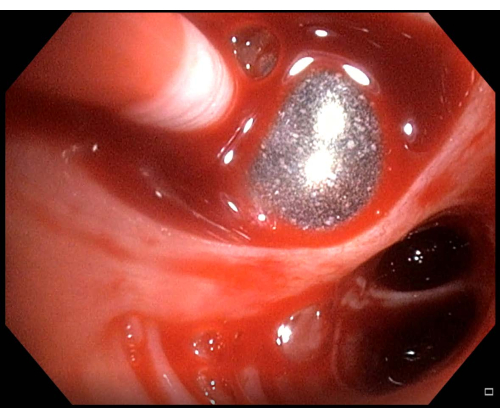
Figura 6: Sangramento menor. Se for observado sangramento após a realização de uma criobiópsia pulmonar transbrônquica, neste caso, sangramento menor, o cateter-balão deve ser mantido inflado alguns minutos antes de tentar novamente a desinflação. Clique aqui para ver uma versão maior desta figura.
5. TBLC em conjunto com R-EBUS e ENB para diagnósticos de PPL
- Navegue e confirme a localização da lesão pulmonar periférica.
- Insira a criossonda de 1.1 mm no canal de trabalho estendido sob a orientação de fluoroscopia.
- Combine a ponta da sonda de congelamento com a posição da sonda EBUS radial.
- Pise no pedal de congelamento por 4-8 s.
- Retraia a criossonda através do canal de trabalho estendido em um movimento rápido enquanto mantém o pedal de congelamento pressionado para continuar o congelamento e evitar que a biópsia caia durante a retração.
- Mantenha o broncoscópio e o canal de trabalho estendido na posição enquanto a criossonda é retraída.
- Repita as etapas 5.2-5.4 até que um número suficiente de biópsias seja obtido.
- Manuseie as biópsias conforme descrito nas etapas 3.3 e 3.4.
Resultados
Com base nas observações dos autores de dois centros de TBLC, o procedimento stepwise descrito para TBLC com um broncoscópio flexível permitiu a amostragem histológica em pacientes dinamarqueses bem selecionados com subtipos de DPI ainda não diagnosticados, apesar do TDM anterior. Observações detalhadas dessas coortes são relatadas em dois estudos publicados recentemente23,25 e para o centro do primeiro autor resumidos n...
Discussão
Independentemente da indicação de CPBT, suas propriedades diagnósticas dependem da qualidade do desempenho do procedimento e dos critérios selecionados para a realização do procedimento. Isso enfatiza a recomendação de implementar um programa de treinamento formal e certificado para adquirir as competências necessárias para realizar um procedimento padronizado de TBLC. Apesar do fato de que atualmente não é possível obter educação oficial sobre TBLC, a recente diretriz da ...
Divulgações
Os autores não têm conflitos de interesse a divulgar.
Agradecimentos
Os autores gostariam de agradecer ao pessoal dos Departamentos de Cirurgia Torácica e Anestesiologia da Enfermaria de Broncoscopia do Hospital Universitário de Odense, Dinamarca, por sua ajuda na preparação dos números para este artigo.
Materiais
| Name | Company | Catalog Number | Comments |
| "Chimney" for tube | |||
| CO2 gas bottle adapter | |||
| CO2 gas tank | Erbe | ||
| Endoscopy column | |||
| Endotracheal tube, size 7.5-8.5 mm | Erbe | ||
| Erbecryo pedal footswitch | Erbe | ||
| Erbecryo2 workstation | Erbe | ||
| Flexible bronchoscope | |||
| Flexible gas hose | Mediland | ||
| Flexible single use cryoprobe, OD 1.1 mm | Erbe | ||
| Flexible single use cryoprobe, OD 1.7 mm | Erbe | ||
| Flexible single use cryoprobe, OD 2.4 mm | |||
| Fluoroscope | |||
| Fogarty balloon catheter | |||
| Formalin glasses in closed system | |||
| NaCl incl. cold NaCl | |||
| Pean for fixating Fogarty balloon | |||
| Sterile disposable cup | |||
| Sterile suction tube | |||
| Sterile tweesers | |||
| Syringe for Fogarty balloon inflation/deflation | |||
| Table bag for flouroscope | |||
| Three way tap for Fogarty balloon syringe | |||
| Tracheal suction | |||
| Ultrasound machine | Erbe | ||
| Valve for biopsy chanel | |||
| Valve to suction duct |
Referências
- Travis, W. D., et al. An official American Thoracic Society/European Respiratory Society statement: Update of the international multidisciplinary classification of the idiopathic interstitial pneumonias. American Journal of Respiratory and Critical Care Medicine. 188 (6), 733-748 (2013).
- Ruaro, B., et al. Editorial: Pulmonary fibrosis: One manifestation, various diseases. Frontiers in Pharmacology. 13, 1027332 (2022).
- Lamas, D. J., et al. Delayed access and survival in idiopathic pulmonary fibrosis: a cohort study. American Journal of Respiratory and Critical Care Medicine. 184 (7), 842-847 (2011).
- Tomassetti, S., Piciucchi, S., Tantalocco, P., Dubini, A., Poletti, V. The multidisciplinary approach in the diagnosis of idiopathic pulmonary fibrosis: a patient case-based review. European Respiratory Review. 24 (135), 69-77 (2015).
- Walsh, S. L. F., et al. Multicentre evaluation of multidisciplinary team meeting agreement on diagnosis in diffuse parenchymal lung disease: a case-cohort study. Lancet Respiratory Medicine. 4 (7), 557-565 (2016).
- Ryerson, C. J., et al. A standardized diagnostic ontology for fibrotic interstitial lung disease. An International Working Group perspective. American Journal of Respiratory and Critical Care Medicine. 196 (10), 1249-1254 (2017).
- Cottin, V., et al. Integrating clinical probability into the diagnostic approach to idiopathic pulmonary fibrosis: An International Working Group perspective. American Journal of Respiratory and Critical Care Medicine. 206 (3), 247-259 (2022).
- Rodrigues, I., et al. Diagnostic yield and safety of transbronchial lung cryobiopsy and surgical lung biopsy in interstitial lung diseases: a systematic review and meta-analysis. European Respiratory Review. 31 (166), 210280 (2022).
- Korevaar, D. A., et al. European Respiratory Society guidelines on transbronchial lung cryobiopsy in the diagnosis of interstitial lung diseases. European Respiratory Journal. 60 (5), 2200425 (2022).
- Colella, S., Haentschel, M., Shah, P., Poletti, V., Hetzel, J. Transbronchial lung cryobiopsy in interstitial lung diseases: best practice. Respiration. 95 (6), 383-391 (2018).
- Hetzel, J., et al. Transbronchial cryobiopsies for the diagnosis of diffuse parenchymal lung diseases: expert statement from the Cryobiopsy Working Group on safety and utility and a call for standardization of the procedure. Respiration. 95 (3), 188-200 (2018).
- Ravaglia, C., Poletti, V. Transbronchial lung cryobiopsy for the diagnosis of interstitial lung diseases. Current Opinion in Pulmonary Medicine. 28 (1), 9-16 (2022).
- Troy, L. K., et al. Diagnostic accuracy of transbronchial lung cryobiopsy for interstitial lung disease diagnosis (COLDICE): a prospective, comparative study. Lancet Respiratory Medicine. 8 (2), 171-181 (2020).
- Ruaro, B., et al. Transbronchial lung cryobiopsy and pulmonary fibrosis: A never-ending story. Heliyon. 9 (4), e14768 (2023).
- Lentz, R. J., Argento, A. C., Colby, T. V., Rickman, O. B., Maldonado, F. Transbronchial cryobiopsy for diffuse parenchymal lung disease: a state-of-the-art review of procedural techniques, current evidence, and future challenges. Journal of Thoracis Disease. 9 (7), 2186-2203 (2017).
- Maldonado, F., et al. Transbronchial cryobiopsy for the diagnosis of interstitial lung diseases: CHEST Guideline and Expert Panel Report. Chest. 157 (4), 1030-1042 (2020).
- Avasarala, S. K., Wells, A. U., Colby, T. V., Maldonado, F. Transbronchial cryobiopsy in interstitial lung diseases: State-of-the-art review for the interventional pulmonologist. Journal of Bronchology Interventional Pulmonology. 28 (1), 81-92 (2021).
- Abdelghani, R., Thakore, S., Kaphle, U., Lasky, J. A., Kheir, F. Radial Endobronchial Ultrasound-guided Transbronchial Cryobiopsy. Journal of Bronchology Interventional Pulmonology. 26 (4), 245-249 (2019).
- Inomata, M., et al. Utility of radial endobronchial ultrasonography combined with transbronchial lung cryobiopsy in patients with diffuse parenchymal lung diseases: a multicentre prospective study. BMJ Open Respiratory Research. 8 (1), e000826 (2021).
- Benn, B. S., Gmehlin, C. G., Kurman, J. S., Doan, J. Does transbronchial lung cryobiopsy improve diagnostic yield of digital tomosynthesis-assisted electromagnetic navigation guided bronchoscopic biopsy of pulmonary nodules? A pilot study. Respiratory Medicine. 202, 106966 (2022).
- Ankudavicius, V., Miliauskas, S., Poskiene, L., Vajauskas, D., Zemaitis, M. Diagnostic yield of transbronchial cryobiopsy guided by radial endobronchial ultrasound and fluoroscopy in the radiologically suspected lung cancer: A single institution prospective study. Cancers. 14 (6), 1563 (2022).
- Ravaglia, C., et al. Transbronchial lung cryobiopsy in diffuse parenchymal lung disease: Comparison between biopsy from 1 segment and biopsy from 2 segments - diagnostic yield and complications. Respiration. 93 (4), 285-292 (2017).
- Davidsen, J. R., Skov, I. R., Louw, I. G., Laursen, C. B. Implementation of transbronchial lung cryobiopsy in a tertiary referral center for interstitial lung diseases: a cohort study on diagnostic yield, complications, and learning curves. BMC Pulmonary Medicine. 21 (1), 67 (2021).
- Laursen, C. B., et al. Lung ultrasound assessment for pneumothorax following transbronchial lung cryobiopsy. ERJ Open Research. 7 (3), 00045-2021 (2021).
- Kronborg-White, S., et al. Integration of cryobiopsies for interstitial lung disease diagnosis is a valid and safe diagnostic strategy-experiences based on 250 biopsy procedures. Journal of Thoracic Disease. 13 (3), 1455-1465 (2021).
- Barisione, E., et al. Competence in transbronchial cryobiopsy. Panminerva Medica. 61 (3), 290-297 (2019).
- Raghu, G., et al. Idiopathic pulmonary fibrosis (an update) and progressive pulmonary fibrosis in adults: An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. American Journal of Respiratory and Critical Care Medicine. 205 (9), e18-e47 (2022).
- Ravaglia, C., et al. Diagnostic yield and risk/benefit analysis of trans-bronchial lung cryobiopsy in diffuse parenchymal lung diseases: a large cohort of 699 patients. BMC Pulmonary Medicine. 19 (1), 16 (2019).
- Hernandez-Gonzalez, F., et al. Cryobiopsy in the diagnosis of diffuse interstitial lung disease: yield and cost-effectiveness analysis. Archivos de Bronconeumología. 51 (6), 261-267 (2015).
- Cooley, J., et al. Safety of performing transbronchial lung cryobiopsy on hospitalized patients with interstitial lung disease. Respiratory Medicine. 140, 71-76 (2018).
- Hetzel, J., et al. Transbronchial cryobiopsy increases diagnostic confidence in interstitial lung disease: a prospective multicenter trial. European Respiratory Journal. 56 (6), 1901520 (2020).
- Kheir, F., et al. Transbronchial lung cryobiopsy in patients with interstitial lung disease: a systematic review. Annals of the American Thoracic Society. 19 (7), 1193-1202 (2022).
- Walscher, J., et al. Transbronchial cryobiopsies for diagnosing interstitial lung disease: real-life experience from a tertiary referral center for interstitial lung disease. Respiration. 97 (4), 348-354 (2019).
- Gnass, M., et al. Transbronchial lung cryobiopsy guided by radial mini-probe endobronchial ultrasound in interstitial lung diseases - a multicenter prospective study. Advances in Respiratory Medicine. 88 (2), 123-128 (2020).
- Ma, X., et al. Global and regional burden of interstitial lung disease and pulmonary sarcoidosis from 1990 to 2019: results from the Global Burden of Disease study 2019. Thorax. 77 (6), 596-605 (2022).
- Kronborg-White, S., et al. A pilot study on the use of the super dimension navigation system for optimal cryobiopsy location in interstitial lung disease diagnostics. Pulmonology. 29 (2), 119-123 (2021).
- Wijmans, L., et al. Confocal laser endomicroscopy as a guidance tool for transbronchial lung cryobiopsies in interstitial lung disorder. Respiration. 97 (3), 259-263 (2019).
- Kheir, F., et al. Using bronchoscopic lung cryobiopsy and a genomic classifier in the multidisciplinary diagnosis of diffuse interstitial lung diseases. Chest. 158 (5), 2015-2025 (2020).
- Renzoni, E. A., Poletti, V., Mackintosh, J. A. Disease pathology in fibrotic interstitial lung disease: is it all about usual interstitial pneumonia. Lancet. 398 (10309), 1437-1449 (2021).
- Chaudhary, S., et al. Interstitial lung disease progression after genomic usual interstitial pneumonia testing. European Respiratory Journal. 61 (4), 2201245 (2023).
- Raghu, G., et al. Use of a molecular classifier to identify usual interstitial pneumonia in conventional transbronchial lung biopsy samples: a prospective validation study. Lancet Respiratory Medicine. 7 (6), 487-496 (2019).
- Kheir, F., et al. Use of a genomic classifier in patients with interstitial lung disease: a systematic review and meta-analysis. Annals of American Thoracic Society. 19 (5), 827-832 (2022).
- Glenn, L. M., Troy, L. K., Corte, T. J. Novel diagnostic techniques in interstitial lung disease. Frontiers in Medicine. 10, 1174443 (2023).
- Kim, S. H., et al. The additive impact of transbronchial cryobiopsy using a 1.1-mm diameter cryoprobe on conventional biopsy for peripheral lung nodules. Cancer Research and Treatment. 55 (2), 506-512 (2023).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados