12.11 : الأسموزية والضغط الأسموزي للمحاليل
يُظهر عدد من المواد الطبيعية والاصطناعية نفاذية انتقائية، مما يعني أن الجزيئات أو الأيونات ذات الحجم والشكل والقطبية والشحنة المعينة وما إلى ذلك هي فقط القادرة على المرور عبر (اختراق) المادة. أغشية الخلايا البيولوجية تقديم أمثلة أنيقة للنفاذ الانتقائي في الطبيعة، في حين أن أنابيب غسيل الكلى المستخدمة لإزالة النفايات الاستقلابية من الدم هي مثال تكنولوجي أكثر بساطة. وبغض النظر عن كيفية تصنيعها، يُشار إلى هذه المواد عمومًا باسم أغشية شبه منفذة.
ضع في اعتبارك جهازاً على شكل حرف U، حيث يتم فصل عينات من المذيب النقي عن المحلول بغشاء يمكن أن تتخلل جزيئات المذيب فقط. سوف تنتشر جزيئات المذيب عبر الغشاء في كلا الاتجاهين. نظرًا لأن تركيز المذيب أكبر في المذيب النقي من المحلول، فإن هذه الجزيئات ستنتشر من جانب المذيب من الغشاء إلى جانب المحلول بمعدل أسرع مما هو عليه في الاتجاه العكسي. والنتيجة هي النقل الصافي لجزيئات المذيب من المذيب النقي إلى المحلول. يُعرف النقل المدفوع بالانتشار لجزيئات المذيبات عبر غشاء شبه نافذ باسم التناضح.
عندما يتم إجراء الأسموزية في جهاز موصوف أعلاه، يزداد حجم المحلول حيث يصبح مخففاً بتراكم المذيب. يؤدي هذا إلى ارتفاع مستوى المحلول ، مما يزيد من ضغطه الهيدروستاتيكي (بسبب وزن عمود المحلول في الأنبوب) وينتج عنه نقل أسرع لجزيئات المذيب إلى جانب المذيب النقي. عندما يصل الضغط إلى قيمة ينتج عنها معدل نقل مذيب عكسي يساوي معدل التناضح ، يتوقف النقل السائب للمذيب. يسمى هذا الضغط الضغط الأسموزي (Π) من المحلول. يرتبط الضغط الأسموزي لمحلول مخفف بمولارية المذاب، M، ودرجة الحرارة المطلقة، T، وفقاً للمعادلة
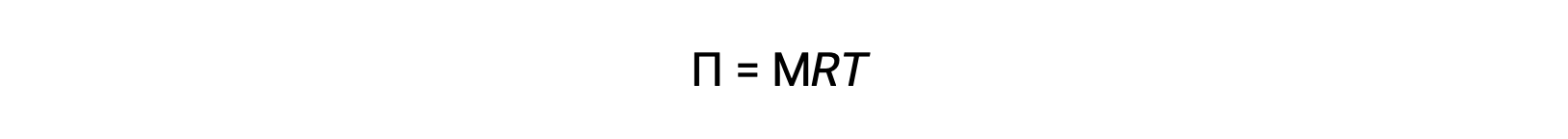
حيث R هو ثابت الغاز العام.
إذا تم وضع محلول في مثل هذا الجهاز، فإن الضغط الذي يزيد عن الضغط الأسموزي للمحلول يعكس عملية التناضح ويدفع جزيئات المذيب من المحلول إلى المذيب النقي. تُستخدم تقنية التناضح العكسي هذه في تحلية مياه البحر على نطاق واسع وعلى نطاقات أصغر لإنتاج مياه الصنبور عالية النقاء للشرب.
هذا النص مقتبس من Openstax, Chemistry 2e, Section 11.4: Colligative Properties.
From Chapter 12:

Now Playing
12.11 : الأسموزية والضغط الأسموزي للمحاليل
Solutions and Colloids
38.8K Views

12.1 : تشكيل المحاليل
Solutions and Colloids
31.0K Views

12.2 : القوى بين الجزيئات في المحاليل
Solutions and Colloids
32.8K Views

12.3 : المحتوى الحراري للمحلول
Solutions and Colloids
24.5K Views

12.4 : المحاليل المائية ودرجات حرارة الماء
Solutions and Colloids
14.2K Views

12.5 : توازن المحلول والتشبّع
Solutions and Colloids
18.3K Views

12.6 : الخصائص الفيزيائية التي تؤثّر على الذوبان
Solutions and Colloids
22.3K Views

12.7 : التعبير عن تركيز المحلول
Solutions and Colloids
58.0K Views

12.8 : تخفيض ضغط البخار
Solutions and Colloids
25.8K Views

12.9 : المحاليل المثالية
Solutions and Colloids
18.9K Views

12.10 : انحدار نقطة التجمّد وارتفاع نقطة الغليان
Solutions and Colloids
33.9K Views

12.12 : الاليكتروليت: عامل فانت هوف
Solutions and Colloids
32.6K Views

12.13 : الغرويات
Solutions and Colloids
17.2K Views
Copyright © 2025 MyJoVE Corporation. All rights reserved